Clear Sky Science · ru
NR6A1 необходим для спецификации, образования и выживания клеток нервного гребня
Как ранние клеточные решения формируют лицо и тело
До нашего рождения особая группа клеток, называемая клетками нервного гребня, перемещается по эмбриону, помогая формировать лицо, сердце, нервы и другие структуры. Когда эти клетки функционируют неверно, у новорождённых могут возникать серьёзные пороки развития. В этом исследовании раскрыт ранее недооценённый молекулярный переключатель — белок NR6A1, который помогает определить, когда и где в эмбрионе млекопитающих формируются клетки нервного гребня, и что происходит при сбое этого переключателя.
Блуждающие строители эмбриона
Клетки нервного гребня возникают очень рано в развитии вдоль границы формирующегося мозга и спинного мозга. Отделившись от этой ткани, они мигрируют на большие расстояния, формируя разнообразные структуры — от костей и хрящей лица до частей периферической нервной системы и пигментных клеток кожи. Поскольку они вносят вклад во многие органы, даже небольшие нарушения их образования могут вызывать широкий спектр заболеваний, называемых нейрокристопатиями, включая краниофациальные синдромы вроде синдрома Тречера Коллинза. Понимание того, как эти клетки появляются впервые, поэтому имеет ключевое значение для объяснения как нормального развития, так и врождённых дефектов.
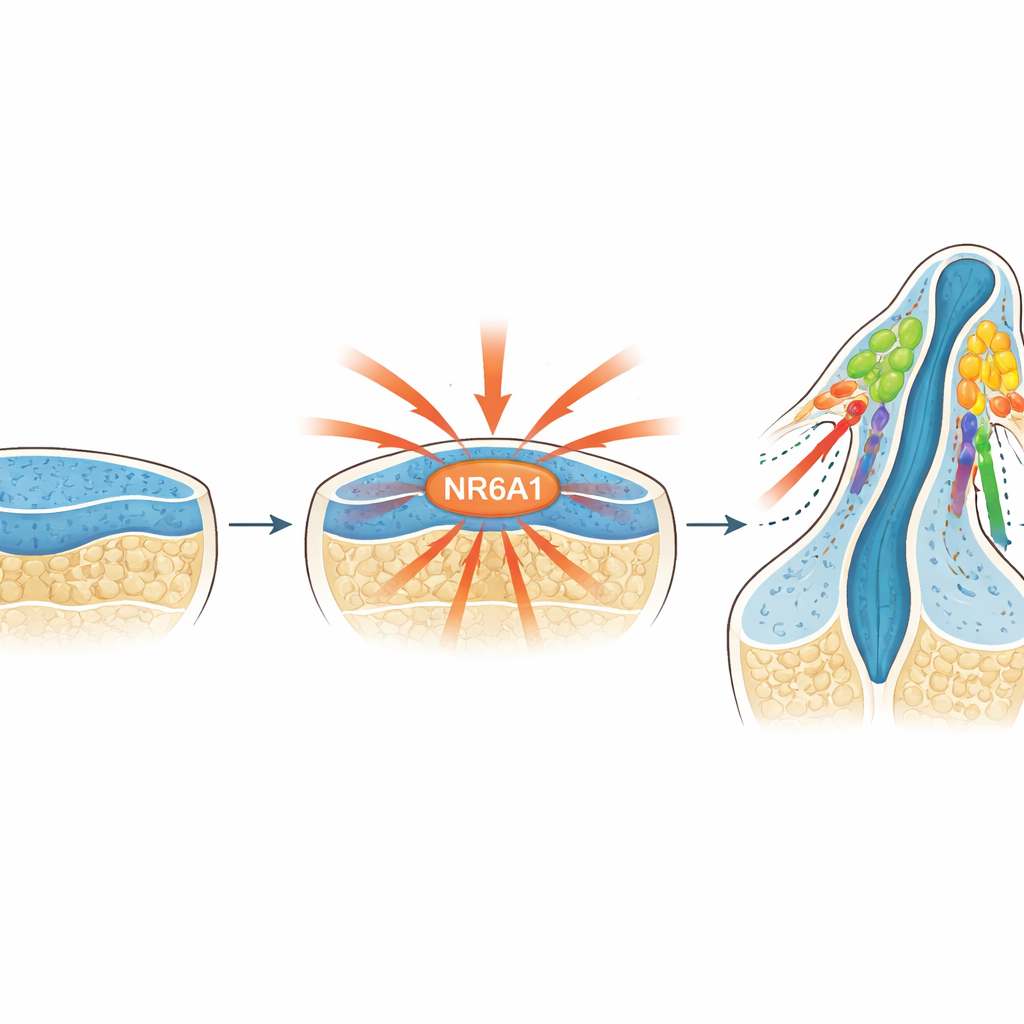
Новопроявленный главный переключатель
Исследователи сосредоточились на NR6A1, члене семейства ядерных рецепторов — белков, управляющих активностью генов. Ранние работы намекали, что NR6A1 может быть связан с дефектами головы и лица, но его роль в клетках нервного гребня была неизвестна. Отслеживая NR6A1 в эмбрионах мыши с момента имплантации и далее, команда обнаружила, что его присутствие тесно коррелирует с местом и временем появления клеток нервного гребня: он появляется в ранней нервной ткани, концентрируется вдоль дорсальной (задней) стороны развивающегося мозга и спинного мозга и также наблюдается в клетках в момент их отрыва от этой ткани для начала миграции.
Что происходит, когда переключатель отсутствует
Мыши, полностью лишённые NR6A1, погибают на ранних стадиях развития, поэтому исследователи изучали эмбрионы незадолго до этой точки. Они наблюдали серьёзную нехватку клеток нервного гребня, особенно позади первой дуги, из которой формируются части челюсти и шеи, где мигрирующие клетки нервного гребня были почти полностью отсутствуют. Ключевые генетические программы, которые обычно маркируют идентичность нервного гребня и позволяют клеткам отделяться и двигаться, были резко ослаблены. В то же время гены, сохраняющие клетки в стволоподобном, активно пролиферирующем состоянии, оставались включёнными, и многие образовавшиеся клетки, похожие на клетки нервного гребня, вскоре погибали. Эти результаты указывают, что без NR6A1 нервные стволовые клетки не способны правильно перейти в мигрирующие клетки нервного гребня и не выживают.
Отключение «стволовости» и включение подвижности
Чтобы понять, как NR6A1 осуществляет этот контроль, авторы объединили несколько мощных молекулярных методов, включая секвенирование РНК по отдельным клеткам, картирование доступности хроматина и целевые анализы связывания ДНК с белками как на моделях мыши, так и в производных человеческих стволовых клеток клетках нервного гребня. Они обнаружили, что NR6A1 физически связывается с определёнными ДНК-мотивами рядом с генами, управляющими двумя противоположными программами: одной, поддерживающей плюрипотентность (способность дать начало множеству типов клеток), и другой, запускающей идентичность клеток нервного гребня и их движение. В присутствии NR6A1 хроматин в окрестностях генов «стволовости», таких как Oct4 и Nanog, становится менее доступным и эти гены приглушаются, в то время как области рядом с генами нервного гребня и эпителиально-мезенхимального перехода становятся более открытыми и активными. Переэкспрессия Oct4 в критическое окно формирования нервного гребня имитировала утрату NR6A1, дополнительно показывая, что «стволовость» должна быть заглушена для появления клеток нервного гребня.
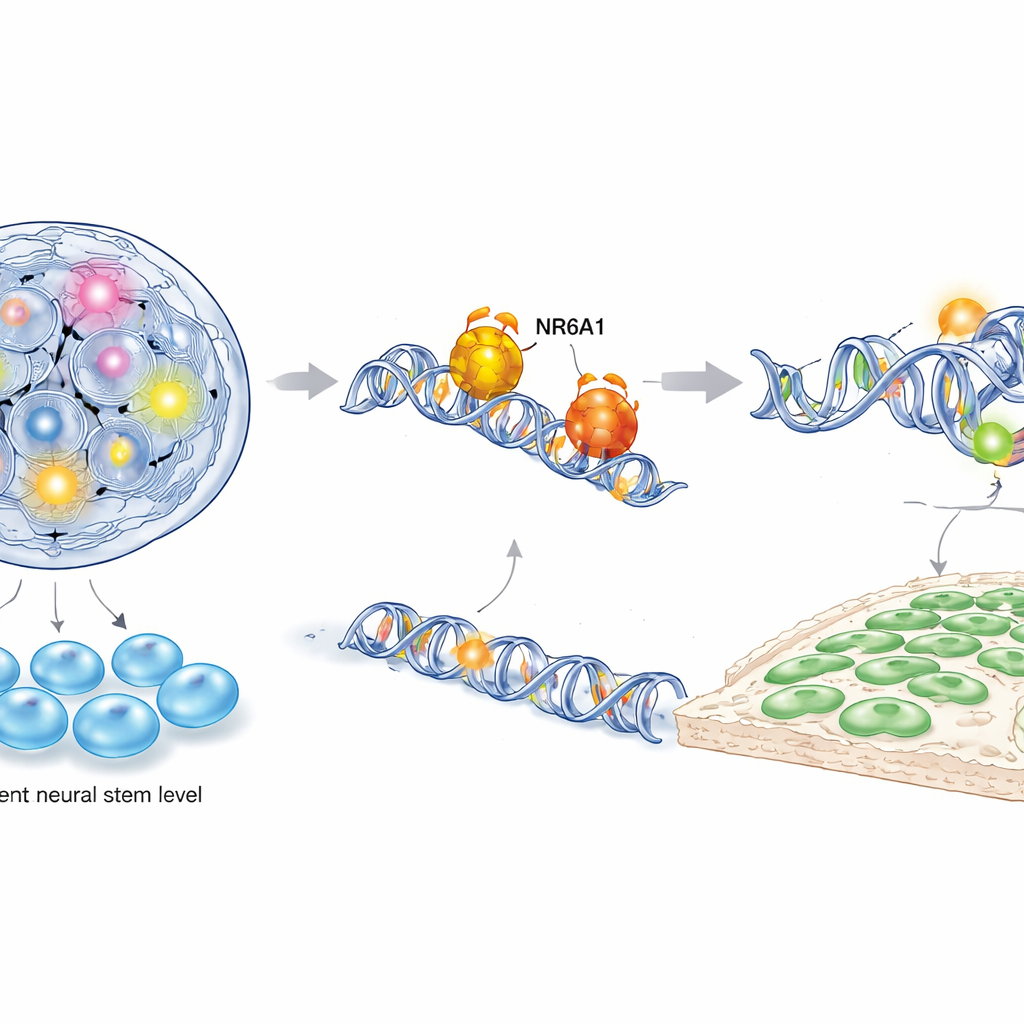
Переписывание временной шкалы раннего развития
Исследование также пересматривает хронологию начала спецификации клеток нервного гребня у млекопитающих. С помощью индуцируемой генетической системы для удаления NR6A1 в разные моменты команда показала, что удаление его к середине гаструляции — стадии, более ранней, чем обычно считалось — было достаточным, чтобы заблокировать активацию генов нервного гребня. Напротив, удаление NR6A1 позже, в том числе с использованием широко применяемой линии-драйвера, специфичной для нервного гребня, не вызывало заметных дефектов. Это означает, что ключевые решения о судьбе нервного гребня принимаются до того, как начинают действовать стандартные инструменты, что объясняет, почему некоторые предыдущие исследования на мышах могли пропустить ранние требования.
Почему это важно для врождённых дефектов и болезней
В совокупности работа показывает NR6A1 как центральный координатор, который помогает нервным стволовым клеткам «повзрослеть» в клетки нервного гребня, одновременно выключая программы плюрипотентности и включая программы миграции и выживания. Это двойное действие, по-видимому, начинается в середине гаструляции, раньше, чем считалось ранее у млекопитающих, и приближает развитие мыши к другим позвоночным. Уточняя, когда и как действует этот переключатель, исследование даёт основу для переосмысления ранних генетических экспериментов, поиска более подходящих инструментов для изучения биологии нервного гребня и, в конечном счёте, для понимания и потенциального предотвращения нейрокристопатий, возникающих при сбоях в этом раннем развитии.
Цитирование: Moore Zajic, E.L., Muñoz, W.A., Dennis, J.F. et al. NR6A1 is essential for neural crest cell specification, formation and survival. Nat Commun 17, 2140 (2026). https://doi.org/10.1038/s41467-026-68647-2
Ключевые слова: клетки нервного гребня, NR6A1, эмбриональное развитие, переключатель плюрипотентности, нейрокристопатия