Clear Sky Science · ru
Проектирование системы MmeFz2-ωRNA для эффективного редактирования генома с помощью интегрированной вычислительно-экспериментальной платформы
Меньшие «генные ножницы» для крупных медицинских задач
Редактирование генома уже изменило подходы учёных к изучению болезней, но превращение этой технологии в безопасное и практичное лечение остаётся серьёзной проблемой. Одно из главных препятствий — то, что сегодняшние самые мощные «ножницы» для ДНК, такие как CRISPR‑Cas9, физически велики и тяжело помещаются в крошечные доставочные носители, используемые у пациентов. В этом исследовании представлен новый компактный инструмент для редактирования генома, созданный на основе малоизвестного семейства ферментов Fanzor2, и показано, как искусственный интеллект может быстро переработать его в перспективный кандидат для будущих генетических терапий.
Новый класс компактных редакторов генома
Большинство современных редакторов генома, например Cas9 и Cas12a, — это громоздкие белки, состоящие из более тысячи аминокислотных звеньев. Их размер затрудняет упаковку в адено‑ассоциированные вирусы (AAV), ведущую платформу доставки для генотерапий. Напротив, белки Fanzor2 существенно меньше и естественно встречаются в эукариотах — ветви жизни, включающей животных и человека. Авторы сосредоточились на одном представителе этого семейства, MmeFz2, который использует короткую молекулу РНК, называемую ωRNA, чтобы находить и разрезать определённые ДНК‑последовательности. На бумаге MmeFz2 выглядел идеальным для терапии: компактный и программируемый. На практике же его активность в человеческих клетках была крайне низкой — редактирование происходило менее чем в одном проценте целевых сайтов. Команда поставила цель превратить этот недостаточно эффективный фермент в практичный инструмент.
Использование ИИ для переработки направляющей молекулы
Первой целью стала ωRNA — направляющая, указывающая MmeFz2, где резать. С помощью AlphaFold3, передовой программы для предсказания трёхмерных структур белково‑РНК‑ДНК комплексов, исследователи построили модель MmeFz2 в сочетании с ωRNA и ДНК‑мишенью. Виртуальная структура показала, что части ωRNA были гибкими, плохо парными и слабо контактировали с белком. Ориентируясь на эту информацию, команда систематически замещала нестабильные участки РНК и удаляла серии уридиновых оснований, которые могут мешать транскрипции. Затем они протестировали десятки вариантов в человеческих клетках. Скомбинировав лучшие изменения и укоротив ненужную стеблевую область, они создали укороченную ωRNA, ставшую на 30% короче, но обеспечившую почти 20‑кратное увеличение эффективности редактирования по множеству ДНК‑сайтов.
Тонкая настройка белка с помощью машинного обучения
Далее команда дорабатывала сам белок. Снова используя AlphaFold3, они картировали области контакта MmeFz2 с РНК и ДНК и спроектировали более сотни одиночных замен аминокислот, направленных на усиление этих контактов или улучшение гибкости. Протестировав эти варианты в клетках, они передали данные о производительности в EVOLVEpro — систему машинного обучения, основанную на языковых моделях белков, обученных на миллионах естественных последовательностей. Этот инструмент выявил признаки, которые обычно повышают активность, и предложил новые комбинации мутаций, предположительно работающие лучше. После нескольких раундов такого вычислительно‑экспериментального цикла учёные получили два оптимизированных варианта фермента, которые в сочетании с улучшенной ωRNA повысили активность редактирования более чем в 60 раз по сравнению с исходной системой.
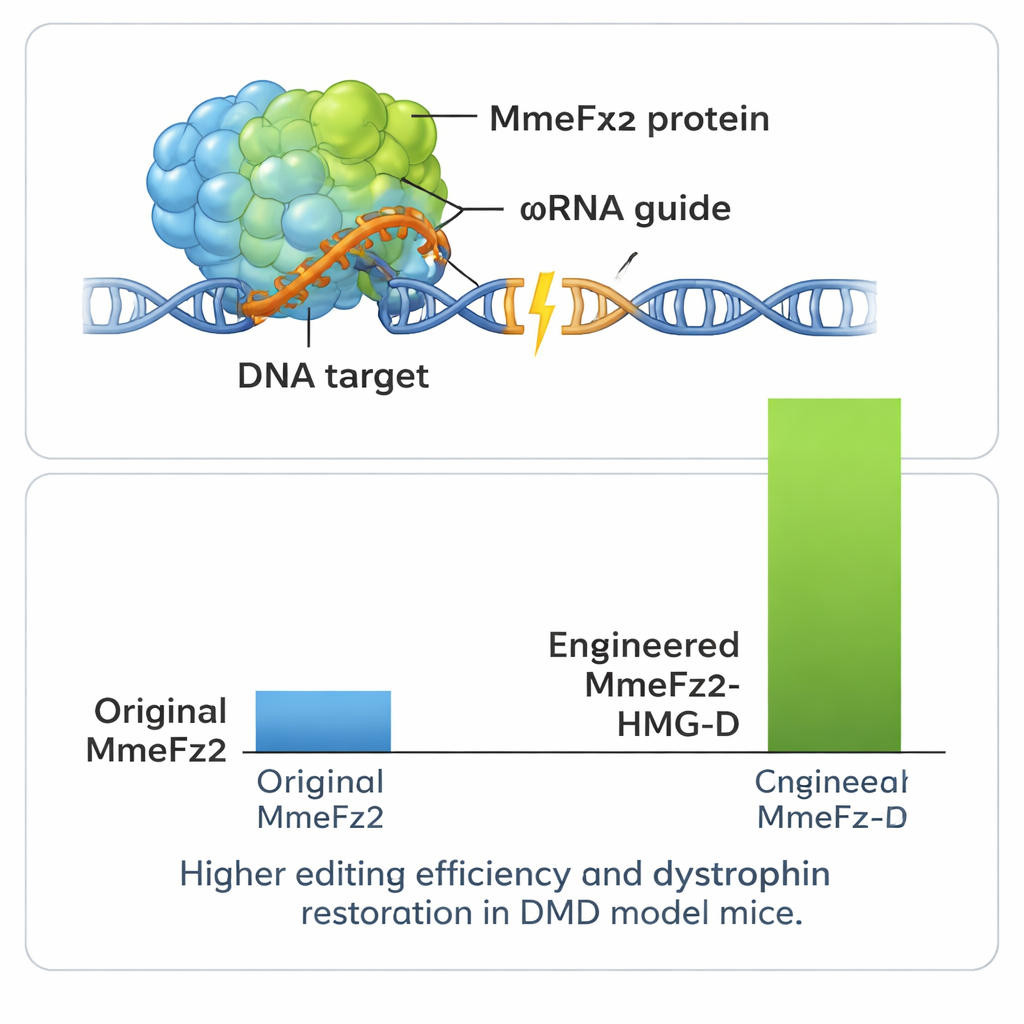
Усиление мощности и тестирование в модели болезни
Чтобы выжать из системы ещё больше, авторы слили MmeFz2 с небольшими ДНК‑связывающими доменами, помогающими белку крепче захватывать генетический материал. Один из них, называемый HMG‑D, оказался особенно эффективным при прикреплении к концу инженерного фермента, обеспечив уровни редактирования выше 80% в некоторых участках. Важно, что тесты предполагаемых офф‑таргетных локусов в геноме показали, что это увеличение мощности не сопровождалось существенной потерей точности. Поскольку весь редактор — и белок, и направляющая РНК — столь компактен, он комфортно помещается в единый вектор AAV, чего невозможно добиться для большинства систем CRISPR. Команда использовала это преимущество в мышиной модели мышечной дистрофии Дюшенна — смертельного заболевания с истощением мышц, вызванного ошибками в гене дистрофина. Одноразовая инъекция AAV‑доставленного редактора в мышцу ноги привела к обнаруживаемым поправкам в РНК гена и восстановлению белка дистрофина в значительной доле мышечных волокон.
Что это значит для будущих генетических терапий
Для неспециалистов главное послание таково: авторы превратили слабый, малоизвестный фермент для разрезания генов в компактный, высокопроизводительный редактор, который можно доставить в одной вирусной упаковке и который способен исправлять серьёзное генетическое заболевание в реалистичной животной модели. Не менее важно и то, как они этого добились: за счёт плотной интеграции предсказаний структуры на основе ИИ и машинного обучения с целенаправленными лабораторными тестами они улучшили и белок, и его направляющую РНК гораздо более эффективно, чем при традиционном методе проб и ошибок. Эта интегрированная стратегия может ускорить создание многих редакторов следующего поколения, приближая точные и более безопасные генетические терапии для пациентов с мышечной дистрофией и другими наследственными заболеваниями.
Цитирование: Li, S., Xu, K., Li, G. et al. Engineering the MmeFz2-ωRNA system for efficient genome editing through an integrated computational-experimental framework. Nat Commun 17, 1867 (2026). https://doi.org/10.1038/s41467-026-68644-5
Ключевые слова: редактирование генов, альтернативы CRISPR, болезнь Дюшенна (мышечная дистрофия), вирусная генотерапия, искусственный интеллект в биологии