Clear Sky Science · ru
Многостраатный геномный анализ подчеркивает региональное распространение холеры в Африке
Почему важно отслеживать микробы через границы
Холера по-прежнему вызывает заболевания и уносит десятки тысяч жизней в Африке ежегодно, однако фундаментальные вопросы остаются: как начинаются вспышки, как они распространяются между странами и почему они возвращаются снова и снова. Это исследование объединяет ученых и команды общественного здравоохранения из семи африканских стран для отслеживания бактерии, вызывающей холеру, по её генетическому коду. Сравнивая сотни бактериальных геномов, исследователи показали, как недавние волны холеры перетекают через границы, какие штаммы циркулируют в каких регионах и как эти знания могут сделать усилия по предотвращению будущих эпидемий более точными.
Взгляд на холеру с континентальной перспективы
Чтобы выйти за рамки разрозненных отчетов о случаях, Африканские центры по контролю и профилактике заболеваний инициировали сотрудничество под названием Консорциум по геномике холеры в Африке (CholGEN). Лаборатории в Камеруне, Демократической Республике Конго, Малави, Мозамбике, Нигерии, Уганде и Замбии секвенировали 763 высококачественных генома бактерии Vibrio cholerae O1, в основном за период с 2019 по 2024 год. Это крупнейший набор геномов холеры, когда-либо полученный внутри самой Африки. Разместив эти новые геномы рядом с почти 1800 ранее секвенированными образцами из Африки и Азии, команда смогла восстановить, как недавние африканские вспышки вписываются в длительную глобальную пандемию холеры.
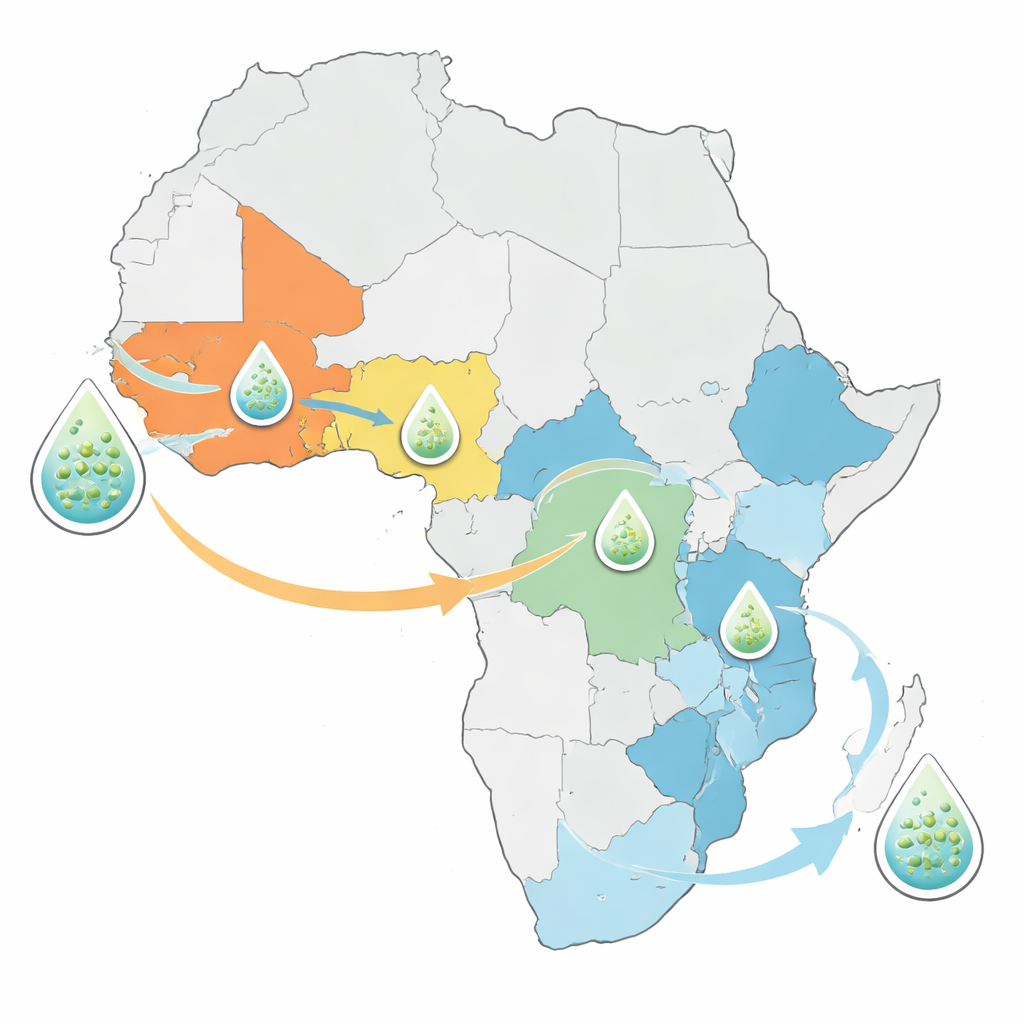
Старые штаммы, новые маршруты
Анализ показал, что штаммы холеры, вызывающие современные африканские вспышки, не представляют собой полностью новую угрозу. Все недавно секвенированные бактерии происходят от ранее известных интродукций линии седьмой пандемии, которая впервые проникла в Африку из Азии в 1970 году. Западно- и Центральноафриканские страны, такие как Нигерия, Камерун и Демократическая Республика Конго, как правило, доминируются одной или двумя долго существующими линиями, сохраняющимися десятилетиями. В странах Восточной и Южной Африки, напротив, одновременно циркулирует смесь нескольких линий. Одна линия в частности, названная AFR15, в последние годы быстро распространяется и связана с необычно крупными вспышками в Малави, Замбии и соседних странах, а также с эпидемиями в некоторых частях Ближнего Востока и Южной Азии.
Размер вспышек — не всегда дело генов
Можно было бы предположить, что взрывное распространение AFR15 связано с крупными генетическими изменениями, делающими её более опасной или способной лучше избегать лечения. Однако при сравнении темпов и паттернов мутаций в нескольких активных линиях исследователи не обнаружили существенных различий. Бактерии эволюционировали с похожей скоростью, а типы мутаций и затронутые гены выглядели в целом одинаково в разных линиях. Общие профили генов устойчивости к антибиотикам также оставались преимущественно стабильными во времени и между странами. Основное исключение — Уганда, где бактерии приобрели крупный мобильный фрагмент ДНК, плазмиду, несущую несколько генов резистентности, вероятно импортированную вместе со штаммами, связанными со вспышками в Йемене и Ливане. Даже в этом случае исследование не выявило новых генов, которые сами по себе объясняли бы тяжесть недавних африканских вспышек.
Скрытые пути, выявленные благодаря лучшей выборке
Поскольку бактериальные геномы несут запись о том, где были обнаружены близкородственные штаммы, команда смогла оценить, как часто холера пересекает границы. Они обнаружили множество примеров международного распространения между соседними странами, включая повторяющиеся обмены между Замбией и Демократической Республикой Конго. Однако при более тщательном рассмотрении статистические сигналы трансграничных скачков были наиболее заметны в годах и местах с интенсивной выборкой. Это указывает на то, что реальные перемещения холеры происходят чаще, чем показывают текущие данные; многие события передачи, вероятно, остаются незамеченными просто потому, что в тех местах или в то время никто не секвенировал бактерий. Чтобы справиться с этим, авторы разработали методику оценки того, сколько новой информации страна получает от секвенирования дополнительных образцов, учитывая генетическое разнообразие, число интродукций и уже имеющиеся данные.
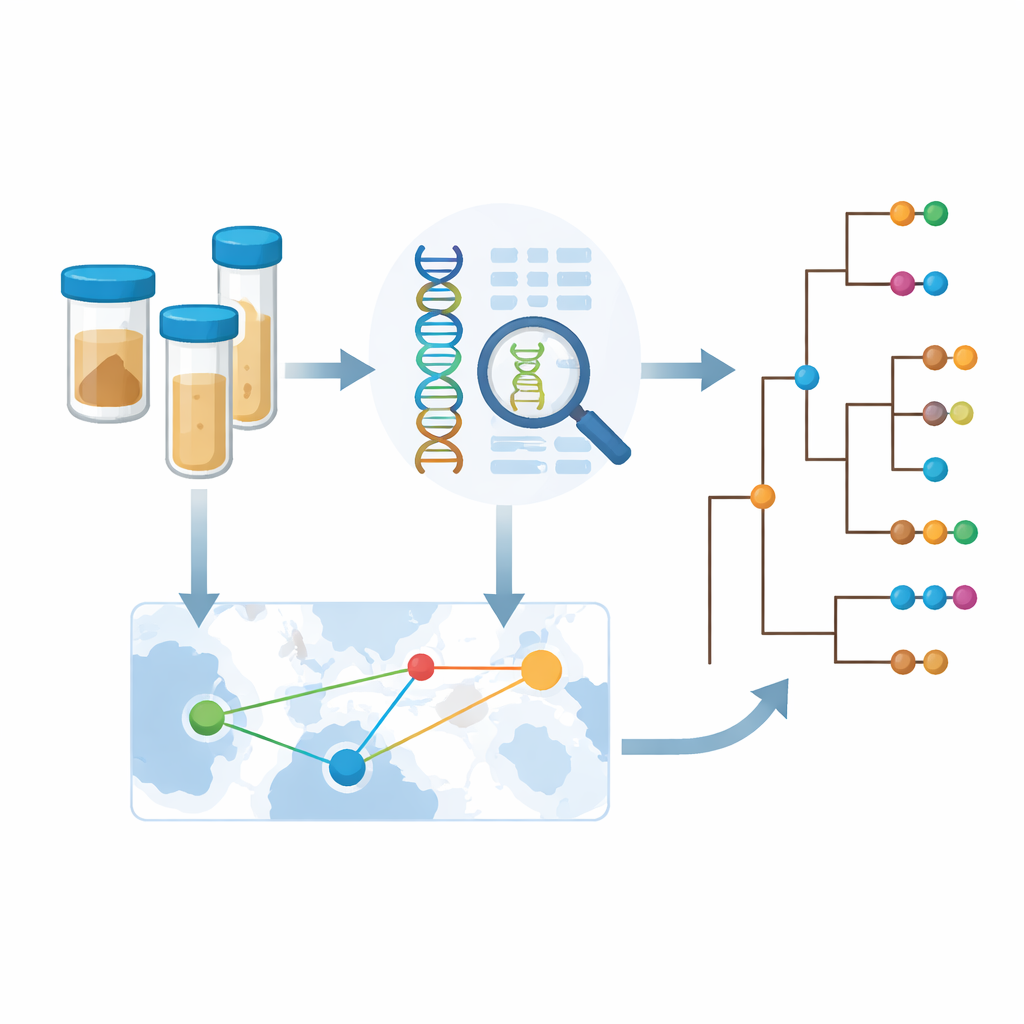
Использование геномики для более умных мер контроля
В исследовании делается вывод, что для холеры в современной Африке важнее то, как и где болезнь распространяется, чем какие-либо драматические изменения в самой бактерии. Полученные данные свидетельствуют в пользу рутинного, регионально скоординированного геномного надзора, чтобы соседние страны могли раньше замечать общие вспышки, отслеживать их источники и эффективнее нацеливать вмешательства, такие как вакцинационные кампании, улучшение водоснабжения и санитарии и реагирование в приграничных районах. Создавая возможности секвенирования внутри африканских лабораторий общественного здравоохранения и делясь данными через границы, инициативы вроде CholGEN дают практический план использования современной генетики для продвижения к амбициозной цели — устранить холеру как угрозу общественному здоровью к 2030 году.
Цитирование: Mboowa, G., Matteson, N.L., Tanui, C.K. et al. Multicountry genomic analysis underscores regional cholera spread in Africa. Nat Commun 17, 2539 (2026). https://doi.org/10.1038/s41467-026-68642-7
Ключевые слова: холера, геномный надзор, Африка, трансграничная передача, антибиотикорезистентность