Clear Sky Science · ru
Оценка стабильности сворачивания белков с явным учётом развёрнутых состояний
Почему стабильность белков важна
Каждый белок в вашем организме — это крошечный молекулярный механизм, который должен свернуться в точную трёхмерную форму, чтобы правильно выполнять свою функцию. Если эта складка слишком хрупка, белок может работать неправильно, слипаться или вовсе не синтезироваться — проблемы, связанные с заболеваниями и с неудачами при создании лекарств и ферментов на основе белков. Измерять стабильность белка в лаборатории медленно и сложно, поэтому учёные ищут компьютерные методы, которые могли бы надёжно сказать по одной лишь последовательности, насколько легко белок будет разворачиваться.
Новый взгляд на свернутые и развёрнутые белки
Большинство современных алгоритмов сосредоточено почти исключительно на свернутой форме белка. Они часто начинают с предсказанной ИИ структуры, например из AlphaFold, и рассматривают эту единственную структуру как главный фактор стабильности. Но на самом деле стабильность — это энергетический зазор между двумя широкими ансамблями: компактным свернутым состоянием и множеством гибких форм, составляющих развёрнутое состояние. Авторы утверждают, что игнорирование развёрнутой стороны этого равновесия — ключевая причина, по которой существующие инструменты не могут точно соответствовать экспериментальным измерениям свободной энергии сворачивания, известной как ΔG.
Новая модель, обучающаяся обоим состояниям
Исследователи представляют IFUM, систему глубокого обучения, разработанную для оценки ΔG, одновременно изучающую баланс свернутых и развёрнутых состояний для каждого белка. Вместо того чтобы считать развёрнутое состояние смутным фоном, IFUM использует идеи из физики полимеров и представляет его как «случайную катушку», кодируя и свернутое, и развёрнутое состояния в виде карт расстояний между парами аминокислот. Модель принимает данные от мощных предварительно обученных сетей для последовательностей и структур, а затем совместно предсказывает общую стабильность и карту вероятностей, описывающую, какая часть популяции белка является свернутой или развёрнутой для каждой пары остатков. Обучение на очень большой базе небольших экспериментально охарактеризованных белков и известных разупорядоченных белков помогает IFUM распознавать как хорошо структурированные, так и гибкие последовательности.
Лучшие показатели и более широкий охват мутаций
При тестировании на тщательно контролируемом наборе небольших белков IFUM предсказывает экспериментальные значения ΔG с меньшей ошибкой и более высокой корреляцией, чем предыдущие методы на базе ИИ, опирающиеся только на свернутую структуру или на языковые модели, обученные на последовательностях. Важным преимуществом является то, что модель также справляется с широким спектром изменений последовательности. Она точно отражает эффекты одно- и двухточечных мутаций, а также вставок и делеций, меняющих длину белка — ситуаций, в которых многие существующие инструменты либо полностью отказывают, либо изначально не были рассчитаны на такую задачу. Внутреннее сопоставление показывает, что исключение цели, связанной с развёрнутым состоянием, заметно ухудшает результаты, что подчёркивает: явное моделирование ансамбля развёрнутых состояний — это не просто концептуальная деталь, а центральный элемент точности предсказаний.
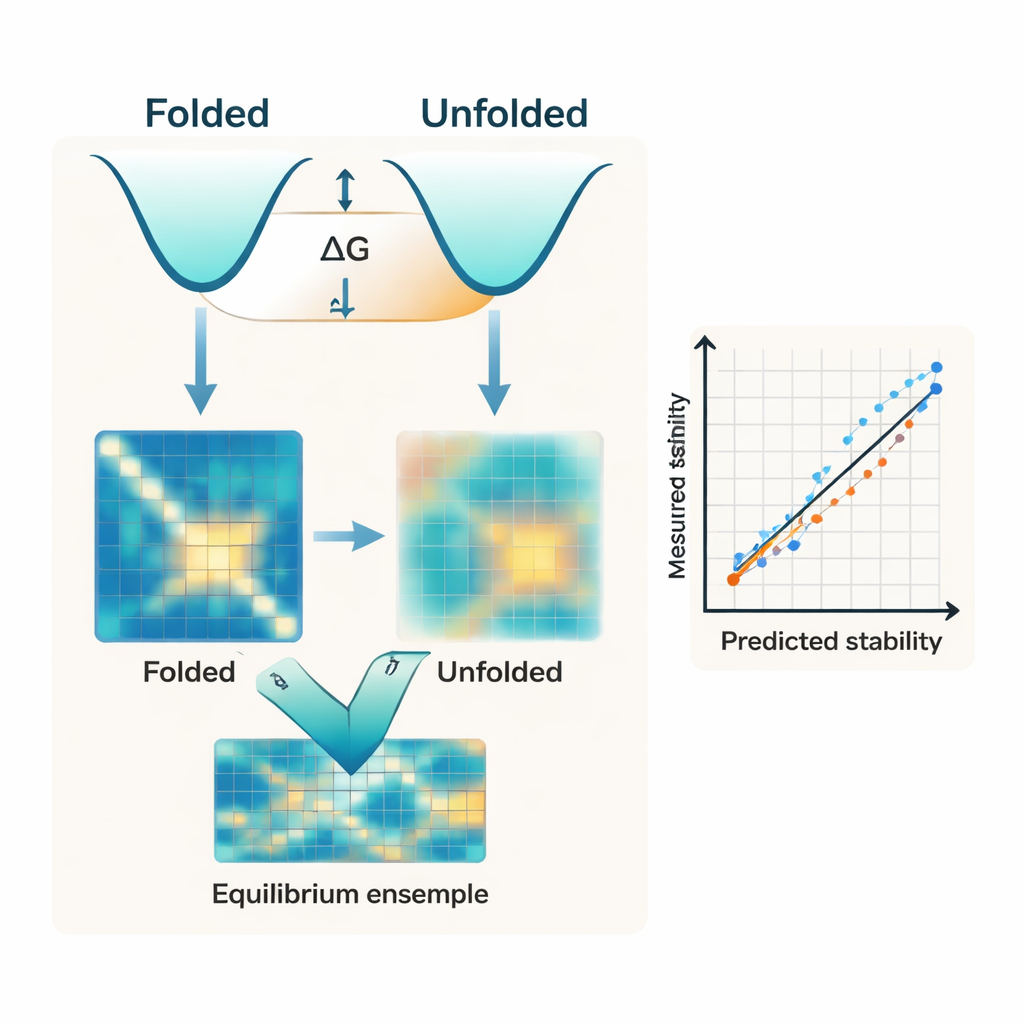
От лабораторного дизайна к реальным испытаниям
Чтобы проверить, может ли IFUM помочь в реальной инженерии белков, авторы применили его к трем сложным задачам дизайна: стабилизации интерферона‑лямбда, перестройке иммунного сигнального белка IL‑10 и улучшению фермента по модификации сахаров UGT76G1. Во всех трёх случаях предсказанная IFUM стабильность хорошо коррелировала с измеренными температурами плавления, которые показывают, сколько тепла белок выдерживает до разворачивания. Модель также помогла отсеять сотни совершенно новых, созданных компьютером белков, выбирая те, которые с наибольшей вероятностью свернутся и останутся растворимыми в клетках, превосходя широко используемые показатели уверенности от сетей предсказания структуры. Эти результаты указывают на то, что IFUM может использоваться как практический «фильтр стабильности» наряду с проверками на основе структуры в современных рабочих процессах по дизайну белков.
Ограничения и направления развития
Как и любая модель, IFUM имеет границы применимости. Она обучена главным образом на коротких, одноцепочечных, растворимых белках, и её абсолютные численные оценки стабильности становятся менее надёжными для значительно более крупных белков или белков с обширными гибкими петлями или мембранными участками. Описание развёрнутого состояния по‑прежнему представляет собой упрощённую статистическую модель, а не полностью реалистичную картину всех возможных форм. Тем не менее подход демонстрирует, что обучение ИИ учитывать оба ансамбля — свернутый и развёрнутый — даёт более надёжные оценки стабильности. Для неспециалистов главный вывод таков: IFUM приближает нас к возможности с количественной уверенностью спросить у компьютера «Удержится ли этот дизайн белка?», что потенциально ускорит разработку более безопасных биологических лекарств и более устойчивых промышленных ферментов.
Цитирование: Lee, H., Cho, Y., Yun, J. et al. Protein folding stability estimation with explicit consideration of unfolded states. Nat Commun 17, 1883 (2026). https://doi.org/10.1038/s41467-026-68637-4
Ключевые слова: стабильность белка, сворачивание белков, глубокое обучение, дизайн белков, мутации