Clear Sky Science · ru
Замаскированные нанороботы нацеливаются на макрофаги и регулируют шаблоны субклеточного взаимодействия органелл для стимуляции регенерации нервов
Почему важны крошечные «маскирующиеся» помощники при травмах спинного мозга
Травма спинного мозга часто ведёт к пожизненному параличу, потому что повреждённую нервную ткань чрезвычайно трудно восстановить. Главная причина в том, что место повреждения превращается в враждебную зону, заполненную воспалением и клеточным стрессом, которые блокируют заживление. В этом исследовании описан новый тип замаскированного наноробота, который путешествует по кровотоку, минует защитные механизмы организма и перепрограммирует иммунные клетки в области повреждения, переводя их из режима атаки в режим восстановления и помогая нервам регенерировать у животных с повреждением спинного мозга.
Проблема: воспаление, которое не выключается
После травмы спинного мозга первая волна повреждений обусловлена самой механической травмой. Но вторая, более медленная волна вызвана воспалением, токсичными молекулами — реактивными формами кислорода — и массовой гибелью клеток. Иммунные клетки, известные как макрофаги, устремляются на участок, чтобы убрать обломки. Первоначально они принимают агрессивный статус «M1», который уничтожает патогены и повреждённые клетки, но также выделяет сильные провоспалительные сигналы. Для начала реального восстановления эти же клетки позже должны переключиться в успокаивающее состояние «M2», которое поддерживает восстановление ткани, рост сосудов и регенерацию нервов. К сожалению, интенсивный стресс в повреждённой ткани может застрягивать макрофаги в вредоносном состоянии M1, закрепляя цикл хронического воспаления и препятствуя функциональному восстановлению.
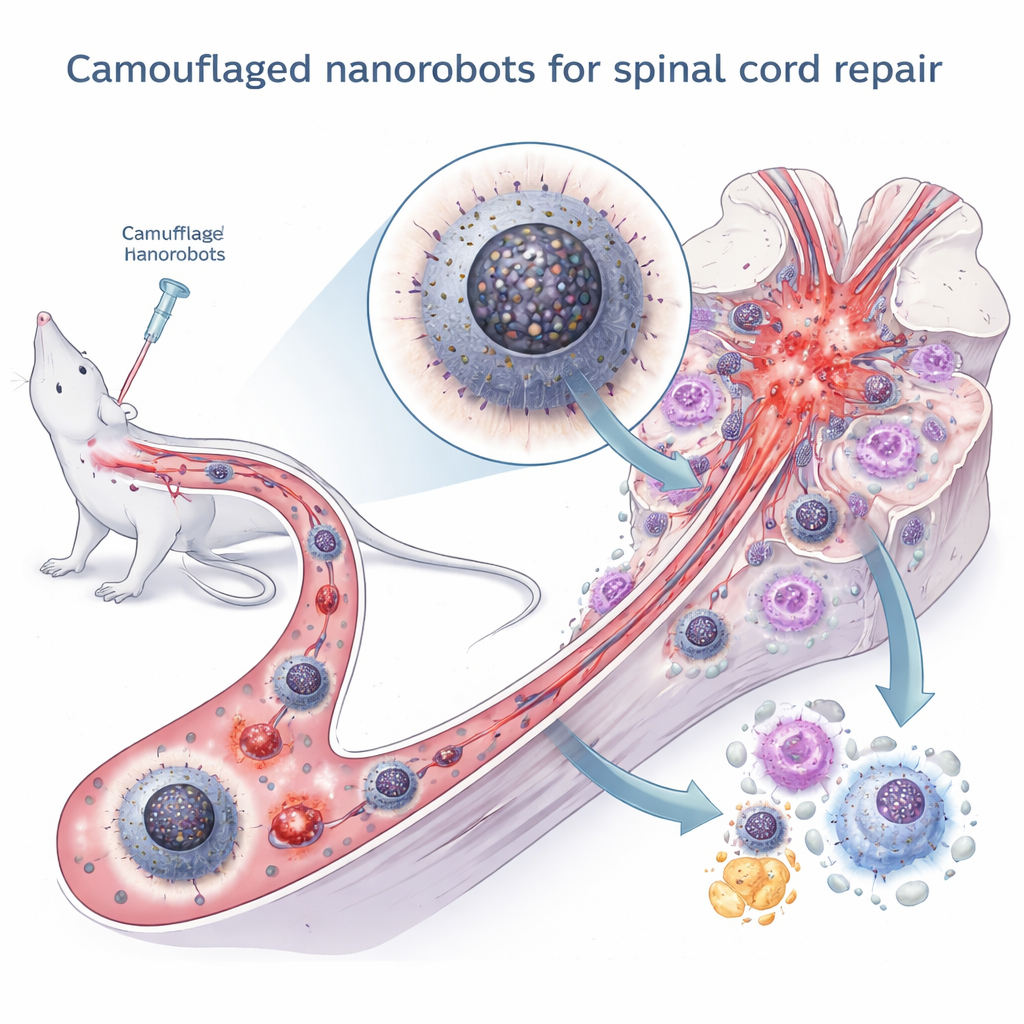
Скрытый разговор между частями клетки
Авторы сосредоточились на тонком, но ключевом внутреннем «диалоге» в макрофагах: взаимосвязи между двумя важными компартментами — эндоплазматическим ретикулумом (который помогает сворачивать белки и хранит кальций) и митохондриями (энергетические станции клетки). В норме эти структуры обмениваются малыми количествами ионов кальция через специализированные контакты, что помогает согласовывать выработку энергии с потребностями клетки. Однако после травмы избыток реактивных форм кислорода вызывает неправильное сворачивание белков и стресс в эндоплазматическом ретикулуме. Этот стресс, в свою очередь, приводит к чрезмерной передаче кальция в митохондрии, что вызывает энергетический крах, образование дополнительных токсичных молекул и утечку митохондриальной ДНК в цитоплазму. Попавшая туда ДНК активирует мощный сигнальный путь cGAS–STING–NFκB, который ещё больше закрепляет макрофаги в провоспалительном состоянии M1.
Проектирование замаскированного наноробота
Чтобы разорвать этот порочный круг, команда создала многослойный наноробот под названием BP@D/N. В его ядре — квантовые точки чёрного фосфора, крошечные частицы с сильными антиоксидантными и противовоспалительными свойствами, но с плохой стабильностью в организме. Эти частицы упакованы в полую оболочку из полидопамина — биосовместимого материала, который защищает их от преждевременного разрушения и сам по себе обладает антиоксидантной активностью. Наконец, вся частица покрыта мембраной, взятой из активированных нейтрофилов — типа белых кровяных клеток, которые естественно привлекаются в зоны воспаления. Эта «маскировка» позволяет нанороботу избегать клиренса иммунной системой, следовать сигналам воспаления к повреждённому участку спинного мозга и прикрепляться к макрофагам для эффективного поглощения.
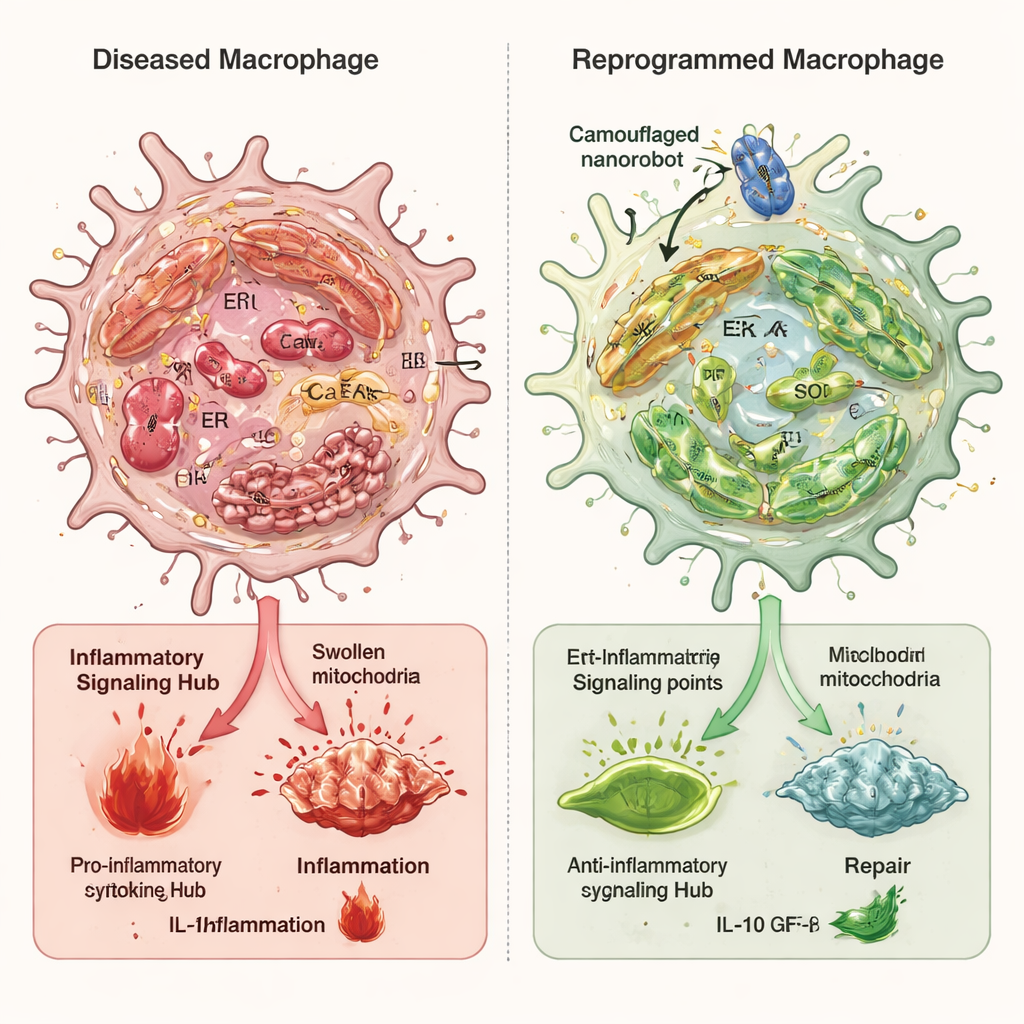
Перенастройка стрессовых иммунных клеток
В клеточных исследованиях макрофаги, подвергнутые воспалительным триггерам, демонстрировали высокий уровень стресса эндоплазматического ретикулума, распухшие и повреждённые митохондрии, кальциевую перегрузку и сильную активацию пути тревоги cGAS–STING–NFκB. При обработке замаскированными нанороботами общий оксидативный стресс резко снижался, внутренние мембраны между эндоплазматическим ретикулумом и митохондриями становились менее избыточно соединёнными, а митохондриальный кальций возвращался ближе к норме. Это предотвращало утечку митохондриальной ДНК в цитоплазму и ослабляло провоспалительную сигнальную каскаду. Ключевую роль в этом процессе сыграл фермент Ero1α, который участвует в регулировании окислительной среды и высвобождения кальция из эндоплазматического ретикулума. Нанороботы снижали активность Ero1α, и когда исследователи искусственно повышали Ero1α, это в значительной степени отменяло эффект наноробота, что подтверждает его центральную роль.
От успокоения воспаления к регенерации нервов
Эти внутренние изменения переворачивали макрофаги из разрушительного состояния M1 в восстанавливающее M2. В культурах клетки со сдвигом в сторону M2 секретировали меньше провоспалительных молекул, таких как TNF-α и IL-6, и больше факторов роста, которые стимулируют рост нейронов и поддерживающих клеток и способствуют удлинению аксонов. В модельных опытах на крысах с травмой спинного мозга повторные инъекции нанороботов приводили к уменьшению вредных иммунных сигналов в очаге поражения, меньшему образованию рубцовой ткани, меньшим полостям и большему числу регенерирующих нервных волокон. Животные, получавшие замаскированные нанороботы, восстановили лучшую работу задних конечностей, сильнее мышечные ответы и улучшенное строение мочевого пузыря по сравнению с нелеченными или получавшими менее целевые наночастицы.
Что это может значить для будущих пациентов
Это исследование показывает, что точная настройка внутриклеточного стресса и коммуникации между органеллами может перевести иммунные клетки из вредящей в помогающую роль для повреждённых нервов. Упаковывая мощные, но хрупкие антиоксидантные частицы в замаскированный, целевой наноробот, исследователи восстановили более здоровый баланс между воспалением и восстановлением в повреждённом спинном мозге крыс. Хотя до испытаний на людях остаётся много работы, это даёт многообещающий план: вместо широкого подавления воспаления будущие терапии могут направленно модулировать внутренние механизмы макрофагов, чтобы создать более благоприятную среду для регенерации нервов после травмы спинного мозга.
Цитирование: Guo, Q., Wang, W., Jiang, X. et al. Camouflaged nanorobots target and regulate macrophage subcellular organelle crosstalk patterns to promote neural regeneration. Nat Commun 17, 1952 (2026). https://doi.org/10.1038/s41467-026-68636-5
Ключевые слова: травма спинного мозга, нанороботы, макрофаги, регенерация нервов, наномедицина