Clear Sky Science · ru
Метаболическая характеристика взаимодействий опухоль‑иммунитет с помощью множественной иммуннофлуоресценции выявляет пространственные механизмы ответа на иммунотерапию при немелкоклеточной карциноме легкого (НМРЛ)
Почему это исследование важно
Иммунотерапия изменила подход к лечению у некоторых пациентов с распространенным раком легкого, однако у большинства больных опухоль продолжает прогрессировать, несмотря на эти мощные препараты. В этом исследовании задается простой, но ключевой вопрос: можно ли, внимательно изучив сам опухолевый материал — где располагаются разные клетки и как они используют энергию — предсказать, кто действительно получит пользу от иммунотерапии? Преобразуя крошечные биоптаты в детализированные клеточные карты, авторы стремятся приблизить лечение рака легкого к по-настоящему персонализированному подходу.
Исследование легочных опухолей как карта города
Команда проанализировала ткани 55 пациентов с распространенной немелкоклеточной карциномой легкого (НМРЛ), которым проводили лечение ингибиторами контрольных точек иммунитета — важным классом препаратов иммунотерапии. До начала терапии их опухолевые образцы были окрашены панелью из 44 маркеров методом множественной иммуннофлуоресценции, что позволило одновременно выявить множество белков. Глубокая нейросеть затем определяла ключевые типы клеток — например, опухолевые клетки, Т‑лимфоциты, В‑клетки, макрофаги и фибробласты — и классифицировала их функциональное состояние (например, активированные, делящиеся или истощенные), а также их метаболический профиль, то есть как они продуцируют и используют энергию. Вместо простого подсчета клеток исследователи также картировали их взаимное расположение, создавая в каждом биоптате регионы, напоминающие «соседства».
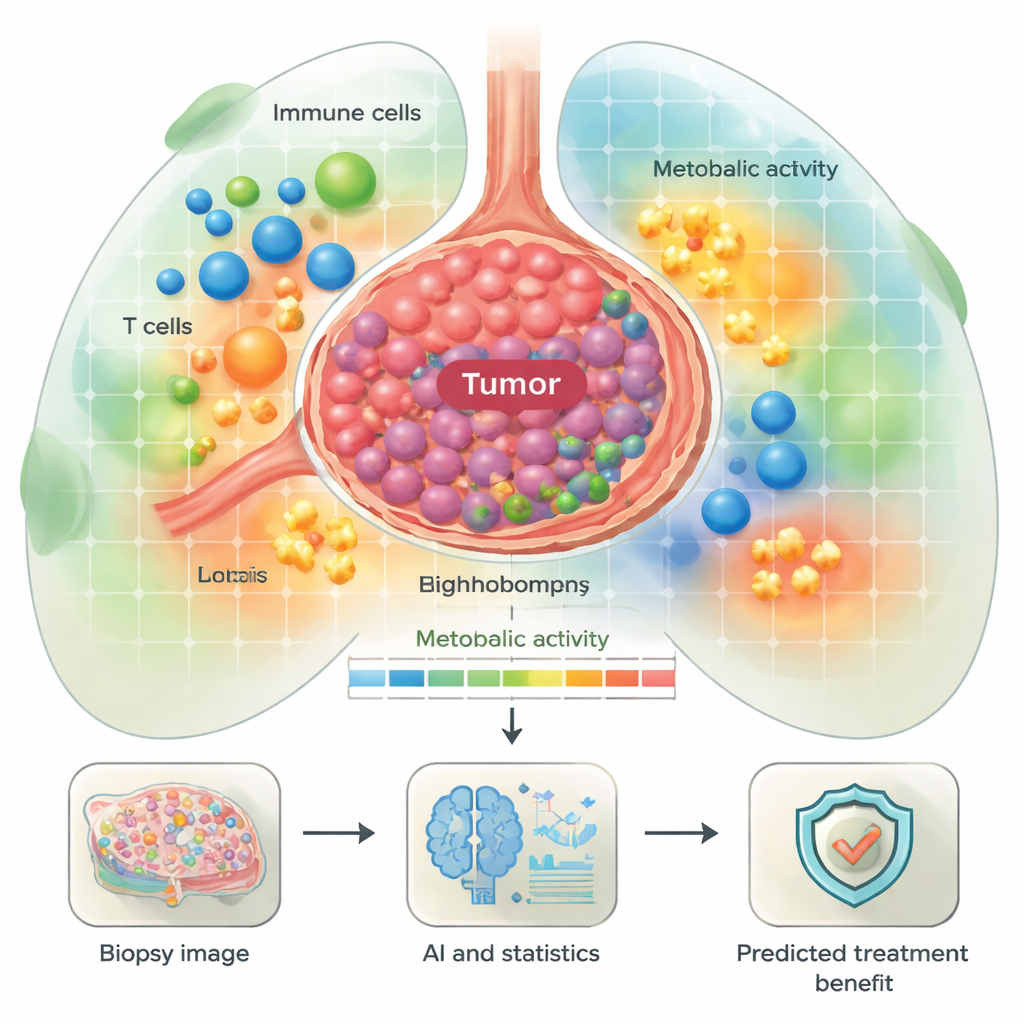
Энергетически активные опухоли и их иммунное окружение
Одним из основных фокусов был метаболизм — способы, которыми клетки генерируют топливо для роста или борьбы с болезнью. Авторы выделили «метаболические соседства» с разным уровнем и типом использования энергии: от зон с низкой активностью до крайне активных областей, богатых окислительным фосфорилированием и гликолизом. Выяснилось, что как опухолевые клетки, так и некоторые иммунные клетки, например макрофаги, зачастую демонстрируют сильные энергетические пути. Некоторые из этих паттернов коррелировали с исходом у пациентов. Так, опухоли с высокой активностью путей, связанных с использованием аминокислот и циклом трикарбоновых кислот, чаще встречались у пациентов, у которых наступил ранний рецидив после иммунотерапии. Напротив, некоторые плазматические клетки (В‑клетки, продуцирующие антитела) с активными энергетическими путями внутри опухоли чаще встречались у пациентов с лучшими результатами, что указывает: не все энергичные клетки вредны — некоторые могут поддерживать эффективный противоопухолевый иммунитет.
«Хорошие» и «плохие» иммунные игроки в ландшафте опухоли
Важна была не только общая численность, но и тип и поведение иммунных клеток. Макрофаги, несущие цитотоксический молекулярный маркер гранзим B, были тесно связаны с худшей безрецидивной выживаемостью, особенно когда они локализовались в метаболически слабых или неактивных соседствах. Такие области могут представлять собой бедные питательными веществами или находящиеся в состоянии покоя участки, где иммунная атака ослаблена. Напротив, определенные конфигурации регуляторных Т‑клеток (Tregs) и фибробластов на границе между опухолью и окружающей тканью ассоциировались с лучшими исходами, возможно, отражая ситуацию, когда иммунноподавляющие клетки удерживаются на периферии и не проникают глубоко в опухоль. Соотношения между разными иммунными популяциями, например гранулоцитов и CD8‑Т клеток, также коррелировали с ответом, подчеркивая, что имеет значение иммунный баланс и позиционирование, а не только абсолютные количества.
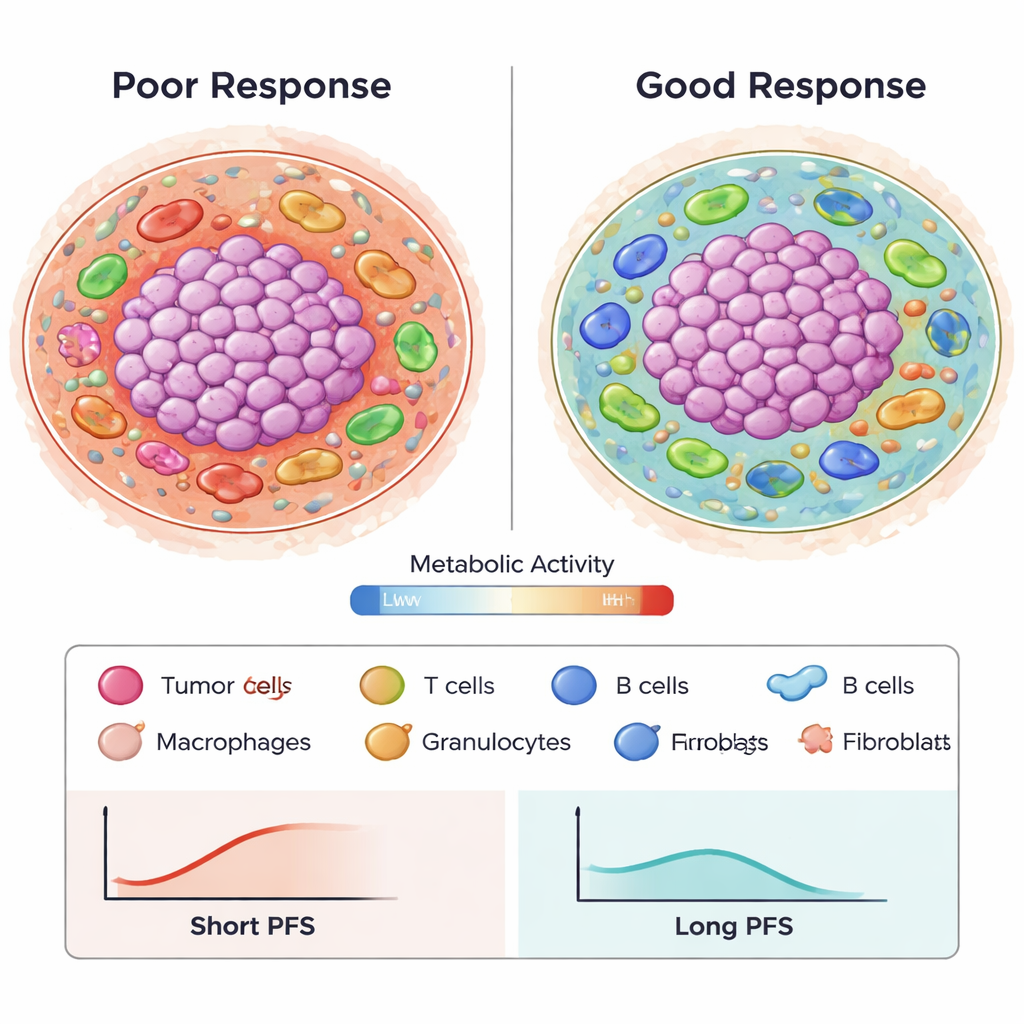
От сложных изображений к предсказуемым паттернам
Чтобы осмыслить более миллиона пространственных признаков, описывающих типы клеток, расстояния и метаболические состояния, авторы применили продвинутый метод отбора признаков (Stabl) и инструменты моделирования выживаемости. Они выделили 87 ключевых признаков, многие из которых отражали, как метаболически активные опухолевые клетки взаимодействуют с макрофагами и Т‑клетками, или как специфические типы иммунных клеток группируются рядом с кровеносными сосудами и фибробластами. Используя эти признаки в моделях регрессии Кокса, исследователи построили предиктор, который оценивал безрецидивную выживаемость с точностью (AUC) около 0,8 за 24 месяца, превосходя традиционные одиночные маркеры, такие как окраска PD‑L1 или нагрузка мутаций опухоли, в ранее опубликованных работах. Важно, что несколько признаков воспроизводились в двух независимых когортных наборах пациентов, что указывает на то, что выявленные паттерны — не просто случайный шум.
Что это означает для пациентов
Для неспециалиста основная мысль такова: где клетки располагаются в опухоли легкого и как они подпитывают свою активность может помочь объяснить, почему одни пациенты хорошо отвечают на иммунотерапию, а другие — нет. Исследование демонстрирует, что богатая пространственная и метаболическая информация из рутинной биопсии в сочетании с искусственным интеллектом и статистическим моделированием может выявлять сигнатуры вероятной пользы или резистентности. Хотя необходимы дальнейшие валидации на больших выборках и в цельных срезах ткани, работа прокладывает путь к будущим тестам, которые могли бы заранее, до начала лечения, указывать врачам, у каких пациентов есть высокий шанс длительного контроля при иммунотерапии, а кому потребуются альтернативные или комбинированные стратегии.
Цитирование: Monkman, J., Kilgallon, A., Lawler, C. et al. Metabolic characterization of tumor-immune interactions by multiplexed immunofluorescence reveals spatial mechanisms of immunotherapy response in non-small cell lung carcinoma (NSCLC). Nat Commun 17, 837 (2026). https://doi.org/10.1038/s41467-026-68633-8
Ключевые слова: устойчивость к иммунотерапии, немелкоклеточный рак легкого, опухолевая микросреда, пространственная биология, метаболизм рака