Clear Sky Science · ru
Гидрогель с сигналами клеточно-клеточного сцепления улучшает регенерацию нервной ткани
Помощь травмированному мозгу в самовосстановлении
Черепно-мозговые травмы могут надолго нарушать движения, память и мышление, потому что повреждённые нейроны в мозге редко заново отрастают или правильно восстанавливают связи. Врачи могут удалить кровяные сгустки или стабилизировать череп, но у них мало средств для восстановления тонкой проводящей сети мозга. В этом исследовании описан мягкий, богатый водой материал — гидрогель — сконструированный так, чтобы имитировать естественные механизмы сцепления клеток мозга. Воссоздавая эти крошечные «рукопожатия» между клетками, материал способствует отрастанию повреждённых нервных волокон, восстановлению связей и восстановлению функций в повреждённых мозгах крыс.
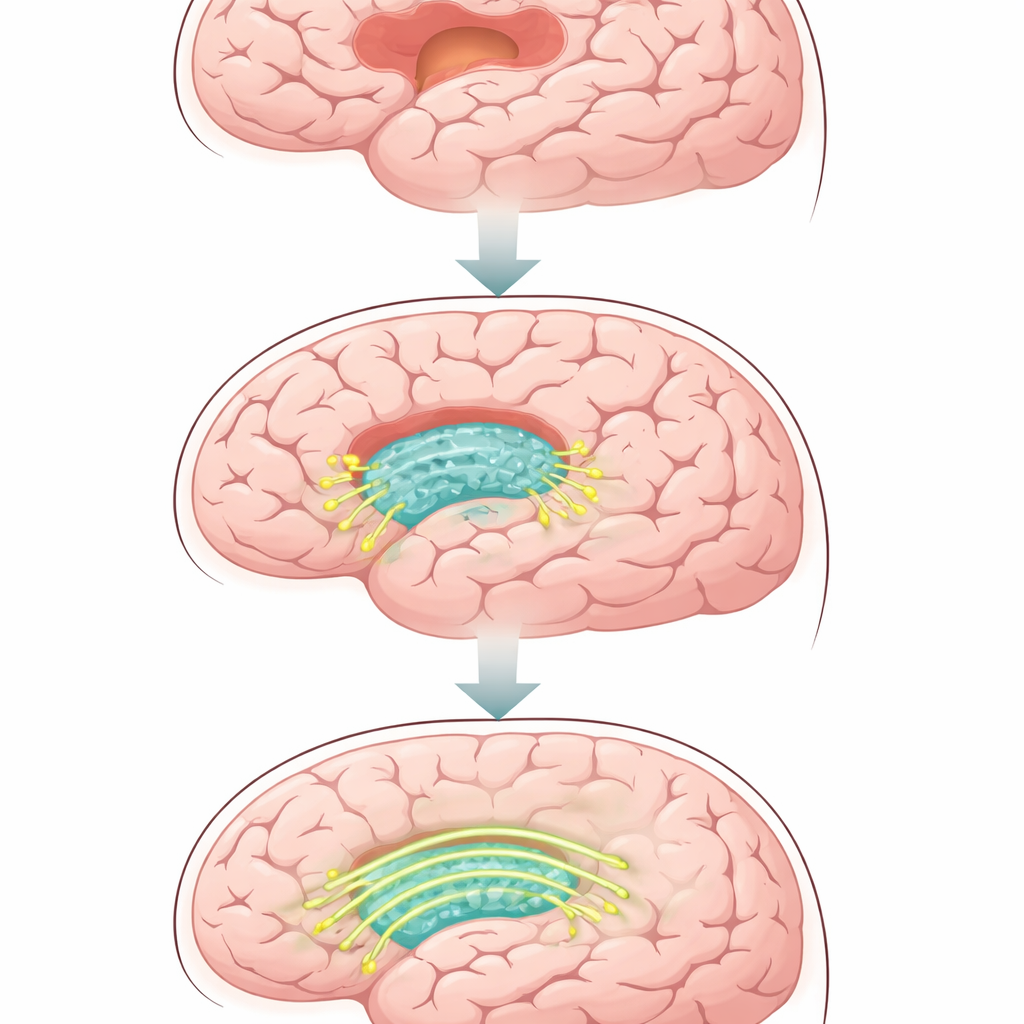
Мягкий каркас для повреждённой мозговой ткани
Исследователи начали с шелкового гидрогеля, по консистенции похожего на ткань мозга — очень мягкий и гибкий, с множеством маленьких пор, по которым клетки могут перемещаться и отращивать отростки. Затем они покрыли этот гель тонким подвижным слоем липидов, который ведёт себя как клеточная мембрана. Этот слой способен удерживать специальные белки, одновременно позволяя им смещаться по поверхности, так же как на настоящих клетках. В результате получился трёхмерный инъецируемый материал, способный заполнять неровные раневые полости мозга и представлять клеткам подвижные сигналы, а не выступать лишь в роли пассивного заполнителя.
Заимствование у природы клеточно-клеточного «рукопожатия»
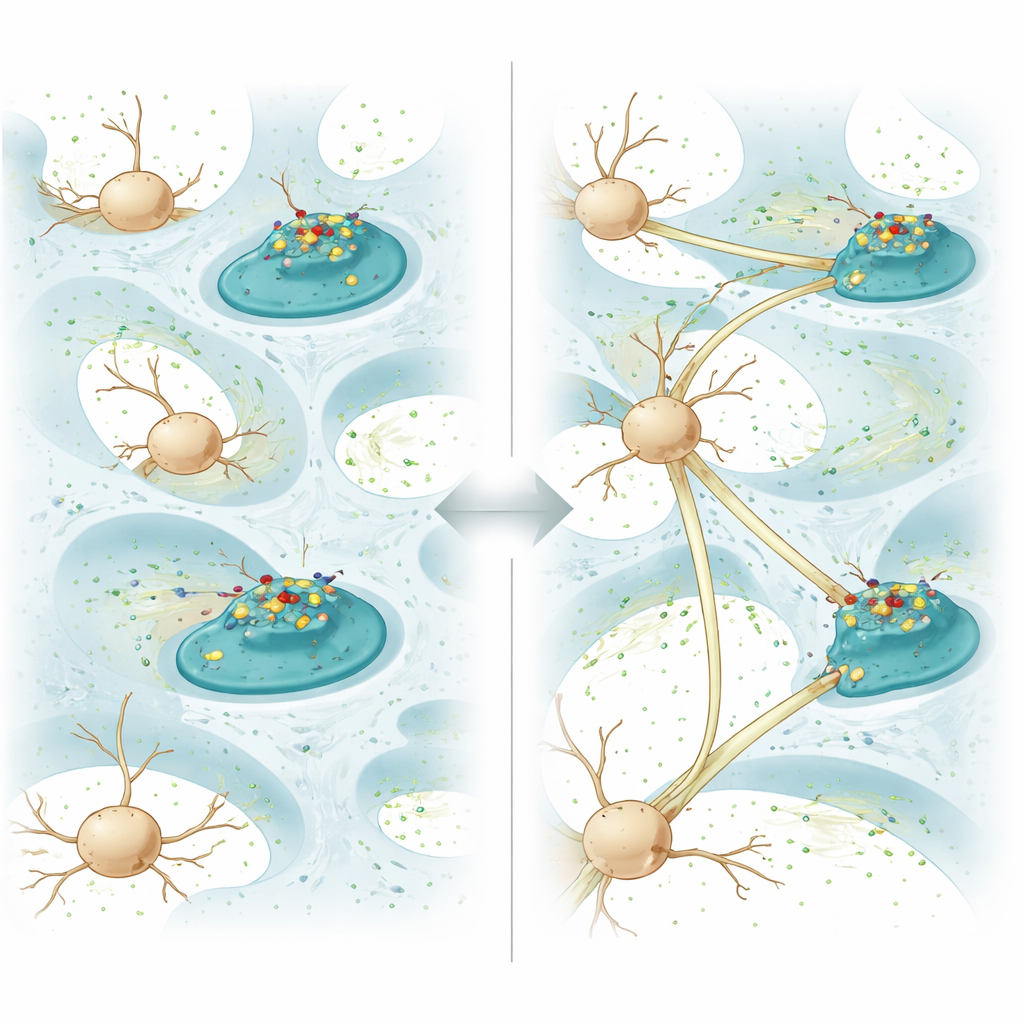
Чтобы превратить гидрогель в активного участника заживления, команда прикрепила к липидному покрытию белок N-cadherin. В мозге N-cadherin располагается на поверхности нейронов и помогает соседним клеткам узнавать и сцепляться друг с другом, формируя стабильные контакты и, в конечном счёте, синапсы, где сигналы переходят от клетки к клетке. В этом геле N-cadherin не зафиксирован жёстко; он может свободно диффундировать по покрытию. Когда нейроны растут у поверхности геля, белок скапливается в точках соприкосновения их мембран с материалом, перестраивая мелкие выросты клеток и запускаючи образование клеточно-клеточных контактов. В культурах нейроны, растущие на таком «диффузном N-cadherin» геле, отращивали более длинные волокна, формировали больше соединений и демонстрировали более сильную электрическую связь по сравнению с аналогичными гелями, где белок был жёстко прикреплён и неподвижен.
Активация программ восстановления в мозге
Помимо простого контакта, гидрогель также стимулирует нейроны включать внутренние пути восстановления. Анализы генов и белков показали, что клетки на диффузном N-cadherin геле снижали сигналы, ведущие к программируемой гибели, и усиливали пути, известные как поддерживающие рост и выживание. В частности, материал повышал уровень белка тромбоспондин‑1, который выделяют опорные клетки мозга и который может одновременно стимулировать формирование синапсов и активировать сигнальные маршруты, благоприятные для роста. Два из этих путей, часто называемые TGF-β/Smad и AKT/mTOR, были сильно активированы, что приводило к более здоровым митохондриям, повышенному производству энергии и усиленному отрастанию перерезанных нервных волокон в микрофлюидной модели, имитирующей разрезанные аксоны.
От чашки Петри до живого мозга
Чтобы проверить, имеют ли эти эффекты значение в живом организме, команда вводила гидрогель крысам с контролируемой формой черепно-мозговой травмы. В течение нескольких недель животные, получавшие диффузный N-cadherin гель, демонстрировали лучшие результаты в тестах на движение и в водном лабиринте, оценивающем обучение и память, по сравнению с животными, которым вводили обычный гель, гель только с липидами или физиологический раствор. Снимки мозга и срезы тканей показали меньшие полости в зоне поражения и больше недавно образовавшихся нервных волокон и синапсов в восстановленном участке. При этом в обработанных мозгах наблюдалось меньше чрезмерно активных иммунных клеток и менее плотная рубцовая ткань, что создавало более благоприятную среду для регенерации. Маркеры клеточной гибели были снижены, тогда как белки, связанные со здоровой коммуникацией между нейронами, увеличились.
Почему это важно для будущего восстановления мозга
Проще говоря, работа демонстрирует, что обеспечение повреждённой мозговой ткани правильными «социальными сигналами» может существенно повлиять на качество её восстановления. Вместо того чтобы лишь механически поддерживать клетки, гидрогель воссоздаёт подвижные контактные сигналы, которые настоящие клетки мозга используют, чтобы находить и удерживать друг друга. На крысах эта стратегия не только заполняла пустоты в мозге, но и помогала восстановить рабочие нейронные цепи и улучшить поведение после травмы. Хотя до применения таких материалов у людей предстоит ещё много испытаний, подход — внедрение свободно подвижных белков клеточного сцепления в мягкие инъецируемые гели — может быть расширен за пределы N-cadherin и мозга, предложив общую рецептуру материалов, которые активно направляют регенерацию тканей.
Цитирование: Tang, X., Zhang, S., Liu, M. et al. Hydrogel with cell-cell adhesion cues enhances neural regeneration. Nat Commun 17, 2178 (2026). https://doi.org/10.1038/s41467-026-68632-9
Ключевые слова: регенерация нервной ткани, черепно-мозговая травма, гидрогелевый каркас, клеточное сцепление, N-cadherin