Clear Sky Science · ru
H3K9me2, опосредованная G9a, координирует регенерацию кишечного эпителия через эпигенетическое подавление генов, связанных с клеточным циклом
Почему самовосстановление кишечника важно
Каждый день поверхность кишечника подвергается суровым воздействиям: желудочной кислоте, частицам пищи и триллионам микробов. Тем не менее эта ткань не только сохраняется, она постоянно восстанавливается. Когда система ремонта дает сбой — после лучевой терапии, при воспалительных заболеваниях кишечника или тяжелых инфекциях — люди испытывают боль, кровотечения и опасные для жизни осложнения. В этом исследовании раскрывается скрытый «переключатель» внутри кишечных клеток, который помогает им решить, когда прекратить покой и начать восстановление, что дает подсказки для новых методов лечения, способных усилить естественную ремонтную бригаду кишечника.
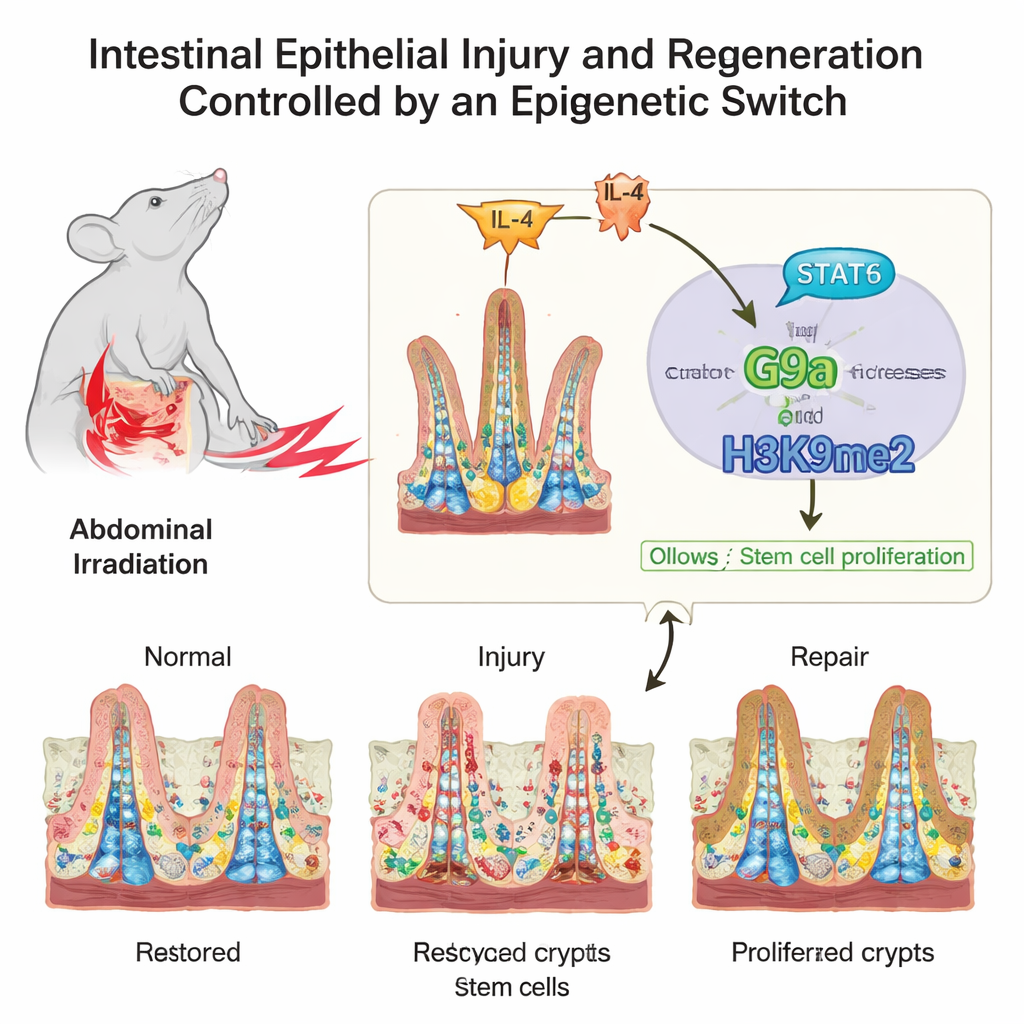
Хрупкая архитектура под постоянным давлением
Внутренняя поверхность кишечника под микроскопом напоминает ворсистый ковер: там есть пальцевидные ворсинки для всасывания питательных веществ и крипты — карманы, где живут стволовые клетки. Эти стволовые клетки и их быстро делящиеся дочерние клетки должны поддерживать баланс между нормальным обновлением и экстренным ремонтом. Авторы сосредоточились на том, как химические метки на белках, упаковывающих ДНК — гистонах — влияют на этот баланс. Эти метки не меняют сами гены, но действуют скорее как регуляторы яркости, усиливая или ослабляя группы генов по мере перехода кишечника от нормального состояния к повреждению и обратно к здоровью.
Эпигенетическая метка, отслеживающая повреждение и заживление
Используя мышей, подвергнутых облучению — частой причине повреждения кишечника при лечении рака — исследователи просеяли многочисленные метки гистонов в криптах, богатых стволовыми клетками. Одна метка, известная как H3K9me2, резко возрастала в момент перехода кишечника от повреждения к восстановлению. Ее пишущий фермент, белок G9a, демонстрировал тот же шаблон. Команда затем изучила образцы человека: у пациентов, получавших тазовую радиотерапию, и у людей с болезнью Крона. В обеих ситуациях более высокие уровни H3K9me2 и G9a в кишечных клетках ассоциировались с лучшими признаками восстановления ткани, что указывает на сохранность этой системы у мышей и человека.
Когда «переключатель» ремонта ломается
Чтобы проверить, является ли эта метка простым наблюдением или действительно управляет заживлением, ученые удалили G9a специфически в кишечной оболочке мышей или блокировали его активность с помощью препарата. В обоих случаях уровни H3K9me2 падали. После облучения или химического повреждения такие мыши теряли больше веса, имели более короткие и более поврежденные кишечники и проявляли меньше регенерирующих крипт и стволовых клеток по сравнению с нормальными животными. Даже без явного повреждения слизистая кишечника у мышей, лишенных G9a, выглядела угнетенной: крипты были мельче, ворсинки короче, а количество стволовых клеток и их специализированных потомков снижалось. Небольшие «мини‑кишечники», выращенные из этих клеток в культуре, также росли плохо, что подчеркивает центральную роль этой молекулярной системы в повседневном обновлении кишечника.
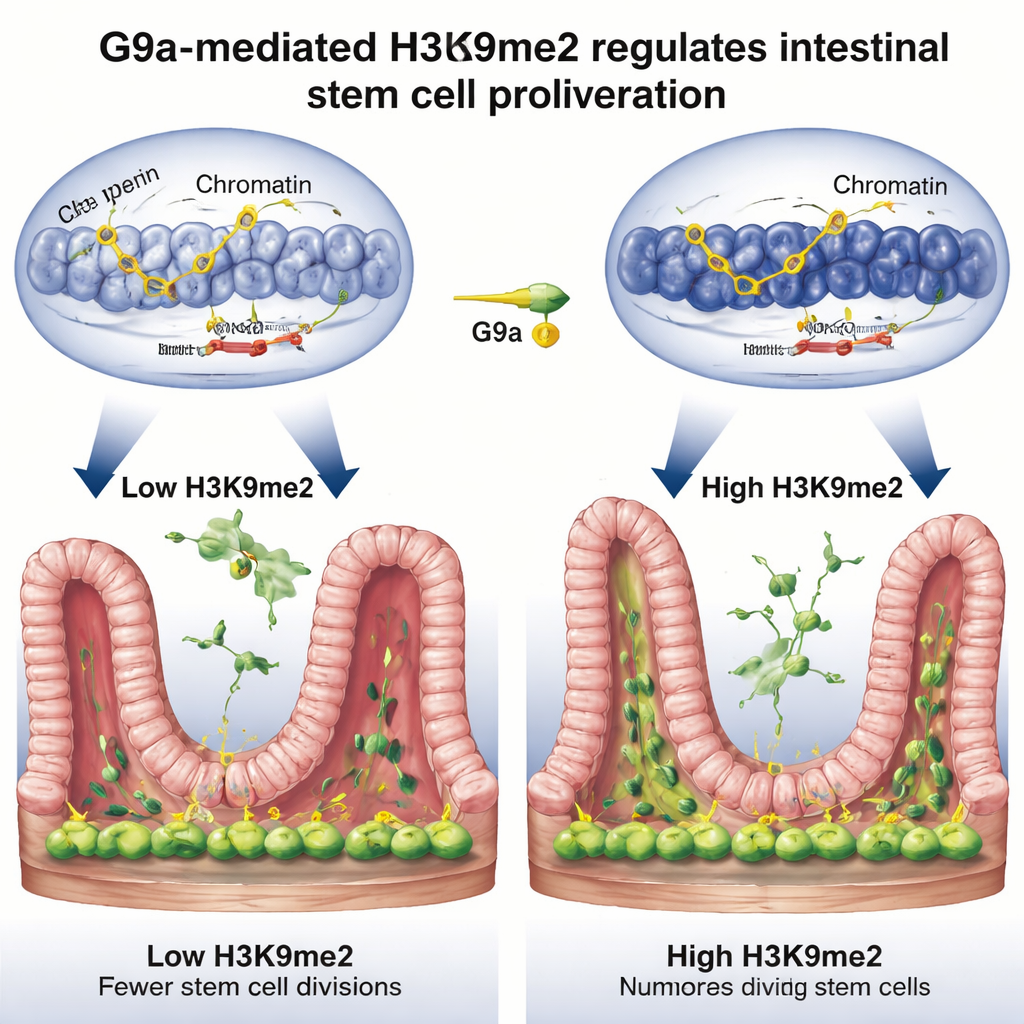
Освобождение тормозов клеточного деления
Углубившись далее, команда выясняла, какие гены контролирует этот «переключатель» ремонта. Объединив три мощных геномных метода, они обнаружили, что H3K9me2, устанавливаемая G9a, обычно располагается на участках ДНК, которые действуют как тормоза клеточного цикла — таких как Rb1cc1, Rb1, Cdkn1a и Pten, замедляющих или останавливающих деление клеток. При отсутствии G9a метка исчезала с этих регионов, окружающая ДНК открывалась, и эти тормозные гены включались сильнее, что вело к замедленной пролиферации стволовых клеток. Во время нормального восстановления после повреждения уровни H3K9me2 на этих генах повышались, их активность снижалась, и стволовые клетки могли свободнее делиться и восстанавливать слизистую. По сути, G9a и H3K9me2 временно приглушают сигналы «стоп», чтобы ткань могла отрастать заново.
Сигнальная цепочка от иммунных сигналов к ремонту
Кишечник не действует в одиночку; он постоянно слушает сигналы иммунной системы. Исследователи проследили один такой сигнал выше по цепочке от G9a. После повреждения повышались уровни иммунного медиатора IL‑4, что приводило к активации белка STAT6 внутри кишечных клеток. Активированный STAT6 непосредственно связывался с регуляторным участком гена G9a, усиливая его экспрессию. Получалась цепочка команд: IL‑4 активирует STAT6, STAT6 повышает уровень G9a, а G9a добавляет H3K9me2 для подавления генов‑тормозов клеточного цикла, позволяя стволовым клеткам расширяться и восстанавливать поврежденную оболочку.
Что это значит для будущих лечебных подходов
Для неспециалиста эти результаты показывают, что восстановление кишечника регулируется не только генами, но и обратимыми химическими метками, которые точно настраивают, когда эти гены используются. Путь IL‑4–STAT6–G9a–H3K9me2 действует как внутренняя панель управления, временно ослабляющая тормоза деления стволовых клеток настолько, чтобы обеспечить заживление, а затем может быть сброшен. В будущем терапевтические подходы, мягко усиливающие этот путь — например лекарства или генетические инструменты, повышающие уровень G9a в нужное время и в нужном месте — могут помочь пациентам быстрее восстанавливаться после лучевых повреждений, вспышек воспалительных заболеваний кишечника или других состояний, повреждающих кишечную оболочку, при минимизации риска неконтролируемого роста клеток.
Цитирование: Chen, J., Shi, X., Zhou, X. et al. G9a-mediated H3K9me2 orchestrates intestinal epithelial regeneration through epigenetic silencing of cell cycle-related genes. Nat Commun 17, 1874 (2026). https://doi.org/10.1038/s41467-026-68626-7
Ключевые слова: регенерация кишечника, эпигенетика, стволовые клетки, метилирование гистонов, воспалительное заболевание кишечника