Clear Sky Science · ru
Двойные синтазы сигналов кворума DspII и DspI координируют переключение вирулентности у Pseudomonas aeruginosa
Как больничный супермикроб меняет тактику атаки
Pseudomonas aeruginosa — печально известный возбудитель больничных инфекций, способный вызывать стойкие инфекции легких и ран, особенно у уязвимых пациентов. Он выживает, переключаясь между двумя образами жизни: защищенным, медленнорастущим сообществом, называемым биопленкой, и быстрым, агрессивным режимом, при котором бактерия активно проникает в ткани. В этом исследовании показано, как сам микроорганизм решает, когда выйти из долговременной биопленки и начать внезапную остро протекающую атаку, что выявляет потенциальные новые уязвимости для будущих терапий.
Жизнь микроба между укрытием и атакой
Многие бактериальные инфекции развиваются стадийно. На ранних этапах свободноплавающие клетки распространяются по организму и применяют мощные факторы, повреждающие ткани хозяина. Позже они часто оседают в биопленках — плотных, слизистых слоях на поверхностях, таких как катетеры, легочная ткань или раны. В таких сообществах клетки заключены в защитную матрицу, что делает их стойкими к антибиотикам и иммунным атакам. Однако биопленки — не тупик. Клетки могут покидать их, восстанавливать подвижность и инициировать новые вспышки острой инфекции в других местах. До сих пор было неясно, как Pseudomonas aeruginosa целенаправленно координирует переход от хронического персистирования к агрессивной болезни.
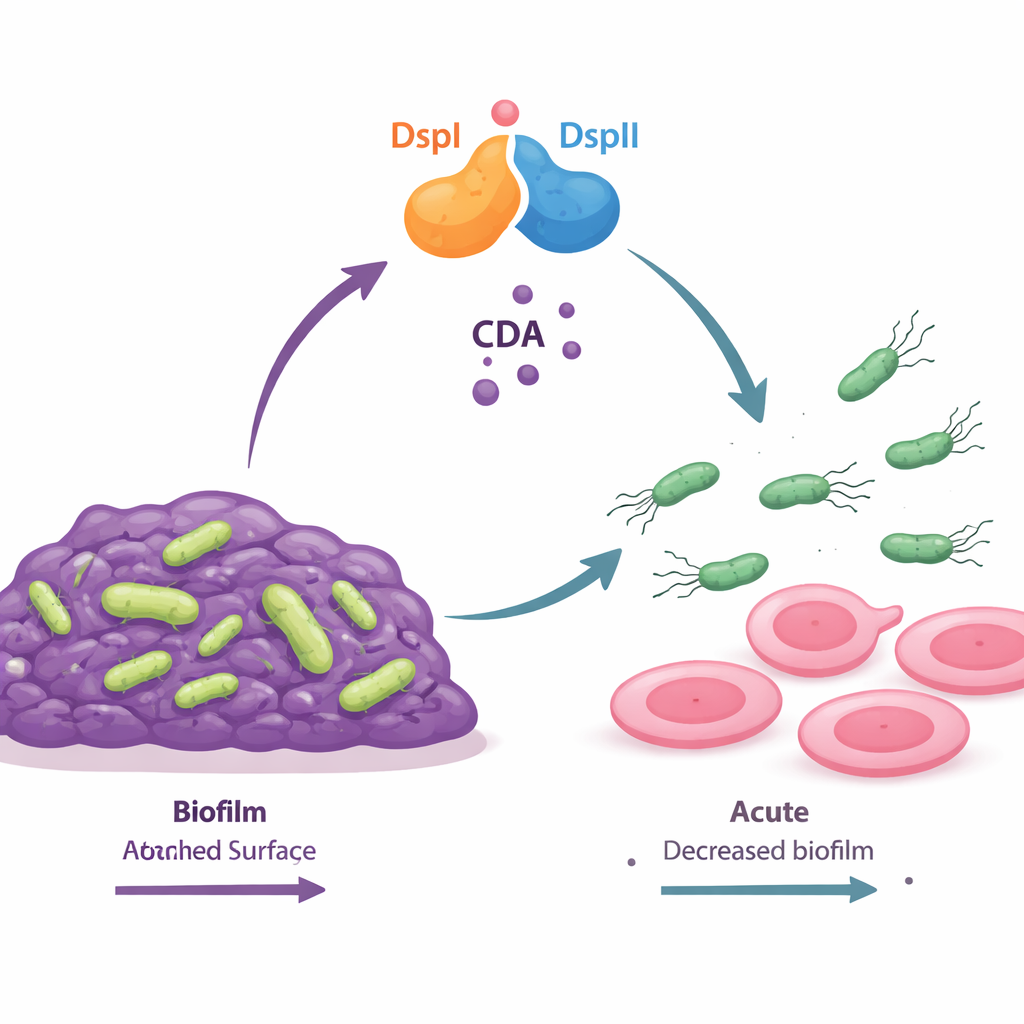
Двухбелковый выключатель, создающий химический «поехали» сигнал
Авторы обнаружили, что две бактериальные белковые молекулы, названные DspI и DspII, действуют вместе как некий молекулярный переключатель. Оба являются ферментами одного общего типа и расположены рядом в геноме бактерии, включаясь вместе по мере увеличения плотности популяции. Когда они образуют пару, они синтезируют небольшую жирную кислоту — cis-2-деценовую кислоту (CDA), относящуюся к более широкой группе молекул связи, известных как DSF-сигналы. Мутантные бактерии, лишенные либо DspI, либо DspII, не могли больше синтезировать CDA, формировали необычно плотные биопленки и теряли способность к роению по поверхностям. Только восстановление обоих белков вместе вернуло клеткам нормальное образование сигнала, распад биопленки и подвижность, что показывает, что эти два фермента функционируют как взаимозависимая команда.
От химического сигнала к движению и бегству
CDA не действует изолированно; он подключается к внутренней проводке бактерии. Авторы показали, что CDA снижает уровень другого сигнального молекулы — циклического ди-GMP — повышая активность специфического фермента RbdA, разрушающего этот мессенджер. Высокий уровень циклического ди-GMP обычно стимулирует построение биопленки, усиливая синтез сахарной матрицы и подавляя жгутики — крошечные пропеллеры, обеспечивающие плавание. При наличии CDA уровни циклического ди-GMP падают, регулятор FleQ меняет режим работы, синтез «липкой» сахарной матрицы снижается, а жгутики удлиняются и укрепляются. В результате биопленки ослабевают, и клетки вновь получают способность отдаляться, заселяя новые территории.
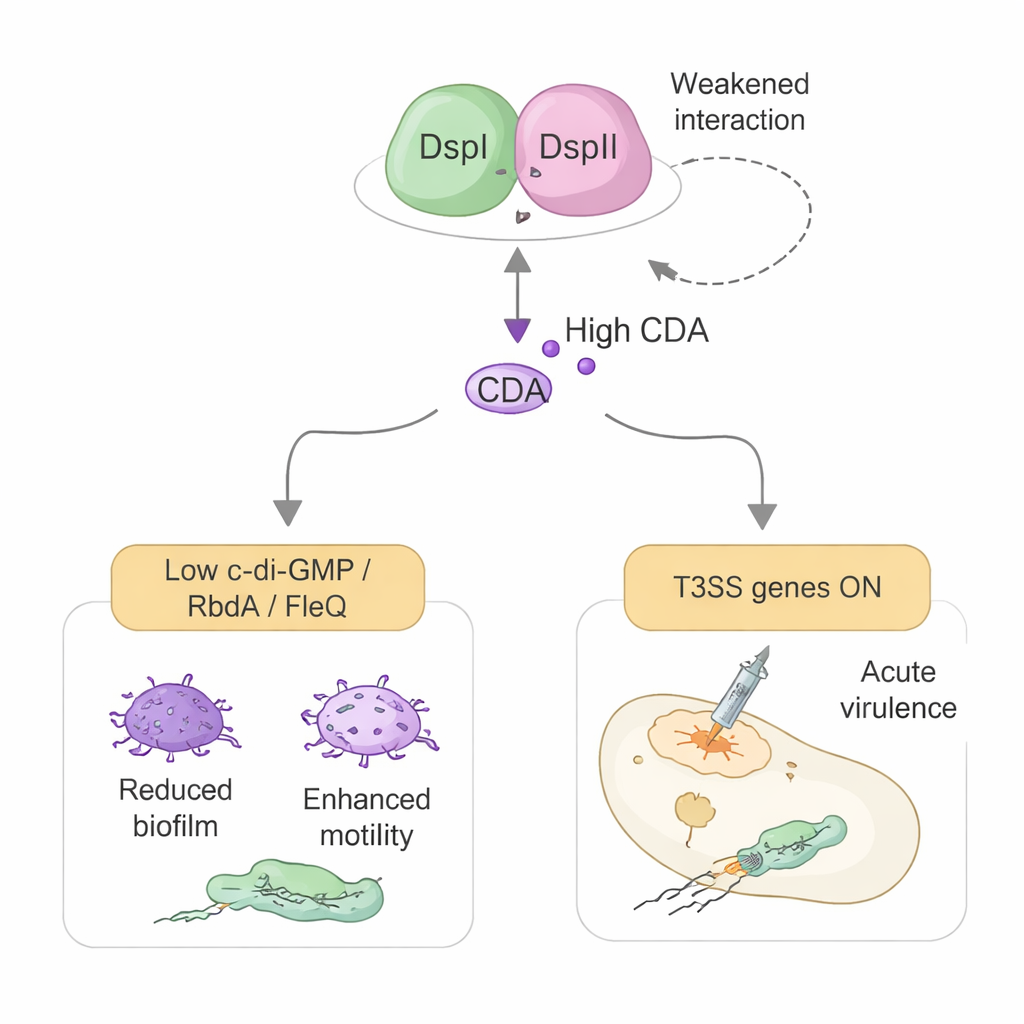
Перепрограммирование системы бактериального оружия
Исследование также выявляет вторую, неожиданную роль DspI и DspII, выходящую за рамки химии. Та же пара белков помогает включать систему секреции типа III (T3SS) — шприцеподобный аппарат, используемый для инъекции токсинов прямо в клетки хозяина. Этот эффект не опосредован CDA, а реализуется через прямой контроль генетических переключателей. DspI и DspII подавляют продукцию двух малых регуляторных РНК, RsmY и RsmZ, которые обычно тормозят синтез белков T3SS. Они делают это, связываясь с ДНК-регуляторным участком одной из этих РНК и физически взаимодействуя с главным регулятором GacA. Когда RsmY и RsmZ удерживаются под контролем, высвобождается движущий регулятор RsmA, и включаются гены T3SS и его главный контроллер ExsA, что повышает цитотоксичность в культурах клеток и приводит к гибели в модели инфекции насекомого.
Самонастраивающаяся система с мишенями для лекарств
Хитро устроено то, что сила партнерства DspI–DspII и их контроль над вирулентностью сами по себе настраиваются уровнями CDA. При низкой концентрации — как ожидается в клетках, только что покинувших биопленку — CDA укрепляет взаимодействие двух белков и поощряет дальнейший синтез сигнала и активацию T3SS. При высокой концентрации, характерной для плотных биопленок, CDA ослабляет их взаимодействие и снижает их способность связываться с ДНК, ограничивая дальнейший синтез сигнала и дорогостоящую выработку «оружия» у клеток, которые остаются на месте. Эта двойная роль делает комплекс DspI–DspII центральным узлом, связывающим размер популяции, уход из биопленки и острую вирулентность. Поскольку нарушение работы комплекса может блокировать как производство сигнала, так и активацию системы токсинов, он представляет собой привлекательную мишень для будущих препаратов, которые могли бы удерживать Pseudomonas в менее вредном хроническом состоянии и предотвращать опасные обострения.
Цитирование: Huang, J., Zhou, T., Zhou, X. et al. Dual-functional quorum sensing signal synthases DspII and DspI coordinate virulence switch in Pseudomonas aeruginosa. Nat Commun 17, 1926 (2026). https://doi.org/10.1038/s41467-026-68622-x
Ключевые слова: Pseudomonas aeruginosa, распад биопленки, кворумное восприятие, переключение вирулентности, cis-2-деценовая кислота