Clear Sky Science · ru
Пространственно разрешённый атлас рака желудка характеризует область с агрегированными лимфоцитами
Почему окружение вокруг опухоли имеет значение
Рак — это не просто скопление ненормальных клеток; он существует в оживлённом окружении, где соседствуют иммунные и структурные клетки, которые могут либо помогать бороться с опухолью, либо давать ей развиваться бесконтрольно. В этом исследовании с беспрецедентной детализацией картируется такое окружение при раке желудка, показывая, как микроскопические «горячие» и «холодные» участки внутри одной и той же опухоли могут влиять на то, ответит ли пациент на современные иммунотерапии.
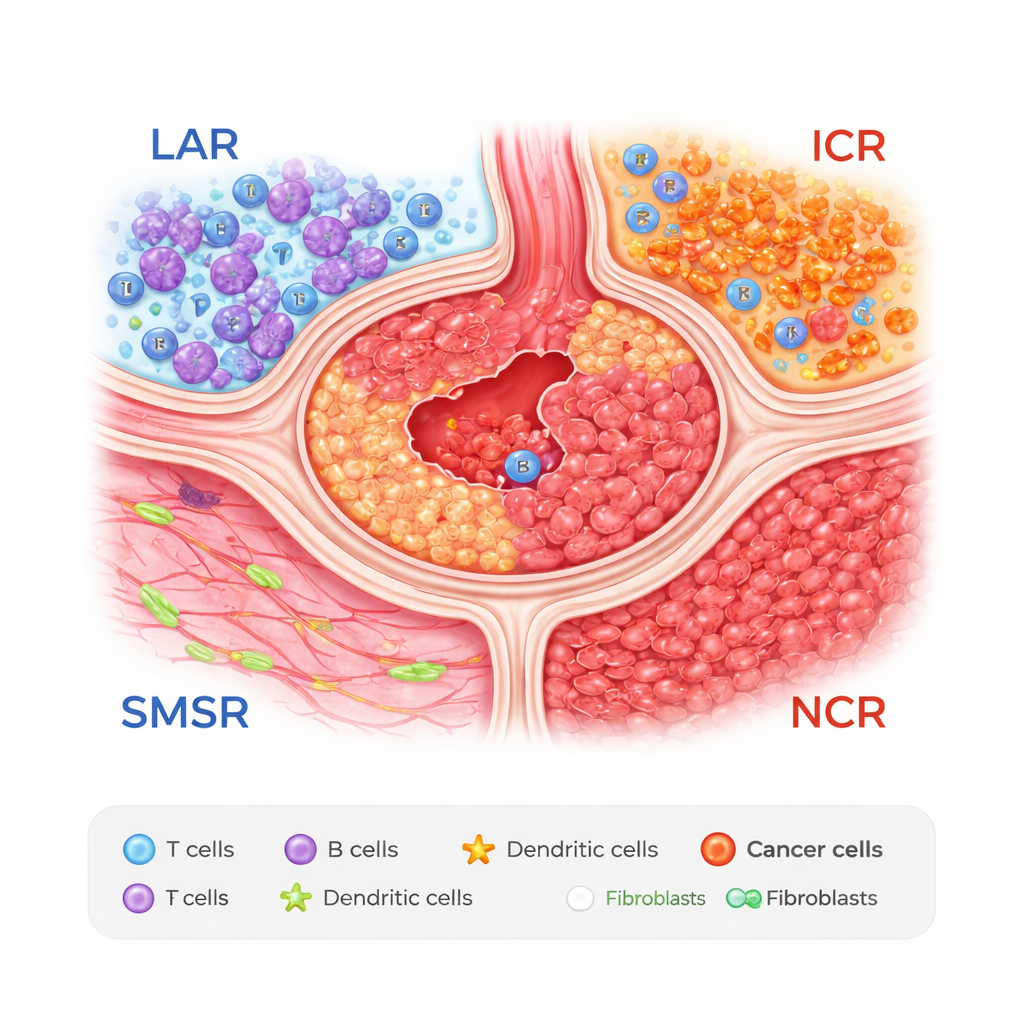
Четыре зоны внутри опухоли желудка
Исследователи объединили два мощных подхода: секвенирование РНК по отдельным клеткам, которое считывает активность генов в индивидуальных клетках, и пространственную транскриптомику, фиксирующую, где эти клетки располагаются в срезах ткани. Изучив образцы от 27 пациентов, они обнаружили, что опухоли желудка можно разделить на четыре повторяющиеся зоны. Одна из них — область с агрегированными лимфоцитами (LAR), богатая скоплениями Т- и В-клеток, напоминающими миниатюрные лимфатические узлы. Другая — область гладкой мускулатуры и стромы (SMSR), где доминируют мышечные и соединительные ткани. Оставшиеся две зоны — области, насыщенные раковыми клетками: иммуногенная раковая область (ICR), где клетки опухоли смешиваются с некоторыми защитными типами желудочных клеток, и негативно-иммуногенная раковая область (NCR), плотно заполненная злокачественными клетками и относительно бедная защитными иммунными клетками.
Иммунные «горячие точки», связанные с лучшими результатами
Команда установила, что зона LAR обогащена генами, обычно характерными для лимфатических узлов, где иммунные клетки обучаются и активируются. Сюда входят сигналы, помогающие привлекать лимфоциты и организовывать их в структуры, называемые третичными лимфоидными структурами. При анализе больших общедоступных онкологических наборов данных опухоли с более высокой экспрессией генов, связанных с LAR, как правило, демонстрировали лучшее выживание пациентов и несколько более высокую вероятность ответа на терапию ингибиторами контрольных точек, снимающими «тормоза» с Т-клеток. Напротив, генетические подписи, характерные для мышечно-обогащённых или сильно раково-насыщенных областей, чаще связывались с худшими исходами в различных типах рака.
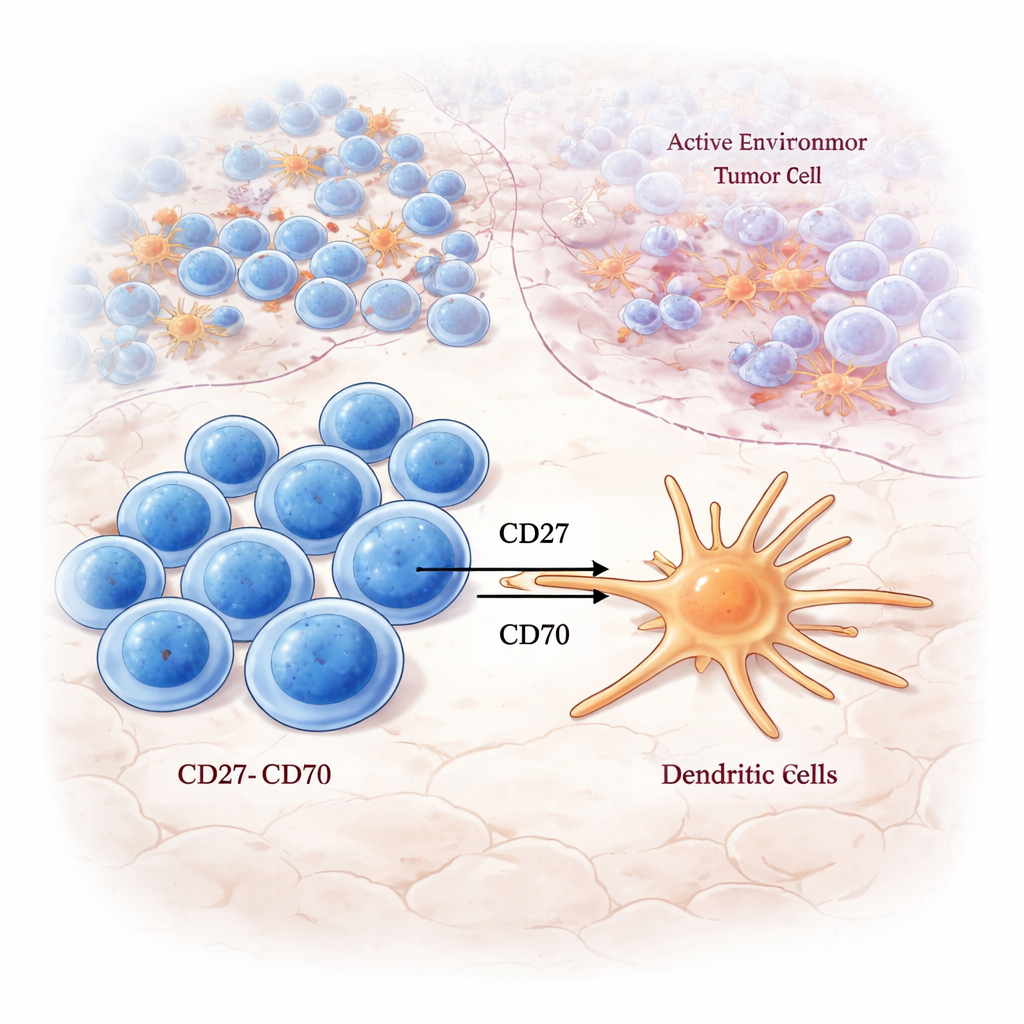
Где наивные Т-клетки учатся сражаться
Углубившись в LAR, авторы обнаружили сильную активность сигнальных путей, ключевых для пробуждения Т-клеток: сигналинг через T‑клеточный рецептор, пути костимуляции и антигенная обработка. Наивные CD8+ Т-клетки — клетки, ещё не полностью принявшие решение атаковать конкретную мишень — особенно ассоциировались с этими сигналами активации внутри LAR, но не в других зонах. С помощью многокрасочной окраски они выявили CD8+ Т-клетки в LAR, несущие маркёры как обновления, так и пролиферации, что указывает на то, что эта область действует как локальная зона обучения и расширения, где готовятся свежие клетки, готовые бороться с опухолью.
Два варианта иммунного окружения
Не все LAR одинаковы. При группировке пациентов по клеточному составу их LAR исследователи выделили две модели. В опухолях «Группы A» LAR были близки по строению к классическим лимфатическим узлам, богаты специализированными В-клетками и дендритными клетками, а раковые области рядом с этими LAR заполнялись активированными, боеготовыми лимфоцитами. В «Группе B» LAR были менее развиты, а прилегающая раковая ткань содержала больше покоящихся, менее вовлечённых Т-клеток. Продвинутый компьютерный анализ изображений тканей подтвердил, что активированные иммунные клетки физически группируются вблизи более зрелых LAR, что указывает на то, что локальная архитектура может направлять, насколько энергично иммунная система атакует опухоль.
Сигналы контрольных точек в пространстве
Исследование также отслеживало, где именно экспрессируются иммунные «переключатели», известные как молекулы контрольных точек. Стимулирующие пары, такие как CD27–CD70, были сосредоточены в LAR, особенно в опухолях Группы A, связывая утомлённые, но реактивные к опухоли CD8+ Т-клетки с дендритными клетками, которые могли бы дополнительно усиливать их активность. Напротив, многие ингибирующие парные молекулы, например TIGIT–NECTIN2 и LAG3–LGALS3, были обогащены в NCR, самой насыщенной раковыми клетками зоне. Это указывает на то, что даже при наличии сигналов через T‑клеточный рецептор окружающий ландшафт контрольных точек может смещать локальный иммунный ответ в сторону атаки или подавления в зависимости от области опухоли.
Что это значит для пациентов
Для неспециалиста ключевое послание таково: где именно находятся иммунные клетки и сигналы внутри опухоли может иметь такое же значение, как и их количество. Эта работа показывает, что рак желудка содержит разные иммунные «окрестности», и что мощные, похожие на лимфатические узлы регионы рядом с опухолью связаны с более активными, лучше расположенными Т-клетками и более благоприятными исходами. Освоив распознавание и, возможно, усиление этих областей с агрегированными лимфоцитами, будущие терапии могли бы быть более точно подобраны — выбирать лекарства, комбинации или даже целевые подходы доставки, которые используют собственные внутренние иммунные опорные точки опухоли.
Цитирование: Gao, S., Qin, S., Wang, D. et al. A spatially resolved atlas of gastric cancer characterises a lymphocyte-aggregated region. Nat Commun 17, 2059 (2026). https://doi.org/10.1038/s41467-026-68612-z
Ключевые слова: рак желудка, микроокружение опухоли, третичные лимфоидные структуры, пространственная транскриптомика, иммунотерапия рака