Clear Sky Science · ru
ZFP57 — регулятор посленатального роста и здоровья на протяжении жизни
Как раннее молоко формирует здоровье на всю жизнь
То, что происходит в первые дни жизни, может отозваться десятилетиями. В этом исследовании показано, что один материнский белок, называемый ZFP57, помогает определять, насколько полно развивается молочная железа, что попадает в грудное молоко и как потомки растут и распоряжаются энергией в течение всей жизни. Отслеживая влияние этого белка от беременной матери до кормящих детенышей, авторы выявляют скрытый генетический уровень под хорошо известными преимуществами раннего питания.
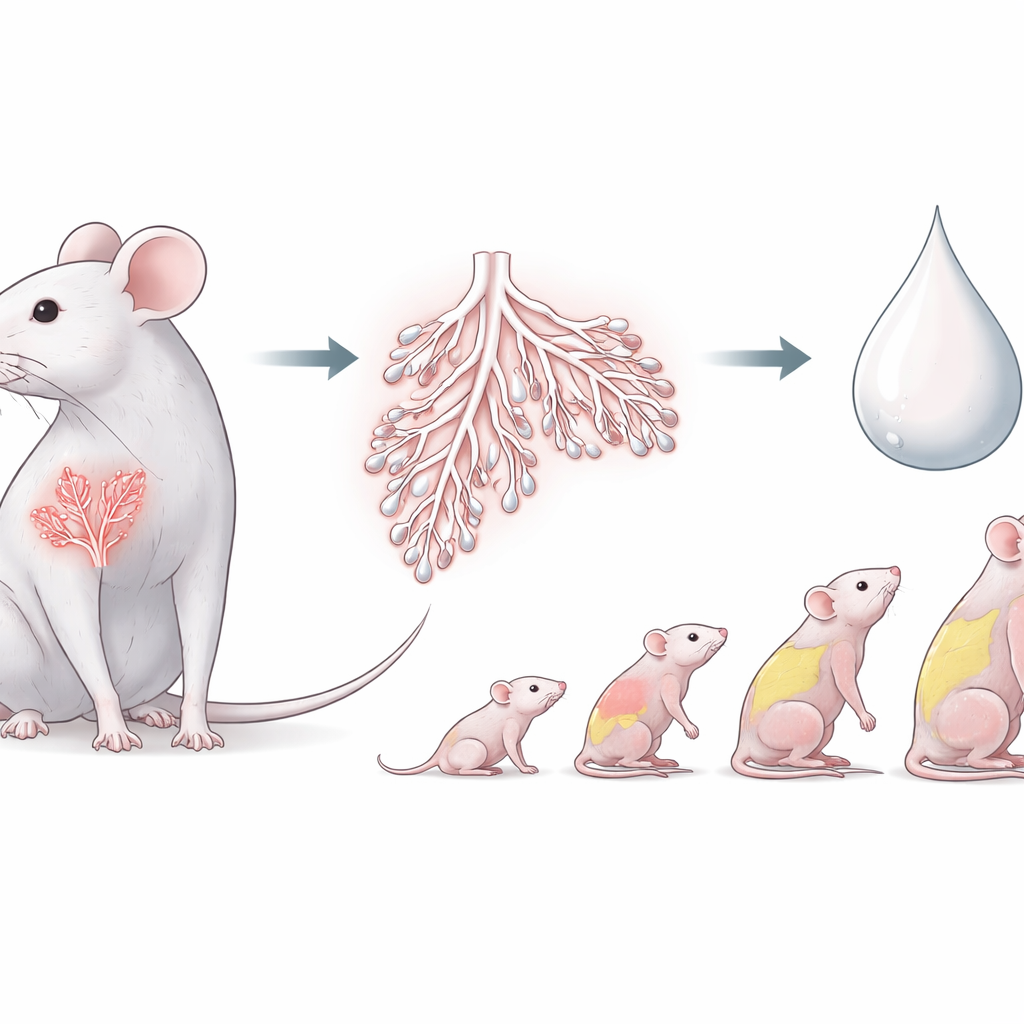
Хранитель роста до и после рождения
ZFP57 уже был известен как ключевой регулятор «геномного импринтинга» — химической маркировки, которая указывает, от какого родителя пришел тот или иной ген. Эти метки важны для нормального роста до рождения. Новая работа задается вопросом, важен ли ZFP57 и позже, после родов, когда матери кормят своих детей молоком. На мышах авторы показывают, что ZFP57 активен не только в эмбрионах и плаценте, но и во взрослых тканях, включая мозг и молочную железу. Это говорит о том, что та же молекула, которая помогает контролировать внутриутробный рост, может также управлять посленатальным питанием.
Как материнская железа настроена на кормление
Команда изучила молочные железы у нормальных самок и у самок с дефицитом Zfp57 на ключевых этапах: до беременности, во время гестации и в начале лактации. Они разделяли разные типы клеток и считывали активность тысяч генов. Хотя общее развитие железы в целом продолжалось, при отсутствии ZFP57 тонкие детали были нарушены. До беременности мутантные железы демонстрировали необычно плотное ветвление и раннюю активацию генов, которые обычно включаются позже, при подготовке к выработке молока. Во время гестации картина менялась: ветвление и активность генов, связанных с молоком, снижались, и многие клетки вступали в программу запрограммированной клеточной гибели. Эти изменения нарушали баланс между типами клеток, которые строят и поддерживают здоровый орган, производящий молоко.
Качество молока, модели роста и несовпадающие матери
Эти структурные и молекулярные сдвиги отразились на составе молока и на потомстве. У матерей с дефицитом Zfp57 молоко содержало больше окисленных жиров и меньше определенных фосфолипидов, которые помогают упаковывать липиды в капли. Детеныши, вскармливаемые такими матерями, независимо от их собственного генотипа, сначала росли медленнее, и некоторые не выживали. Тем не менее одна группа потомков, несшая специфическую мутацию Zfp57 и развивавшаяся в матке самок с дефицитом Zfp57, отреагировала иначе: несмотря на ранние проблемы с сосанием и задержку видимого потребления молока, в период лактации они набирали избыточный вес. Эксперименты по перекрестному вскармливанию, в которых новорожденных меняли между матерями разных генотипов, показали: наилучший рост наблюдался, когда генетический фон кормившей матери соответствовал условиям, пережитым в утробе. Когда детеныши, адаптированные к одной материнской среде, попадали к матери с другим генотипом, их рост и метаболизм часто сдвигались к крайностям.
От раннего кормления к взрослому метаболизму
История не закончилась отъёмом от груди. Исследователи наблюдали мышей в течение шести месяцев, что примерно соответствует ранней взрослой жизни у человека. Потомки, развившиеся у матерей с дефицитом Zfp57 и сами несущие измененную копию Zfp57, продемонстрировали стойкие изменения: больше жировой массы, меньше постной массы и более сильную зависимость от сжигания жиров вместо углеводов, даже при той же стандартной диете, что и контрольные животные. У некоторых также ухудшалось очищение глюкозы из крови — признак плохой толерантности к глюкозе, связанный с метаболическим синдромом. Примечательно, что эти долгосрочные проблемы были наиболее выражены, когда таких потомков перекладывали к нормальным матерям, что подчеркивает: несоответствие между пренатальной средой и посленатальным питанием может закрепить нездоровые траектории.
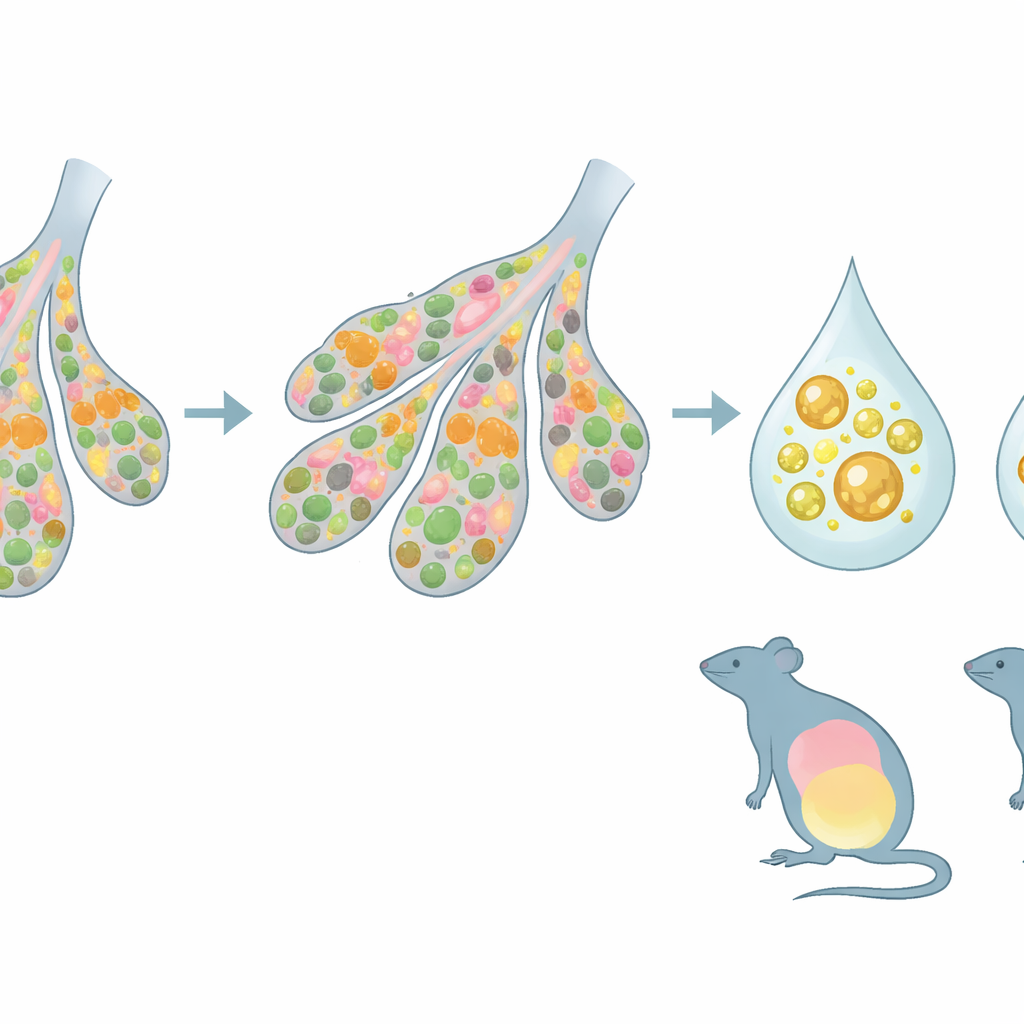
Почему это важно для здоровья человека
Открывая роль ZFP57 в формировании функции молочной железы и состава молока, независимо от его классической функции в импринтинге, эта работа связывает материнский ген с контролем ресурсов до и после рождения. Она поддерживает идею генетической коадаптации матери и потомства: среда утробы и молочный ресурс согласованы друг с другом, и нарушение этого соответствия может иметь долгосрочные издержки. Хотя исследование проведено на мышах, ZFP57 важен и у людей, где мутации связаны с метаболическими проблемами в раннем возрасте. Полученные данные указывают, что некоторые риски ожирения и диабета на всю жизнь могут возникать не только из-за диеты как таковой, но и из-за того, как наши гены формируют раннее питание и насколько пренатальная и посленатальная среды совпадают.
Цитирование: Hanin, G., AlSulaiti, B., Costello, K.R. et al. ZFP57 is a regulator of postnatal growth and life-long health. Nat Commun 17, 2080 (2026). https://doi.org/10.1038/s41467-026-68608-9
Ключевые слова: питание в раннем возрасте, эпигенетика, молочная железа, метаболическое здоровье, геномный импринтинг