Clear Sky Science · ru
Расширение ассортимента загружаемых веществ в конъюгатах антитело–лекарство с помощью доставки препаратов с гидроксильными группами через саморазрушающиеся фосфорамидаты
Более умные «ракетки» против рака
Противораковые препараты могут быть чрезвычайно сильнодействующими, но часто действуют как ковровая бомбардировка: поражают здоровые ткани почти так же сильно, как и опухоли. Конъюгаты антитело–лекарство (ADC) были созданы, чтобы решить эту проблему — они присоединяют мощный препарат к антителу, которое нацеливается на раковые клетки, превращая лечение в управляемую ракету. В этой статье объясняется новое химическое «соединение» между антителом и лекарством, которое делает такие «ракеты» более точными и гибкими, открывая путь для гораздо большего числа типов противораковых средств, чем могут нести современные ADC.
Почему современные таргетные препараты всё ещё ограничены
ADC состоят из трёх частей: антитела, распознающего маркер на раковых клетках, токсичного препарата («груза») и химического звена, которое их связывает. Большинство одобренных ADC полагаются всего на несколько типов грузов, которые повреждают ДНК или блокируют деление клеток схожими способами. Одна из основных причин — звено: оно должно надёжно удерживать препарат во время циркуляции в крови и затем чисто освобождать его внутри опухолевой клетки. Существующие звенья хорошо работают только с определёнными химическими группами в препаратах, особенно с аминами, и часто испытывают трудности со многими лекарствами, содержащими гидроксильные группы (–OH). В результате множество перспективных противораковых средств остаются неиспользованными, потому что их нельзя безопасно или эффективно доставить с помощью текущих конструкций ADC.
Заимствование приёма у противовирусных лекарств
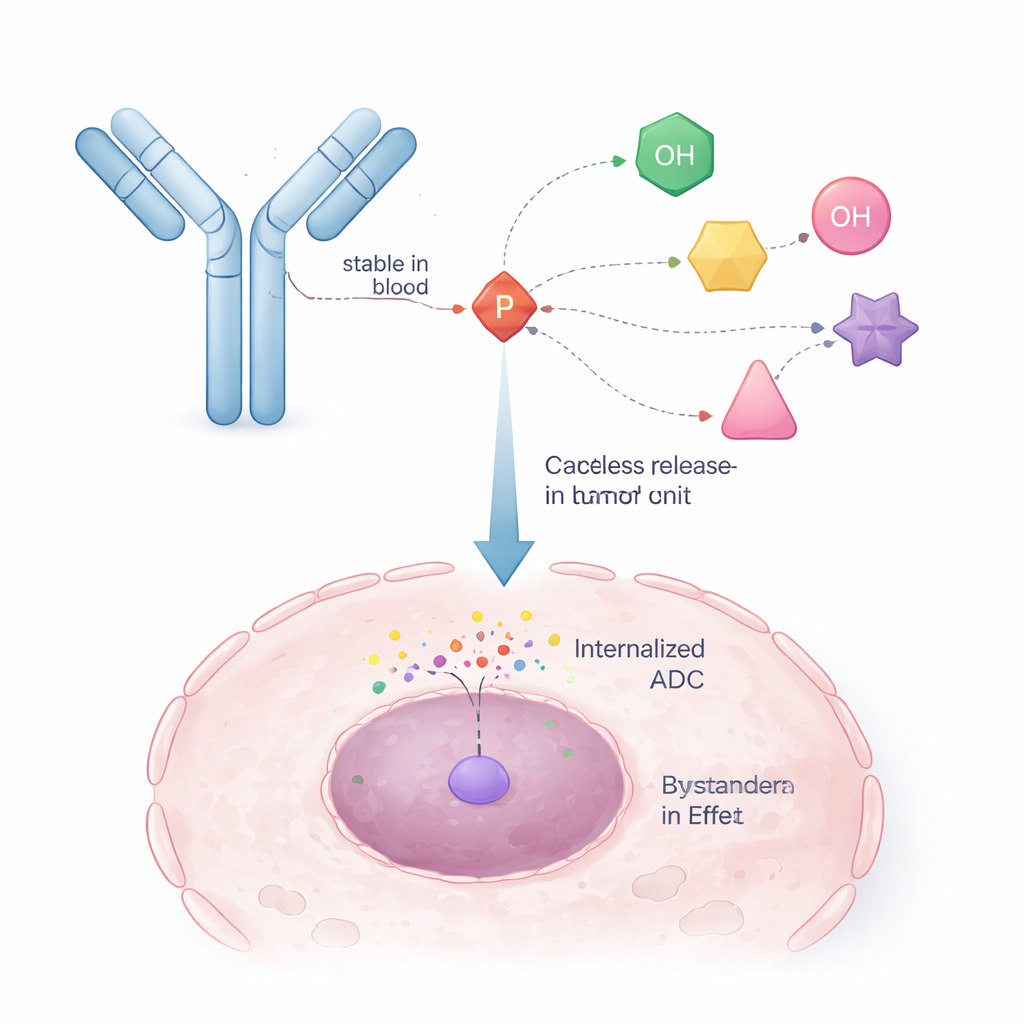
Исследователи обратились к стратегии, уже доказавшей свою эффективность в противовирусных препаратах, называемой ProTide. В этих лекарствах фосфорсодержащая химическая единица временно маскирует заряженную фосфатную группу препарата, чтобы тот мог попасть в клетки, а затем распадается внутри, высвобождая активную форму. Авторы переосмыслили эту концепцию так, чтобы одна «ветвь» фосфорного ядра использовалась для присоединения к антителу, а остальные держали противораковый препарат. Это создаёт «саморазрушающееся» звено: как только внутренний триггер (например, фермент в опухолевой клетке) отсекает небольшую часть структуры, фосфорный модуль контролируемо коллапсирует и высвобождает исходную молекулу препарата с восстановленной и немодифицированной гидроксильной группой.
Создание универсального химического «штекера»
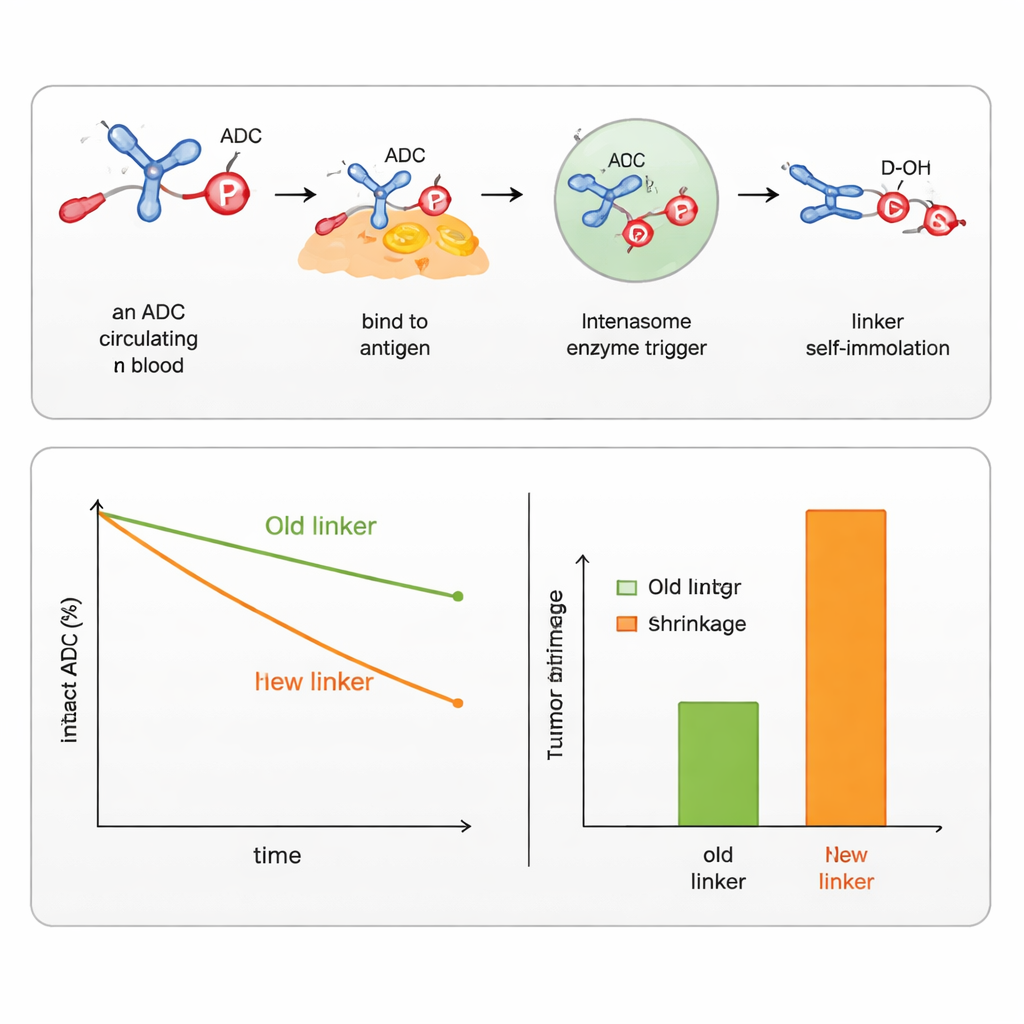
Команда показала, что, изменяя группы вокруг атома фосфора, можно точно регулировать, насколько стабилен коннектор в крови и как быстро он разрушается в клетках. Они разработали версии, реагирующие на несколько типов триггеров, характерных для раковых клеток, включая эстеразы и протеазы (ферменты, разрезающие определённые связи), а также ферменты, распознающие сахарные группы, или восстановительные условия в клеточных компартментах. С помощью этих конструкций им удалось успешно присоединять и освобождать как ароматические спирты (например, химиопрепарат SN38), так и алифатические спирты (например, DXd, груз в одобренном ADC для рака молочной железы). В сравнении с существующими коммерческими звеньями для SN38 и DXd новые фосфорамидатные звенья дольше удерживали препараты в сыворотке, доставляли больше лекарства в опухоли и вызывали более сильное уменьшение опухолей у мышей, при этом оказывая меньшее влияние на здоровые клетки.
Открытие многих новых грузов для противораковых препаратов
Чтобы оценить универсальность звена, исследователи собрали ADC, несущие десять различных препаратов, каждый из которых содержал по крайней мере одну –OH-группу, но действовал по очень разным механизмам внутри раковых клеток. Это включало ингибиторы синтеза ДНК, сворачивания белков (HSP90), энергетического обмена (NAMPT и DHODH) и трансляции белков, а также известные вещества, такие как паклитаксел и гемцитабин. Несмотря на широкий спектр структур, им удалось получить однородные ADC с высоким содержанием препарата для всех случаев. В клеточных исследованиях на разных типах рака большинство этих ADC показали наномолярную или даже субнаномолярную активность и явную селективность в отношении клеток, экспрессирующих мишень антитела, что подтверждает способность звена последовательно высвобождать активный препарат внутри нужных клеток.
Гемцитабин как демонстрационный пример
Гемцитабин широко используется в химиотерапии, но в своей обычной форме он так быстро удаляется из организма, что пациенты должны получать большие повторные дозы, что ограничивает максимально безопасный объём лечения. Используя фосфорамидатное звено, авторы присоединили гемцитабин к антителу, нацеленному на HER2, в одном из двух спиртовых положений и показали, что обе версии полностью восстанавливают активность после попадания в раковые клетки. В мышиных моделях HER2-положительных опухолей единичная доза ADC с гемцитабином — содержащая примерно в тысячу раз меньше суммарного гемцитабина, чем типичные схемы с свободным препаратом — обеспечила сильный и селективный контроль опухоли. Поведение ADC в кровотоке было близко к таковому у «голого» антитела, а высокие дозы хорошо переносились у крыс, что указывает на широкую маржу безопасности.
Что это означает для будущего лечения рака
Для неспециалистов главный вывод таков: эта работа предлагает новое, высокоадаптируемое химическое соединение, позволяющее антителам переносить намного более широкий набор противораковых препаратов, чем раньше, и делать это более безопасно. Обеспечивая удержание препаратов во время циркуляции и чистое высвобождение только после внутренней транспортировки ADC в раковую клетку, фосфорамидатные звенья повышают долю лекарства, попадающего в опухоль, и сокращают сопутствующее повреждение здоровых тканей. Не менее важно, что они позволяют переиспользовать существующие мощные малые молекулы с очень разной формой и механизмами действия в качестве таргетных терапий. Это может значительно расширить ассортимент доступных пациентам ADC и помочь бороться с опухолями, ставшими резистентными к ограниченному набору грузов, применяемых сегодня.
Цитирование: Ochtrop, P., Jagtap, A.P., Felber, J.G. et al. Expanding the payload scope in antibody-drug conjugates by delivery of hydroxy-containing drugs through self-immolative phosphoramidates. Nat Commun 17, 759 (2026). https://doi.org/10.1038/s41467-026-68605-y
Ключевые слова: конъюгаты антитело–лекарство, доставка противораковых препаратов, саморазрушающиеся звенья, фосфорамидатная химия, направленная химиотерапия