Clear Sky Science · ru
Регидивергентное и энантioселективное C–H цианирование вторичных аминов, контролируемое лигандом
Почему изменение крошечных связей важно для крупных лекарств
Во многих широко используемых лекарствах есть небольшие азотсодержащие блоки — амины. Незначительные изменения в том, как атомы соединены вокруг этих аминов, могут превратить слабое средство в мощное и избирательное лечение — или же в неактивное либо даже вредное вещество. В этой работе описан новый способ модификации аминовых фрагментов по желанию синтетика, позволяющий выбирать точное место на молекуле для реакции и желаемую зеркальную форму (энантиомеру), что критически важно для разработки более безопасных и эффективных препаратов.
Выбор одного участка в густонаселенном молекуле
Амины в лекарствах часто имеют несколько очень похожих связей углерод–водород (C–H), которые обычно ведут себя почти одинаково. Химикам хочется заменить лишь один из этих водородов на полезную группу, например «циано» (–CN), не затрагивая остальную часть молекулы. Это сложно, потому что стандартные реакции идут к наиболее реакционноспособному участку, определяемому структурой молекулы, а не выбором химика. Авторы работы используют простые гибкие вторичные амины с двумя разными алкильными цепями на азоте. Они показывают, что, начиная с одного и того же амина, можно направлять реакцию на один из двух соседних позиций — либо рядом с маленькой N‑метильной группой (т.н. α′‑позиция), либо на один углерод дальше по другой цепи (β‑позиция) — просто меняя лиганд, окружающий медный катализатор.
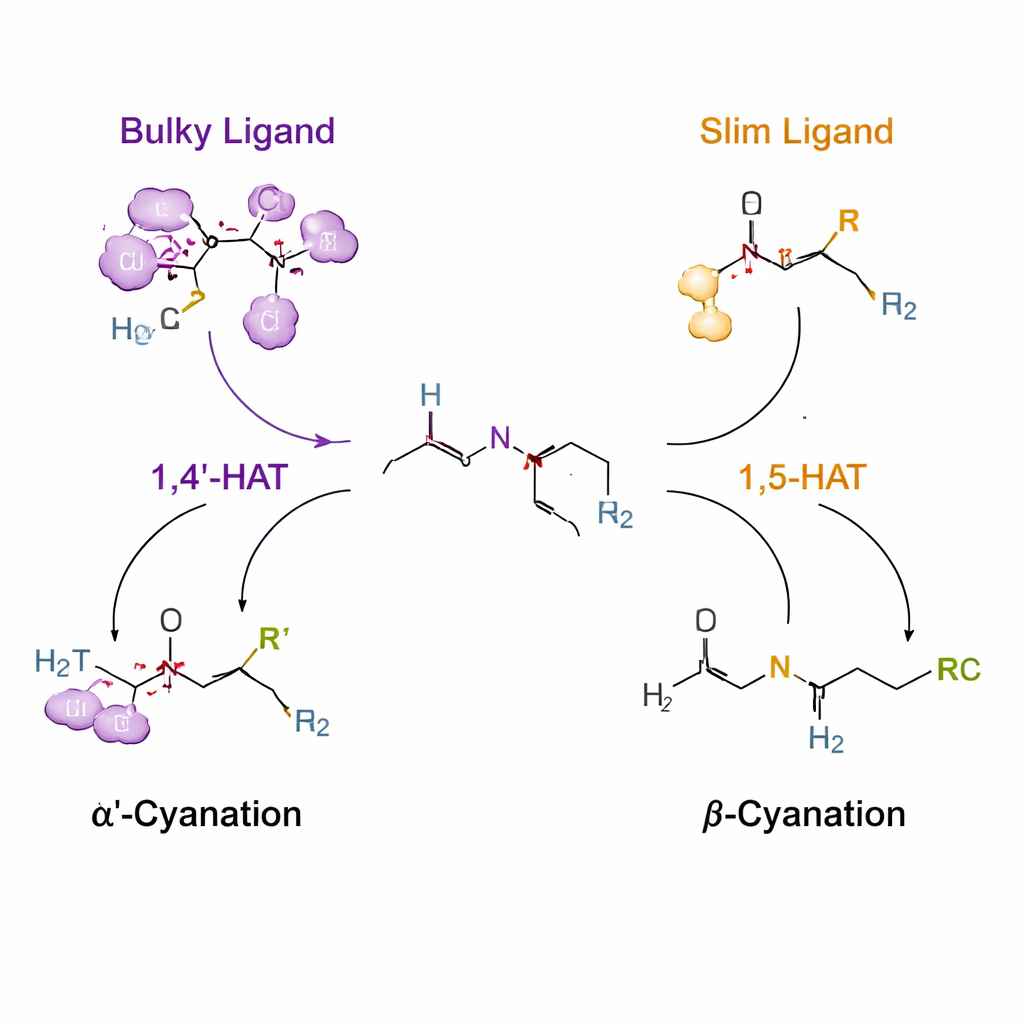
Использование управляемых «перескоков» водорода для направления реактивности
Ключевой прием основан на процессе, называемом переносом атома водорода (HAT), при котором короткоживущий радикал, центрированный на азоте, «срывает» водород с соседнего углерода. Как правило, такие радикалы предпочитают определенную длину взаимодействия, благоприятствуя шестичленным «достием», известному как 1,5‑HAT. Авторы присоединяют к амину временную уретановую (уреа) и хлорную ручки, так что при медной катализации формируется азотный радикал, который может забрать водород либо с α′‑, либо с β‑позиции. Путем проектирования лигандов — органических молекул, обвивающих медь — они изменяют окружение радикала. Очень громоздкий лиганд (обозначенный L14) сдвигает систему в сторону необычного шага 1,4′‑HAT, направленного на N‑метильную группу, обеспечивая селективное α′‑цианирование. Более тонкие лиганды (например, L8) допускают обычный путь 1,5‑HAT и тем самым направляют реакцию на β‑позицию.
От контроля положения к контролю «рукопожатия»
Кроме выбора места реакции, команда добивалась контроля над «праворукостью» или хиральностью, что важно, потому что многие лекарства существуют в виде левых и правых форм, которые по‑разному ведут себя в организме. Для этого они вводят хиральные лиганды — молекулы с собственной направленной формой — в медный комплекс. Два таких лиганда, L24 и L41, дают сильное предпочтение одной из зеркальных форм при установке циано‑группы в β‑положениях, включая как бензильные участки (рядом с ароматическими кольцами), так и аллильные участки (рядом с двойной связью C=C). На широком наборе аминовых субстратов метод обеспечивает β‑цианированные продукты с отличной селективностью как по участку реакции, так и по хиральности, и работает в грамм‑масштабе, показывая практичность и надежность процесса для синтеза.
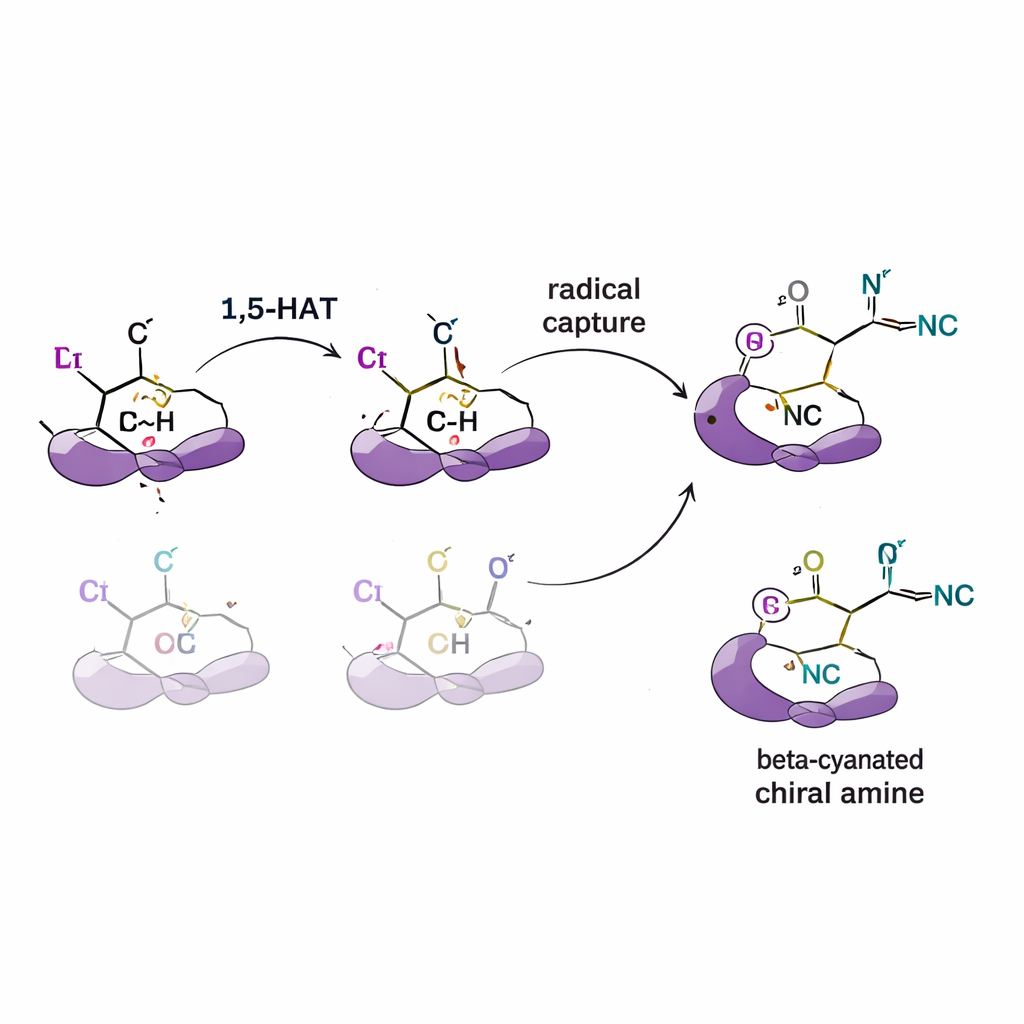
Проверка механизма селективности
Чтобы понять, как возникает этот контроль, авторы провели серию механистических экспериментов. Добавляя радикальные «ловушки», они подтверждают участие реактивных радикальных интермедиатов. Используя субстраты, в которых некоторые водороды заменены дейтерием (более тяжелый изотоп водорода), они обнаружили кинетические изотопные эффекты, указывающие на то, что шаг переноса водорода является медленным и определяющим селективность этапом реакции. Метки также показывают, что водород перемещается в одиночном, однонаправленном шаге, а не перескакивает туда‑обратно между позициями. Дополняющие вычислительные симуляции (теория функционала плотности) подтверждают эти выводы, указывая на то, что форма и объем лиганда изменяют энергетику конкурентных путей переноса водорода и последующего присоединения радикала к меди и цианиду, что в результате дает предпочтительную зеркальную форму.
Что это значит для будущей разработки лекарств
В целом эта работа представляет гибкую стратегию для переформирования распространенных аминовых групп в двух близких позициях по требованию с тонким контролем молекулярной хиральности. Меняя только лиганд в медном катализаторе, химики могут решить, поместить ли циано‑группу на малую N‑метильную единицу или на соседний углерод другой боковой цепи, и делать это в отношении многих сложных, похожих на лекарственные молекул. Поскольку циано‑группы являются ценными промежуточными звеньями для превращения в многие другие функциональные группы, подход «выбери место» и «выбери руку» упростит исследование и оптимизацию новых лекарств, построенных на одних и тех же базовых аминовых скелетах.
Цитирование: Mao, YJ., Chen, X., Li, HL. et al. Ligand-controlled regiodivergent and enantioselective C–H cyanation of secondary amines. Nat Commun 17, 1869 (2026). https://doi.org/10.1038/s41467-026-68598-8
Ключевые слова: функционализация аминов, перенос атома водорода, медная катализация, энантioселективное цианирование, медицинская химия