Clear Sky Science · ru
Двойная локализация в геноме и регуляторные функции гена MBD-2 с NuRD и без него у Caenorhabditis elegans, лишённой метилирования ДНК
Как крошечные черви переписывают правила контроля генов
Наши клетки используют химические метки на ДНК и белках, чтобы запоминать, какие гены должны быть включены или выключены. Одна из самых известных меток — метилирование ДНК — отсутствует у некоторых животных, но они при этом нормально растут и размножаются. В этой статье исследуют, как маленький червь Caenorhabditis elegans управляет регуляцией генов без метилирования ДНК и показывают неожиданно гибкую запасную систему, которая может изменить представления об эпигенетике.
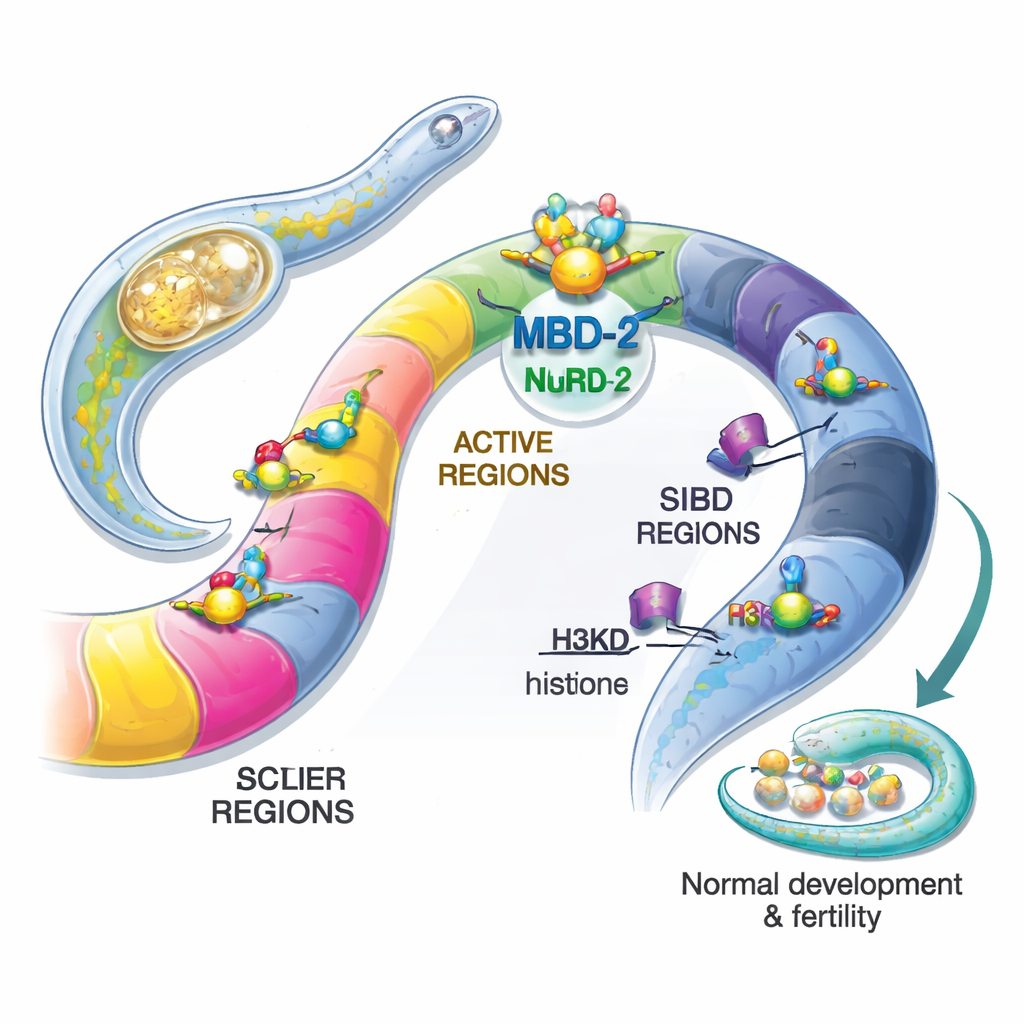
Отсутствие метки ДНК ставит большой вопрос
У млекопитающих химическая метка 5‑метилцитозин (5mC) помогает замалчивать гены во время развития, инактивировать X‑хромосому и защищать геном от мобильных элементов. Белки MBD2 и MBD3 распознают эти метки и привлекают большой белковый комплекс NuRD, который может перестраивать и деактивировать участки хроматина. Странно, но многие беспозвоночные, включая C. elegans и плодовых мух, утратили 5mC и ферменты, которые его ставят — однако они сохранили белок, похожий на MBD2/3. Возникает загадка: зачем хранить «ридер» метилирования ДНК в геноме, который уже не использует эту метку, и какую функцию он выполняет теперь?
Скарфолд-белок, без которого черви не выживут
Авторы сосредоточились на версии этого белка у червя, названной MBD‑2. В отличие от своих млекопитающих аналогов, червячий MBD‑2 утратил классический домен связывания метилированного цитозина, но сохранил гибкие и коиловые участки, которые могут цепляться за другие белки. Метив MBD‑2 флуоресцентными метками, исследователи показали, что он локализуется в ядрах почти всех клеток на протяжении всей жизни червя, что согласуется с широкой ролью в регуляции генов. С помощью генной инженерии они создали червей, полностью лишённых MBD‑2, или лишённых только его коилового домена, который обеспечивает контакт с NuRD. Обе мутации вызывали серьёзные нарушения: животные были мелкими, с плохой подвижностью, деформированными репродуктивными структурами и в основном стерильны. Это продемонстрировало, что MBD‑2 необходим для нормального развития и фертильности, даже при отсутствии метилирования ДНК.
Воссоздание машины NuRD в мире без метилирования
Чтобы выяснить, сохраняет ли червячий MBD‑2 взаимодействие с NuRD, авторы вытянули меченый MBD‑2 из экстрактов червей и идентифицировали его партнёров методом масс‑спектрометрии. Большинство известных компонентов NuRD были обнаружены, что подтверждает роль MBD‑2 как центрального скарфолдера в этом комплексе, аналогично MBD2/3 у млекопитающих. При удалении коилового домена многие из этих взаимодействий пропадали, особенно с белками, ремоделирующими нуклеосомы. В то же время масштабное РНК‑секвенирование показало, что более четверти всех генов червя изменяют свою активность в мутантах по MBD‑2, при этом значительно больше генов включается, чем выключается. Такая картина указывает, что MBD‑2, часто в связке с NuRD, в целом действует как репрессор, удерживая неподобающие гены в молчании, одновременно помогая поддерживать правильную активность подмножества сильно экспрессируемых генов.
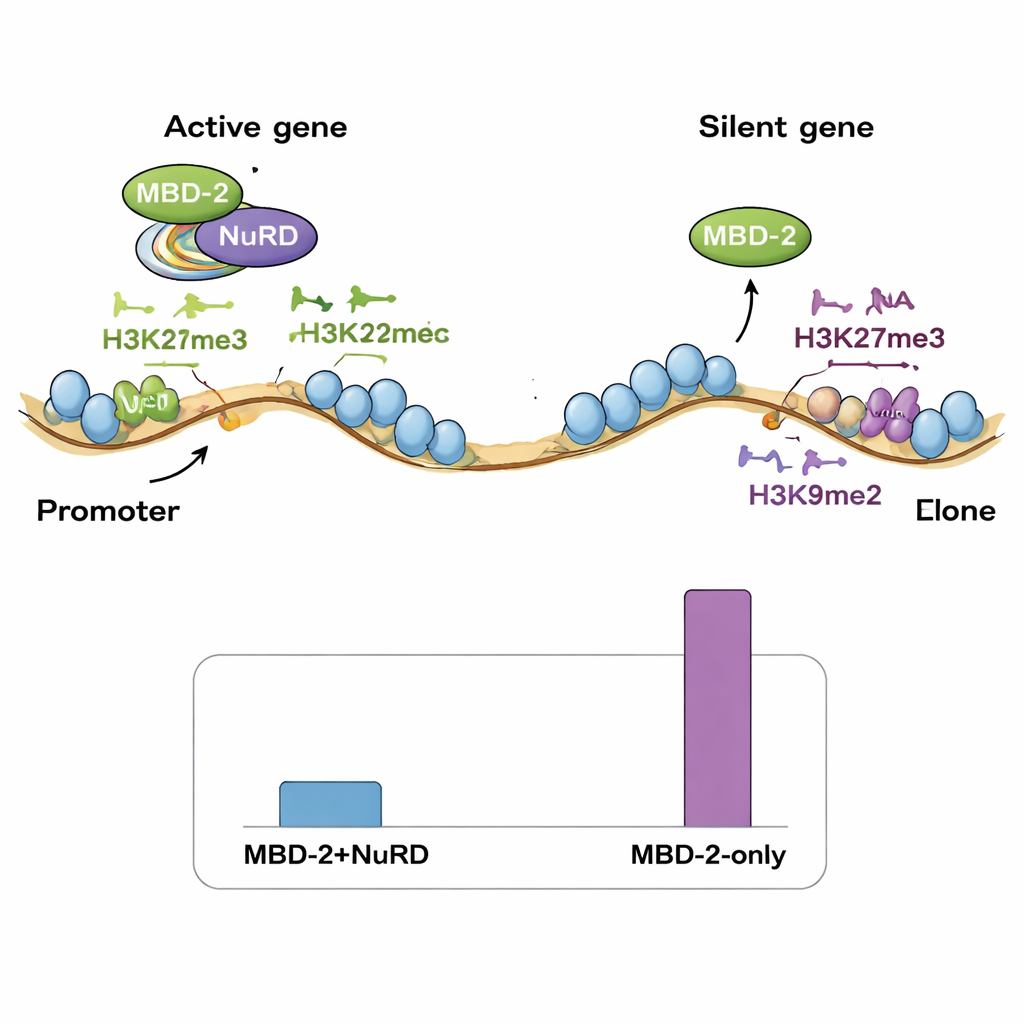
Два режима связывания в геноме
Далее команда картировала места привязки MBD‑2 по геному с помощью ChIP‑seq и сравнивала эти позиции с картами компонентов NuRD и различными метками на гистонах. Удивительно, но лишь небольшая доля сайтов MBD‑2 тесно перекрывалась с белками NuRD и метками открытой, активной хроматиновой области. Подавляющее большинство сайтов MBD‑2 находилось в других местах — в «рукавах» хромосом, богатых репрессивными метками гистонов, такими как H3K27me3 и H3K9me2/3. Иначе говоря, MBD‑2 демонстрирует двойное поведение: на меньшинстве сайтов он действует вместе с NuRD, тонко регулируя активные гены, а на многих других участках связывается независимо в уже молчащих регионах. Также важно, где внутри гена локализуется связывание — при скоплении MBD‑2 рядом с начальными участками генов потеря белка обычно приводит к активации этих генов, тогда как связывание глубже в теле гена часто связано с понижением экспрессии при утрате MBD‑2.
Эволюционный резерв при утрате метилирования ДНК
Авторы предлагают, что у видов, потерявших метилирование ДНК, репрессивные метки гистонов — особенно H3K27me3 — могли расшириться и занять похожую регуляторную нишу. Похоже, что червячий MBD‑2 был перепрофилирован: вместо чтения 5mC на ДНК он теперь ассоциируется с участками хроматина, помеченными специфическими модификациями гистонов, при этом по‑прежнему якорит комплекс NuRD через сохранённые домены белково‑белковых взаимодействий. Эта работа показывает, что древний инструмент для подавления генов может быть перебран эволюцией: химическая метка на ДНК может исчезнуть, но связанная белковая машинерия выживает, переключаясь на альтернативные сигналы. Для неспециалистов главный вывод таков: регуляция генов удивительно пластична — клетки могут утратить крупную эпигенетическую метку и тем не менее сохранять сложный контроль тысяч генов, больше полагаясь на другие метки хроматина и на универсальные скарфолдинговые функции белков вроде MBD‑2.
Цитирование: Tsui, H.N., Wong, C.Y.Y., Zheng, C. et al. Dual genomic localizations and gene regulatory functions of MBD-2 with and without NuRD in Caenorhabditis elegans which lacks DNA methylation. Nat Commun 17, 1875 (2026). https://doi.org/10.1038/s41467-026-68592-0
Ключевые слова: эпигенетика, хроматин, регуляция генов, C. elegans, модификация гистонов