Clear Sky Science · ru
Высоко динамичный монокоричный безгемаферный фермент железа для двухступенчатого биосинтеза изонитрилов
Как бактерии создают экзотические химические инструменты
Изонитри́лы — небольшие, но мощные химические группы, которые похожи на швейцарский армейский нож: они связывают металлы, участвуют в разнообразных реакциях и часто служат «ударной частью» сильнодействующих природных антибиотиков и токсинов. Некоторые патогенные бактерии, включая возбудителя туберкулёза Mycobacterium tuberculosis, присоединяют изонитрилы к липидным молекулам, чтобы выманивать металлы у хозяина. В этой статье рассматривается, как один из их ферментов, называемый Rv0097, выполняет эту необычно требовательную химию в два тщательно скоординированных этапа.
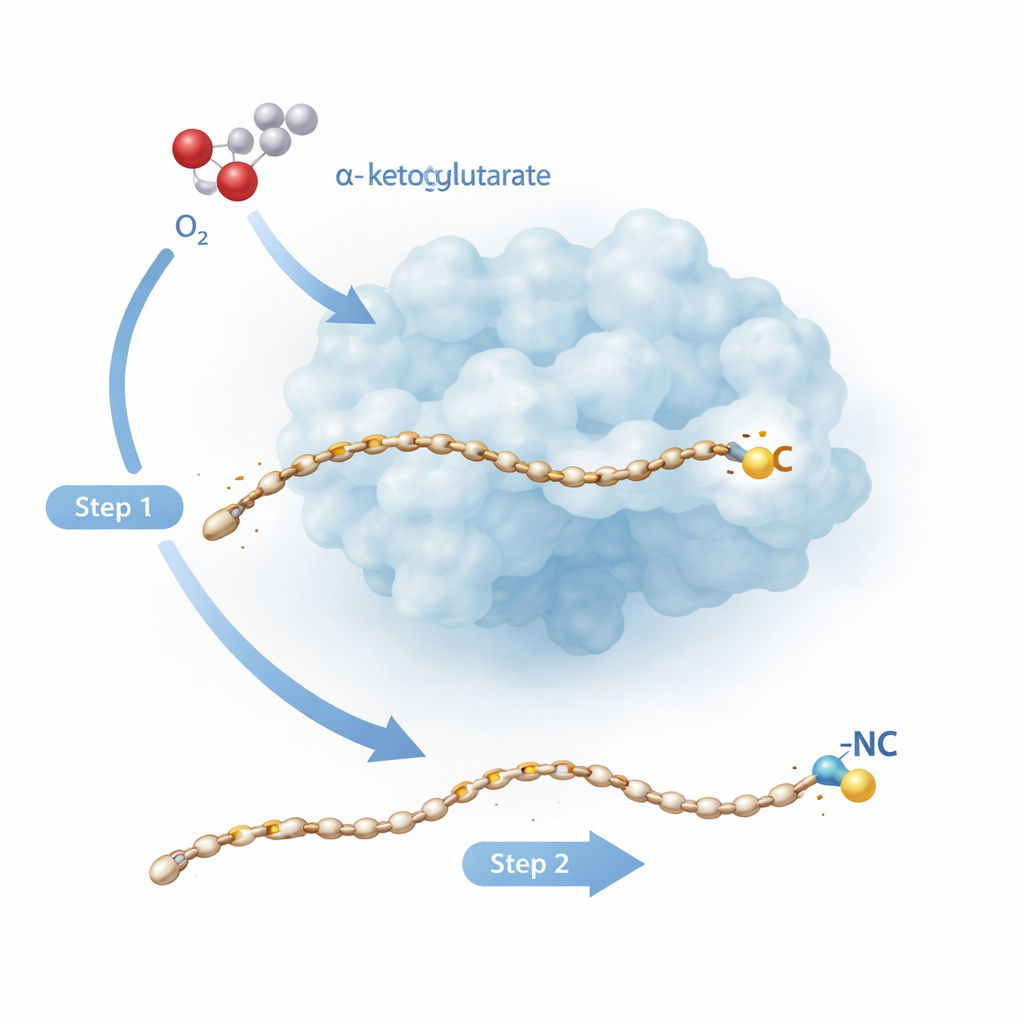
Двухступенчатое молекулярное преобразование
Rv0097 принадлежит к большой семье железозависимых ферментов, которые обычно выполняют более простые задачи, например добавление кислорода в одно место молекулы. Здесь задача сложнее: начиная с «глицил–жирнокислотного» строительного блока, фермент должен создать совершенно новую группу изонитрил, причём оба ключевых атома — углерод и азот — берутся из одного маленького фрагмента глицина. Предыдущие исследования родственного фермента ScoE показали, что это нельзя сделать за один приём. Вместо этого нужны два отдельных «полу‑цикла» реакции, каждый из которых запускается железо‑кислородным видом, образующимся при расщеплении вспомогательной молекулы α‑кетоглутарата и взаимодействии с атмосферным кислородом. Новое исследование обращается к туберкулёзному ферменту Rv0097, чтобы наблюдать на атомном уровне, как фермент связывает эти два радикальных шага на одном субстрате, не теряя контроля.
Замораживание фермента в действии
С помощью рентгеноструктурного анализа авторы получили шестнадцать высокоразрешающих «снимков» Rv0097 в различных состояниях: пустого, связанного с его липидным субстратом (десятиуглеродная молекула CADA), связанного с помощником α‑кетоглутаратом и в комбинациях, имитирующих мимолётные промежуточные состояния реакции. Эти структуры показывают, что у Rv0097 раздвоенная личность. В состоянии покоя активный центр в основном закрыт: ключевая аминокислота (фенилаланин 102) переключается между двумя ориентациями, удерживая длинный гидрофобный хвост в сухом кармане, готовом для липофильного связывания. Когда связывается CADA, этот остаток фиксируется в одной ориентации, полярная «головка» субстрата якорится заряженными боковыми цепями, а его масляный хвост устраивается в плотном туннеле. Мутации этой «заслоняющей» пары остатков (F102 и соседнего глицина G204) либо блокируют карман, либо пропускают слишком много воды, что резко снижает активность и изменяет предпочтительную длину цепей у фермента.
Двигающиеся крышки и динамичные петли
За пределами кармана для субстрата Rv0097 ведёт себя как крошечная машина с движущимися дверцами. Исследователи наблюдали «открытые» и «закрытые» конформации, в которых две крышкообразные области разводятся в стороны или сходятся над активным центром. Открытие обнажает центр железа и создаёт путь для входа α‑кетоглутарата и субстрата; закрытие защищает реакцию от окружающей воды, как только она запущена. Две гибкие поверхностные петли, называемые His‑петлёй и Arg‑петлёй по несущим их гистидину и аргинину, действуют как дополнительный затвор. В некоторых структурах эти петли загибаются внутрь, так что остаток аргинина может захватить α‑кетоглутарат; в других они отводятся наружу, очевидно образуя боковой канал, через который отработанные фрагменты помощника (сукцинат и углекислый газ) могут выйти, а свежий α‑кетоглутарат войти для второго шага — при этом промежуточный продукт, происходящий от субстрата, остаётся зажатым на месте.
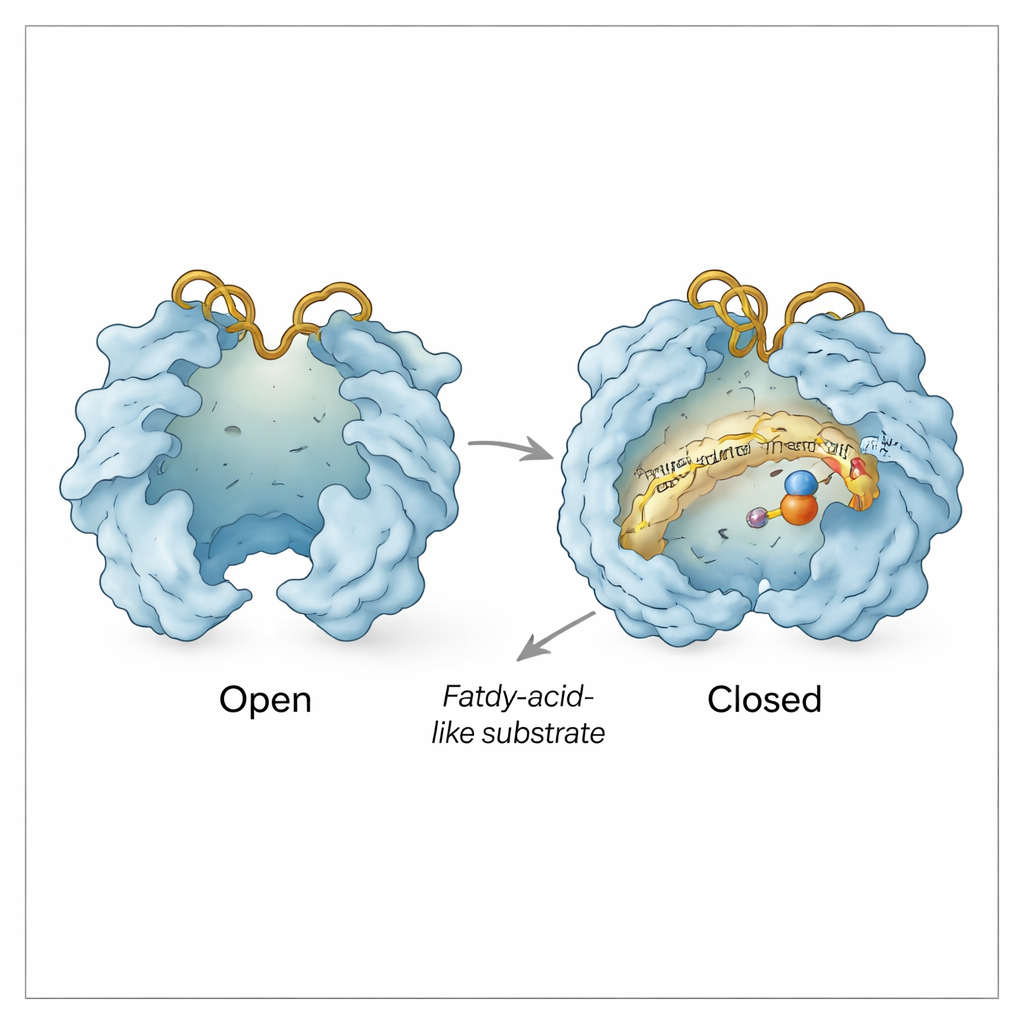
Защита хрупкого промежуточного продукта
Биохимические анализы подтверждают эту структурную картину. Первая половина реакции превращает CADA в крайне реакционноспособный имино‑промежуточный продукт, который быстро распался бы, оказавшись в растворе. Химически улавливая продукт распада, авторы показывают, что большая часть этого промежуточного соединения обнаруживается лишь в присутствии фермента, что подразумевает его связанное и защищённое состояние внутри Rv0097 между двумя полу‑реакциями. Структуры объясняют, как это достигается: тонкие перепозиционирования His‑ и Arg‑петель в сочетании с небольшими сдвигами соседних остатков, по-видимому, запечатывают промежуточный продукт в укромной полости, при этом оставляя контролируемые каналы для обмена малыми молекулами, такими как α‑кетоглутарат, сукцинат и углекислый газ.
Почему это важно для туберкулёза и не только
В сумме результаты показывают Rv0097 как высокодинамичную одно‑белковую конвейерную систему, которая дважды подряд использует железосодержащую химию на одном и том же субстрате, не выпуская опасный промежуточный продукт. Для бактерий, вызывающих туберкулёз, эта точность лежит в основе синтеза молекул, украшенных изонитрилом, которые помогают им получать жизненно важные металлы в организме; генетические исследования указывают, что этот путь важен для их выживания во время инфекции. Для химиков и разработчиков лекарств работа даёт план для инженерии родственных ферментов с целью создания новых соединений, содержащих изонитрил, и предполагает, что вмешательство в движущиеся крышки и затворы Rv0097 может быть путём разработки новых антибиотиков.
Цитирование: Ye, N., Del Rio Flores, A., Zhang, W. et al. A highly dynamic mononuclear non-heme iron enzyme for the two-step isonitrile biosynthesis. Nat Commun 17, 2034 (2026). https://doi.org/10.1038/s41467-026-68588-w
Ключевые слова: биосинтез изонитрилов, безгемаферный фермент железа, Mycobacterium tuberculosis, динамика ферментов, натуральные продукты, связывающие металлы