Clear Sky Science · ru
Нарушение гомеостаза железа повышает чувствительность рака поджелудочной к необратимой электропорации
Объединяя электричество и железо против смертельно опасного рака
Рак поджелудочной железы — один из самых трудноизлечимых типов рака: даже агрессивные локальные методы часто не предотвращают рецидив. В этом исследовании изучается новый способ увеличить эффективность и безопасность существующей процедуры — необратимой электропорации (IRE), которая убивает опухоль короткими мощными электрическими импульсами. Умело нарушая то, как раковые клетки обращаются с железом, авторы показывают, что можно заставить уцелевшие клетки вступить в разрушительный тип гибели, что потенциально снижает вероятность возврата опухоли.
Почему одних электрических импульсов недостаточно
Необратимая электропорация лечит опухоли путем введения тонких электродов в опухоль или вокруг нее и подачи быстрых высоковольтных импульсов. Эти импульсы пробивают постоянные отверстия в мембранах клеток, убивая многие раковые клетки и вызывая иммунный ответ. Однако электрическое поле неоднородно. Участки, получающие несколько более слабые импульсы, могут оставлять живые раковые клетки, и эти выжившие способны дать начало новой опухоли. При внимательном изучении клеток рака поджелудочной и опухолей у мышей, подвергнутых сублетальному электрическому полю, выяснилось, что вместо гибели через железозависимый процесс — ферроптоз — эти клетки включали широкую антиоксидантную программу защиты. Ключевые защитные гены, в том числе участвующие в нейтрализации повреждений, связанных с железом, были активированы, что позволяло клеткам пережить стресс и восстановиться.
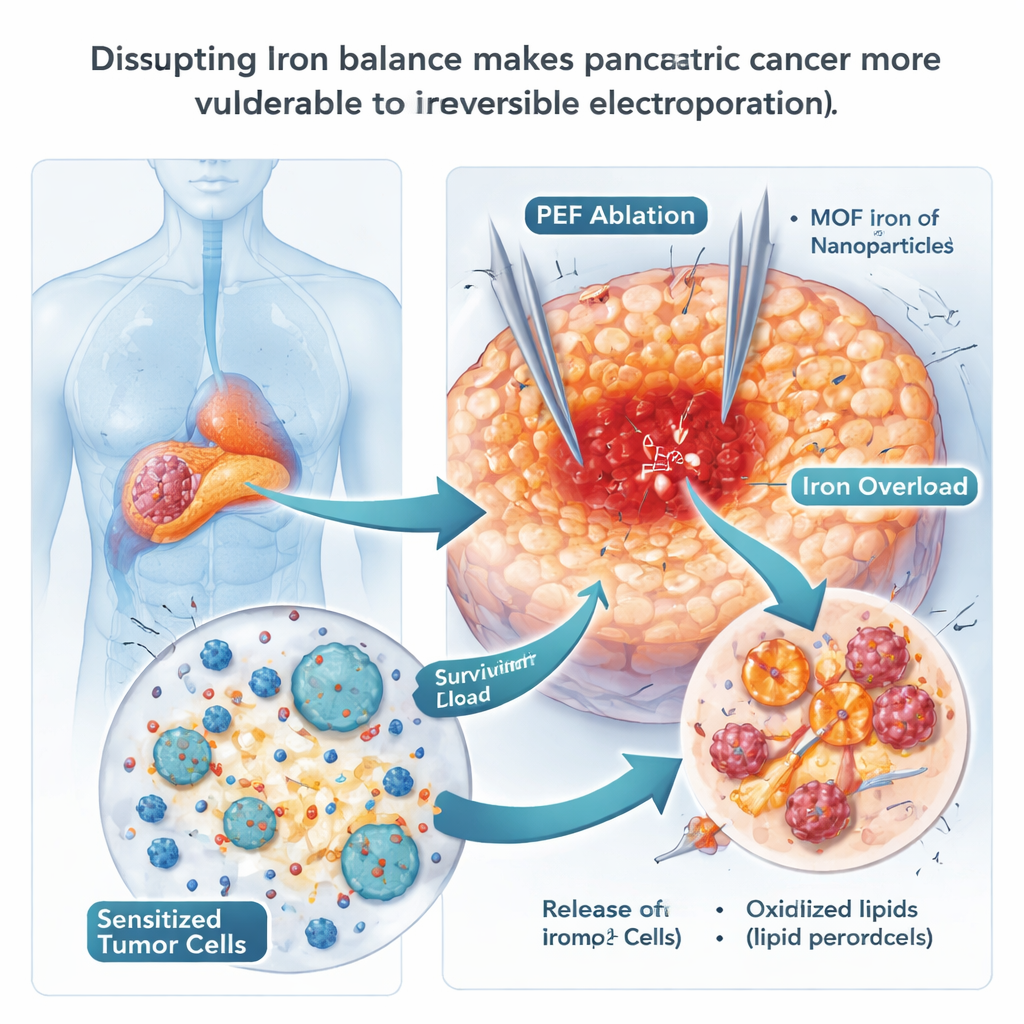
Использование наночастиц железа, чтобы подтолкнуть клетки к гибели
Поскольку ферроптоз зависит от железа, ученые проверили, смогут ли богатые железом наночастицы довести раковые клетки до края выживания. Они использовали специально разработанные частицы на основе металло-органической структуры, содержащие железо (MOF-Fe), которые быстро высвобождают железо внутри кислых компартментов клетки. В культурах клетки рака поджелудочной, поглощавшие эти частицы, накапливали свободное железо и окисленные жиры в мембранах — классические признаки ферроптоза — и образовывали значительно меньше колоний. У мышей сочетание MOF-Fe с IRE задерживало рост опухоли дольше, чем любое из этих лечений само по себе, и опухоли демонстрировали больше признаков окислительного повреждения. Однако эффект оказался временным: примерно через три недели опухоли начали рецидивировать, что указывает на способность рака адаптироваться к избытку железа.
Атакуя «сейф» клетки для железа
Чтобы понять эту резистентность, команда проанализировала, какие белки изменялись после лечения MOF-Fe. Выделялся тяжелый цепной фрагмент ферритина 1 (FTH1), часть комплекса хранения железа в клетке — молекулярный эквивалент огнеупорного сейфа для избытка железа. При экспериментальном повышении уровня FTH1 раковые клетки становились более устойчивыми к ферроптозу; при снижении FTH1 они становились более уязвимы. Это указало на FTH1 как на центральный щит от железозависимой гибели. Исследователи затем создали дизайнерскую молекулу C20U4V, состоящую из арахидоновой кислоты (легко окисляемый жир), связанной с «PROTAC»-каркасом, который направляет специфические белки в систему утилизации клеточных белков. В присутствии MOF-Fe C20U4V связывал ферритин и привлекал механизмы пометки и разрушения, резко снижая уровни FTH1 и лишая клетку возможности безопасно изолировать железо.
От культур клеток до мини-опухолей и мышей
При совместном применении MOF-Fe и C20U4V клетки рака поджелудочной демонстрировали повышенный окислительный стресс, больше поврежденных мембранных липидов, больные митохондрии и резко сниженные способности к регенерации. Этот синергизм также наблюдался в трехмерных органоидах, полученных от пациентов — крошечных опухелеподобных структурах, выращенных из материалов реальных пациентов — где пара препаратов приводила к сокращению размера и числа органоидов. Поскольку C20U4V маслянист и нерастворим в воде, его поместили в крошечные мицеллы, чувствительные к реактивным формам кислорода (M-C20U4V), которые циркулируют в крови и могут высвобождать препарат в стрессированной, поврежденной опухолевой ткани. В моделях у мышей с опухолями под кожей и в поджелудочной, тройная комбинация IRE, MOF-Fe и M-C20U4V сокращала опухоли гораздо эффективнее и продлевала выживаемость по сравнению с любым одиночным или двойным лечением. Леченые опухоли содержали меньше делящихся клеток, больше маркеров ферроптоза и сильнее инфильтрировались Т-клетками и другими клетками иммунной системы, что указывает на то, что стратегия не только напрямую убивает раковые клетки, но и помогает иммунной системе распознавать и атаковать опухоль.
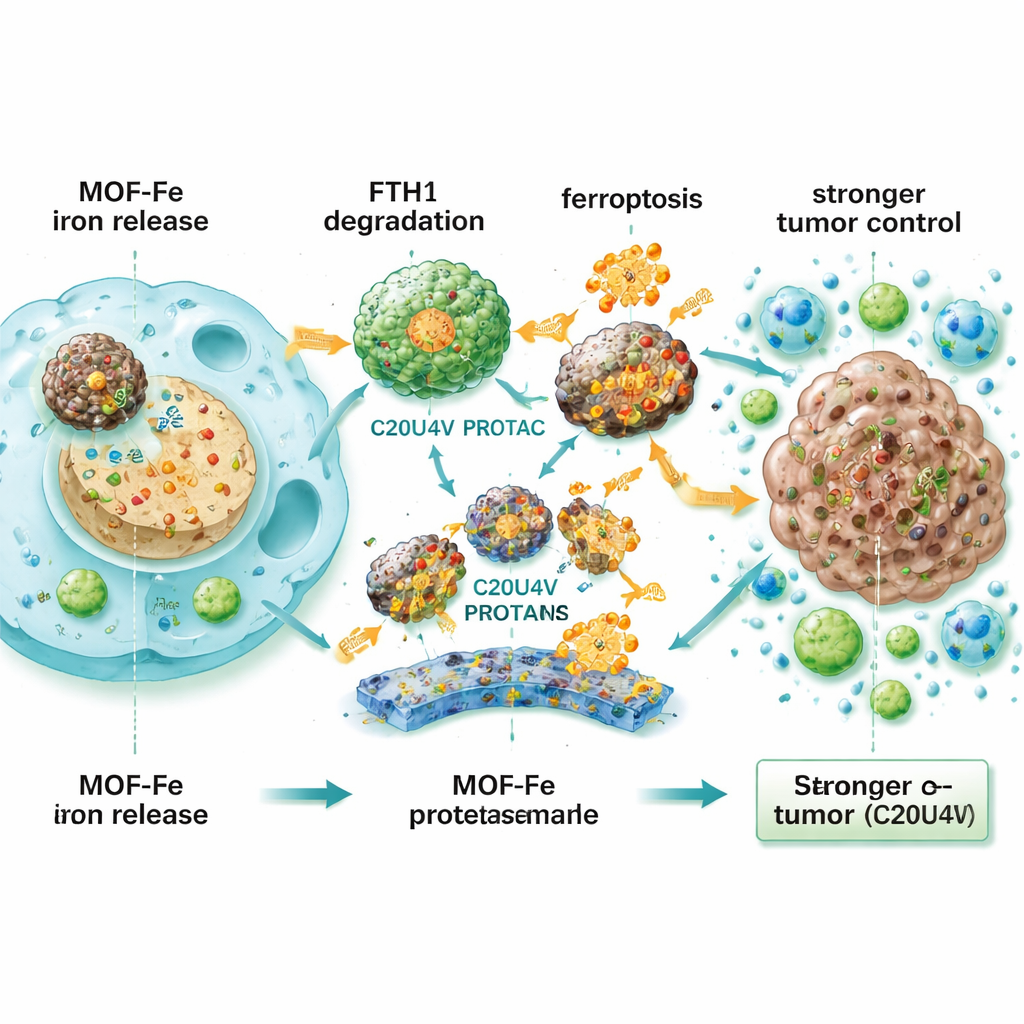
Что это может значить для пациентов
Для неспециалиста ключевая идея проста: опухоли поджелудочной часто ускользают после абляции электрическими импульсами, потому что некоторые раковые клетки выживают и быстро адаптируются. Эта работа показывает, что загрузив эти клетки железом и одновременно выведя из строя их «сейф» для железа, можно заставить их вступить в саморазрушительное состояние, против которого они не в состоянии сопротивляться. Хотя подход все еще на экспериментальной стадии и потребует масштабных проверок на безопасность и реализуемость у людей, он демонстрирует, что тонкая настройка того, как опухоль обращается с таким базовым элементом, как железо, может превратить несовершенную локальную терапию в более решительный удар по одному из самых смертоносных раков.
Цитирование: Li, L., Su, S., Wang, Z. et al. Disruption of iron homeostasis sensitizes pancreatic cancer to irreversible electroporation. Nat Commun 17, 1866 (2026). https://doi.org/10.1038/s41467-026-68585-z
Ключевые слова: рак поджелудочной железы, необратимая электропорация, ферроптоз, наночастицы железа, терапия PROTAC