Clear Sky Science · ru
HIF поддерживает транскрипционный регуляторный контур экспрессии EPAS1 при почечно-клеточном раке почки
Почему рак почки требует пристального внимания
Почечно-клеточный рак почки (clear cell) — самая распространённая форма рака почки, и многим пациентам сейчас назначают препараты, блокирующие белок HIF‑2α. Эти лекарства могут уменьшать опухоли, но действуют не одинаково хорошо у всех. В данном исследовании поставлен простой, но важный вопрос: почему некоторые опухоли почки вырабатывают так много HIF‑2α и может ли понимание этого «включателя» помочь предсказывать, кто получит наибольшую пользу от лечения, и как разрабатывать новые методы терапии?
Датчик кислорода, который выходит из-под контроля
Здоровые клетки почки используют защитный белок VHL, чтобы держать под строгим контролем факторы, чувствительные к кислороду, известные как HIF. Когда кислорода достаточно, VHL помечает белки HIF для удаления, не давая им включать гены, которые стимулируют рост кровеносных сосудов и деление клеток. При почечно-клеточном раке почки VHL обычно теряется или повреждается. В результате один из членов семейства HIF, HIF‑2α (кодируемый геном EPAS1), избегает разрушения и накапливается. Предыдущие работы показали, что высокая активность HIF‑2α связана с более быстрым ростом опухоли и худшим прогнозом, и что блокирование HIF‑2α может замедлять или останавливать опухоли у некоторых пациентов. Однако молекулярные шаги, повышающие активность гена EPAS1 в опухолях почки, были плохо понятны.
Скрытый ДНК-включатель для онкогена
Используя образцы опухолей пациентов, данные одиночных клеток и модели раковых клеток, авторы показывают, что матричная РНК HIF‑2α существенно выше в почечно-клеточных опухолях по сравнению с нормальной почечной тканью или другими типами опухолей почки. Затем они сканируют регион EPAS1 в геноме в поисках химических и структурных отметок, указывающих на активную регулирующую ДНК. Это выявляет мощный энхансер — своего рода дальний генетический переключатель — расположенный примерно в 70 000 нуклеотидов вверх по течению от EPAS1, который специфически активен в clear cell опухолях. В опухолевых клетках хроматин в этом энхансере открыт, украшен метками активации и физически петлится для контакта с промотором EPAS1, тогда как в нормальных канальцевых клетках почки этот район в основном молчит. Активность этого энхансера коррелирует с повышенным уровнем EPAS1 в больших онкологических базах данных. 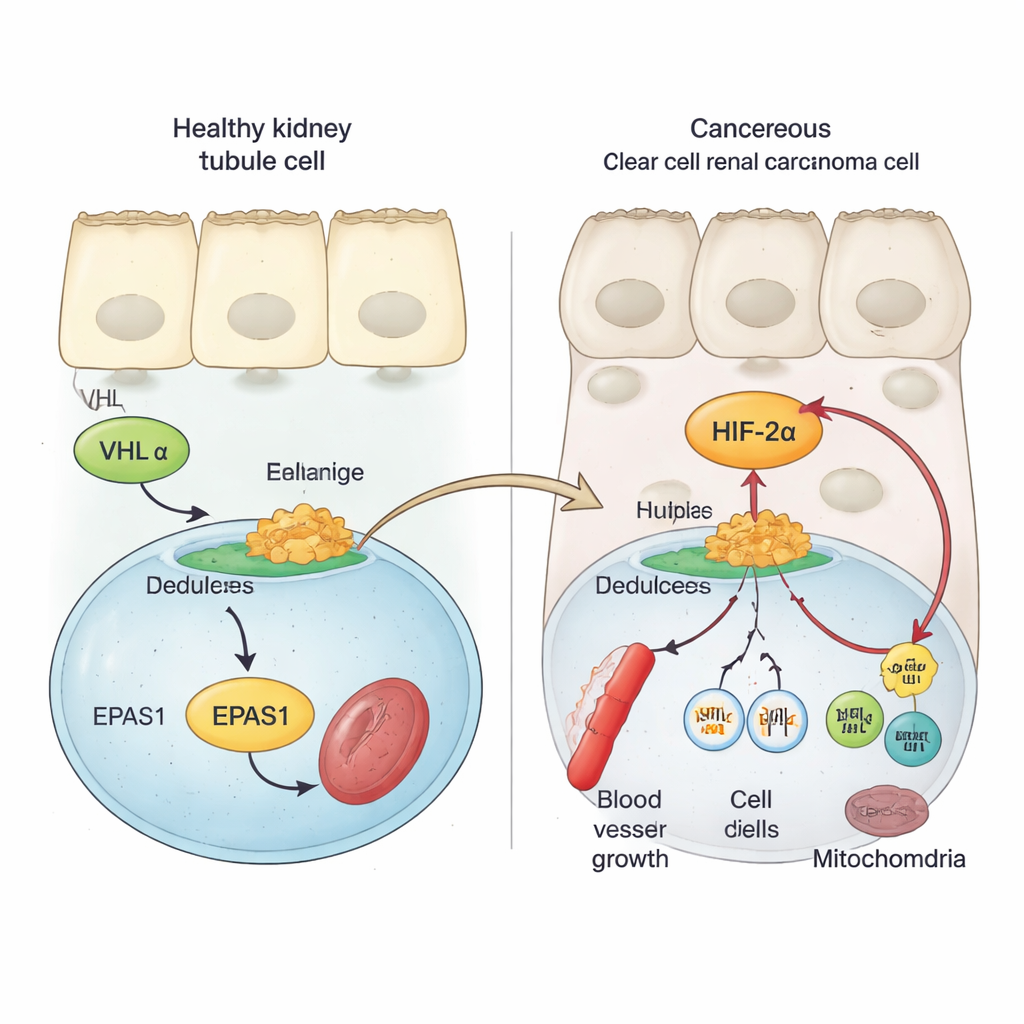
Самоподдерживающаяся петля, управляемая факторами почечной идентичности
Исследование показывает, что белки HIF делают больше, чем просто реагируют на низкий уровень кислорода — они фактически способствуют собственной продукции. Когда исследователи восстанавливают VHL или удаляют ключевого партнёра HIF (HIF‑1β), уровни EPAS1 падают и энхансер становится менее доступным. Прямое картирование контактов белок–ДНК показывает, что HIF связывается с двумя регионами энхансера выше EPAS1, включая энхансер, специфичный для clear cell. В клетках почечной опухоли этот энхансер также занят транскрипционными факторами PAX8 и HNF‑1β, которые помогают определять идентичность почечной клетки и известны как поддерживающие рост опухоли. Нарушение функции PAX8 или HNF‑1β, либо мутации в их сайтах связывания внутри энхансера, уменьшает количество РНК и белка HIF‑2α и ослабляет активность энхансера. В совокупности эти находки выявляют авто-регуляторный контур: HIF‑2α в сотрудничестве с факторами почечной линии усиливает активность энхансера EPAS1, что, в свою очередь, стимулирует дальнейшее производство HIF‑2α.
Генетический риск и поведение опухоли сходятся на одном контуре
Регион EPAS1 давно отмечается в исследованиях ассоциаций по всему геному как «горячая точка» риска рака почки: некоторые наследуемые варианты связаны с более высокой частотой рака и с мутациями VHL в опухолях. Объединив генетические данные и измерения экспрессии генов, авторы показывают, что люди, несущие версию ключевого варианта EPAS1 с высоким риском, как правило, имеют более высокие уровни HIF‑2α в своих опухолях — и даже в нормальных канальцевых клетках почки, когда HIF экспериментально стабилизируют. Это говорит о том, что наследуемые различия в ДНК могут настраивать чувствительность энхансера, предрасполагая некоторые почки к более сильному наращиванию HIF‑2α после потери VHL. Эксперименты на клетках глиобластомы показывают, что тот же энхансер может быть задействован и в некоторых опухолях мозга, что указывает на возможность повторного использования данного регуляторного модуля в других раках, где важна роль HIF‑2α. 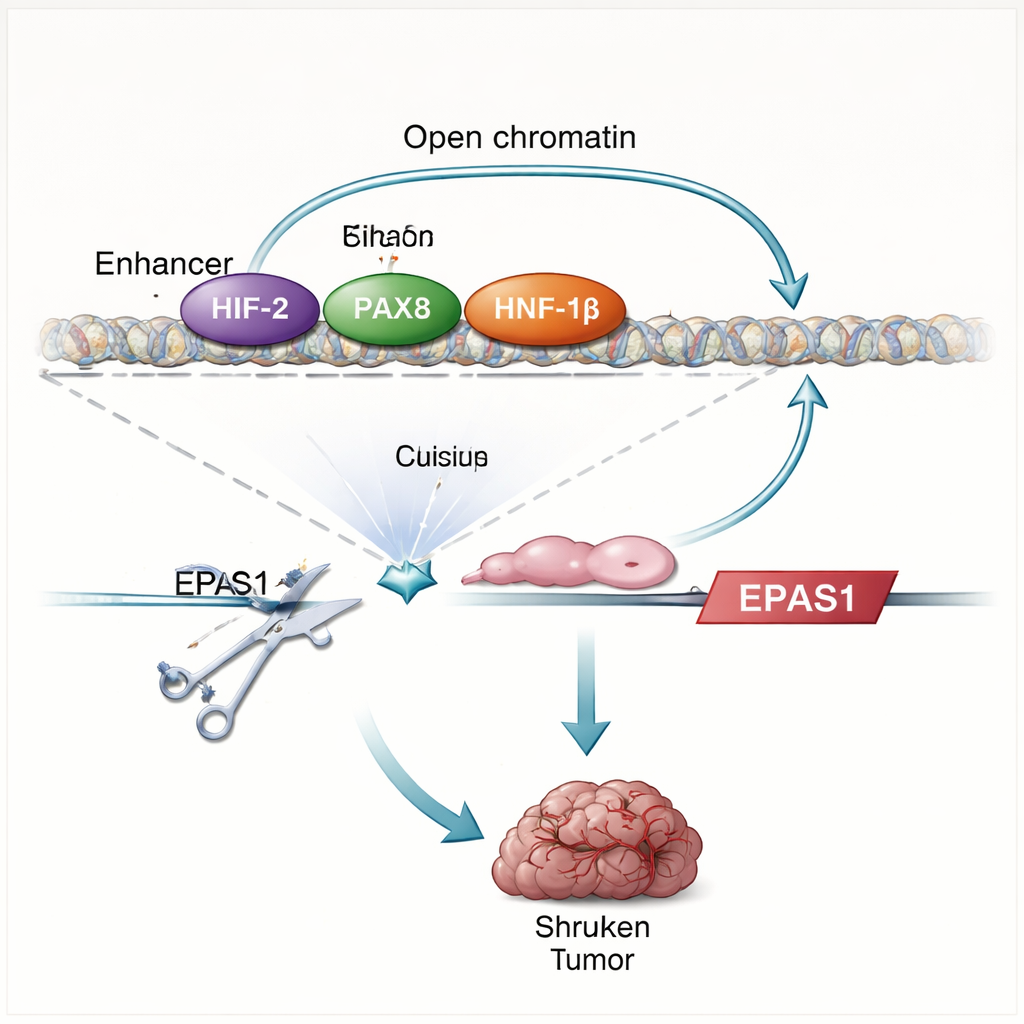
Разрыв петли для остановки роста опухоли
Чтобы проверить, насколько важен этот энхансер, команда использует редактирование генома CRISPR, чтобы повредить мотивы связывания HIF в нём в линиях клеток рака почки и в свежих опухолевых клетках пациентов. Это вмешательство сокращает уровень РНК HIF‑2α примерно на одну треть — до половины, снижает уровни известных мишеней HIF‑2α, таких как CCND1 и VEGFA, и ослабляет более широкую гипоксическую генную программу. Когда отредактированные клетки имплантируют мышам, они в основном не образуют опухолей, что резко контрастирует с контролями. Паттерн изменений экспрессии генов после нарушения энхансера тесно напоминает эффекты прямой блокировки HIF‑2α клиническим препаратом, подчёркивая, что этот единичный элемент ДНК является главным драйвером пути HIF‑2α в этих опухолях.
Что это значит для пациентов и терапии
Для неспециалистов ключевое сообщение состоит в том, что авторы обнаружили самоподдерживающийся ДНК‑включатель, который удерживает на высоком уровне важный онкогенный белок HIF‑2α в почечно-клеточных опухолях. Этот переключатель зависит как от потери тормоза VHL, так и от почечных вспомогательных факторов, и на него влияют наследуемые генетические варианты. Поскольку энхансер активно работает во многих clear cell опухолях и тесно связан с интенсивностью активации пути HIF‑2α, измерение его активности — или прямое нацеливание на него — может помочь выделить пациентов, которые наиболее вероятно получат пользу от существующих ингибиторов HIF‑2α, и предложить новые способы подавления этого пути, когда опухоли становятся устойчивыми к препаратам.
Цитирование: Naas, S., Krüger, R., Grampp, S. et al. HIF sustain a transcriptional regulatory circuit of EPAS1 expression in renal clear cell carcinoma. Nat Commun 17, 1764 (2026). https://doi.org/10.1038/s41467-026-68576-0
Ключевые слова: почечно-клеточный рак почки (clear cell), HIF-2α, энхансер EPAS1, мутация VHL, генетика рака почки