Clear Sky Science · ru
Атропоселективная прерванная CuAAC-реакция с использованием циклических диарилиодониев
Почему эта новая химия важна
Химики давно полагаются на простую «click»-реакцию, которая позволяет быстро и чисто соединять молекулярные строительные блоки — прием, лежащий в основе всего, от поиска лекарств до самовосстанавливающихся материалов. В этой статье описан изящный поворот классической click-реакции, позволяющий создавать более сложные трехмерные молекулы с заданной хиральностью — структуры, высоко ценимые в современной фармации и передовых материалах.
Дать классической click-реакции новую задачу
Отправной точкой является медью катализируемое присоединение азида к алкину, обычно называемое CuAAC. Оно соединяет два небольших компонента — азид и алкин — в пятичленное кольцо триазола при мягких условиях и с выдающейся надежностью. Традиционно после формирования триазольного кольца роль меди фактически заканчивает реакцию. Однако в последние годы химики научились «прерывать» этот процесс, улавливая мимолетный медь–триазольный интермедиат с третьим партнером для построения более сложных продуктов. До сих пор такие прерывания не позволяли универсально контролировать молекулярную хиральность, что ограничивало их применимость для синтеза сложных хиральных молекул.
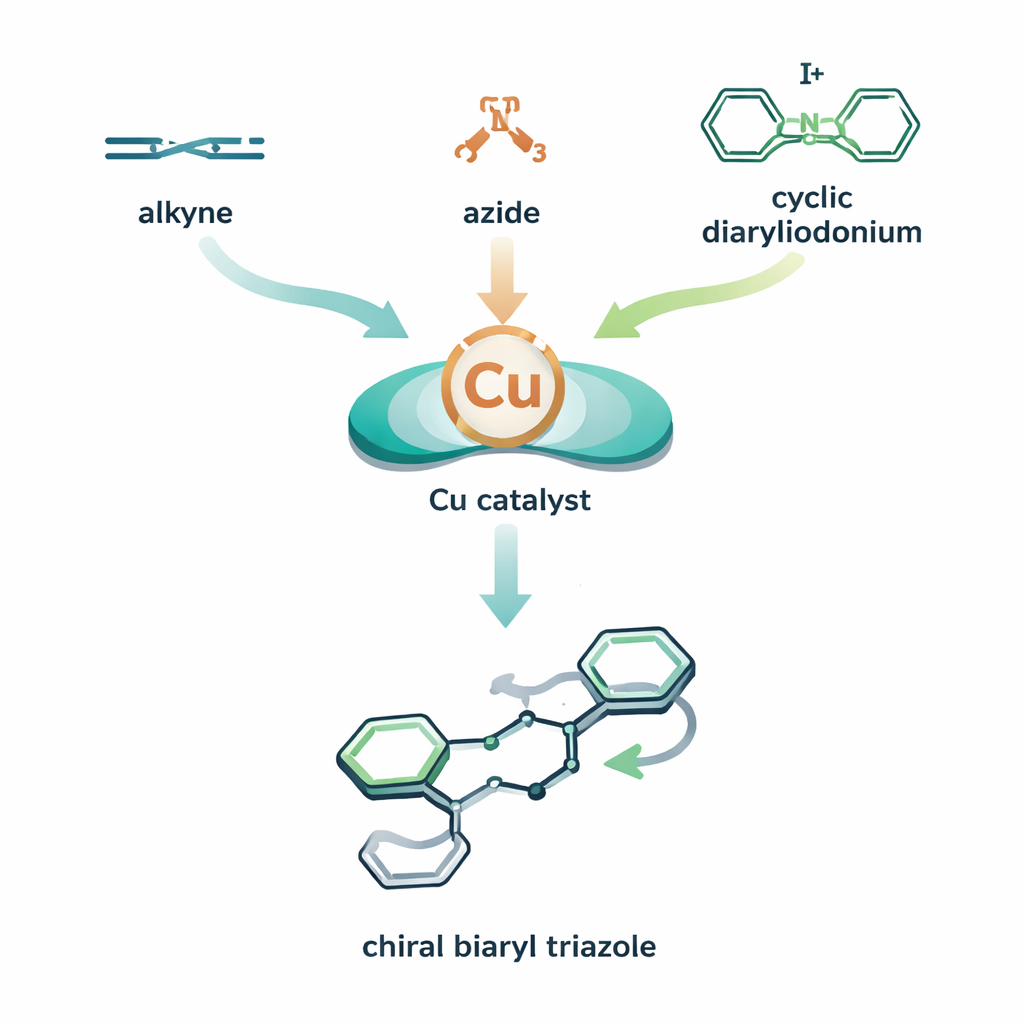
Молекулярная головоломка из трех частей с поворотом
Авторы объединяют два медных каталитических цикла в одном скоординированном процессе. В их схеме медный катализатор сначала помогает алкину и азиду сформировать медь–триазольный интермедиат. Прежде чем этот интермедиат будет нейтрализован, вводят третий компонент — кольцевую, высокореактивную йодсодержащую молекулу, называемую циклическим диарилиодонием. Медь внедряется в это кольцо и затем раскрывает его, присоединяя одну из ароматических фрагментов к триазолу. В результате получается биарил-триазол: две кольцевые системы, соединенные вокруг связи, которая может выступать в роли хиральной оси, подобно пропеллеру, способному закручиваться влево или вправо. Сочетая медь с тщательно подобранным хиральным лигандом, команда смещает баланс так, чтобы один из поворотов образовывался гораздо чаще другого, добиваясь высокой атропоселективности (контроля над тем, какая осевая «рука» формируется).
Оценка гибкости и надежности метода
Чтобы понять, насколько универсальна эта реакция, исследователи систематически варьировали каждый из трех строительных блоков. Они показали, что в реакции участвуют многие разные алкины, включая содержащие электронно-обогащенные, электронно-обедненные и гетероароматические кольца, при этом сохраняются хорошие выходы и сильное предпочтение одной хиральной формы. Некоторые громоздкие замещения повысили селективность, но могли снижать выход, что указывает на компромисс между стерическим затруднением и эффективностью. Партнёры-азиды лучше всего работали, когда они происходили от простых сложных эфиров или амидов, либо от бензильных позиций; ряд таких азидов давал сильно обогащенные хиральные продукты. Циклический диарилиодоний также можно было настраивать: некоторые замещения сохраняли как выход, так и селективность, тогда как другие, особенно вблизи реакционноспособного атома йода, замедляли реакцию или снижали её показатели. В целом исследование предоставило широкую коллекцию новых атропизомеров биарил-триазолов, доступных в один шаг.
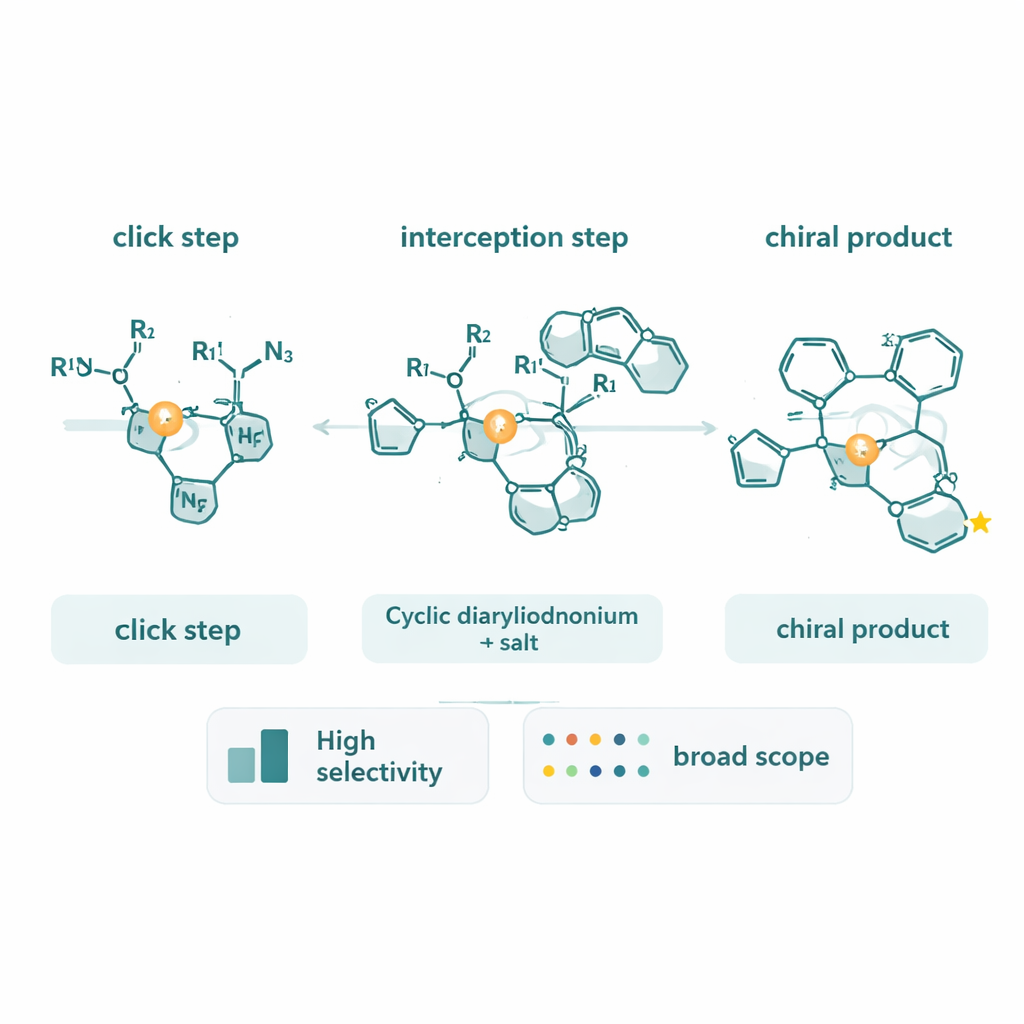
Заглянуть внутрь механизма реакции
Помимо синтеза новых молекул, команда посвятила значительные усилия выяснению механизма реакции. С использованием дейтерированных алкинов они наблюдали необычный обратный кинетический изотопный эффект, что указывает на лимитирующий стадию, в которой углерод алкина меняет характер своей связи, а не просто разрывает C–H связь. Анализ хода реакции с помощью калориметрии показал, что скорость реакции сильно зависит от концентраций алкина и азида, но слабо — от циклического диарилиодония. Эти измерения поддерживают картину, в которой формирование и преобразование медь–триазольного комплекса и его окислительное присоединение к кольцу диарилиодония совместно задают темп реакции. Они также обнаружили, что сами хиральные триазольные продукты могут связываться с медью и замедлять каталитический цикл, что указывает на пути дальнейшей оптимизации системы.
Что это значит для будущего
Проще говоря, исследователи научили хорошо известную click-реакцию новому приему: вместо того, чтобы просто соединять две части, она теперь помогает собирать три компонента в сложные, похожие на пропеллер молекулы, почти исключительно формируя один предпочтительный поворот. Это обеспечивает масштабируемый путь к хиральным биарил-триазолам — структурам, ценным как потенциальные лекарственные вещества, катализаторы и функциональные материалы. Механистические выводы — особенно о том, как ключевой интермедиат перехватывается и как продукт может «отравлять» катализатор — дают дорожную карту для разработки еще более эффективных и селективных вариантов этой химии. Для неспециалистов главное — уже мощный молекулярный «конструктор» стал более универсальным, позволяя химикам сооружать более сложные и полезные формы с тонким контролем их трехмерной структуры.
Цитирование: Li, Y., Yang, S., Duan, L. et al. Atroposelective interrupted CuAAC reaction using cyclic diaryliodoniums. Nat Commun 17, 944 (2026). https://doi.org/10.1038/s41467-026-68574-2
Ключевые слова: щелочная химия (click chemistry), медная катализация, хиральный биарил, атропизомер, триазол