Clear Sky Science · ru
Структуры нуклеотид-связанной человеческой теломеразы на нескольких этапах цикла добавления тандемных теломерных повторов
Почему концы наших хромосом важны
Каждый раз при делении клетки защитные колпачки на концах хромосом — теломеры — становятся немного короче. Если они укоротятся слишком сильно, клетки прекращают делиться или начинают работать неправильно, что способствует старению и заболеваниям. Молекулярная машина под названием теломераза может восстанавливать эти колпачки и необычно активна во многих видах рака. В этом исследовании с беспрецедентной детализацией показано, как человеческая теломераза захватывает и поэтапно удлиняет теломеры, давая подсказки о том, как однажды мы могли бы точно регулировать этот фермент при возрастных нарушениях и раке.
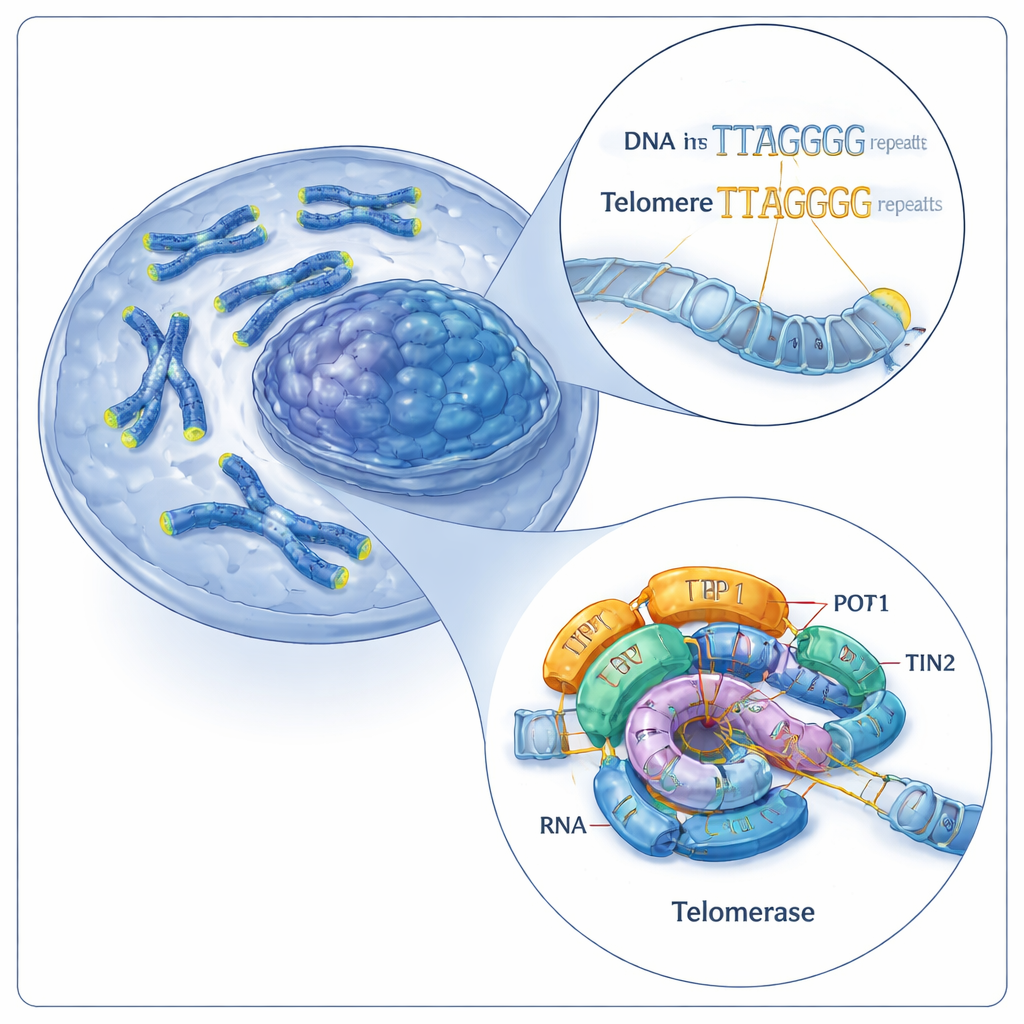
Команда ремонта хромосомных колпачков в клетке
Теломеры состоят из коротких повторяющихся последовательностей ДНК (у людей это шестибуквенный мотив: TTAGGG). Теломераза удлиняет теломеры, добавляя к концам хромосом дополнительные такие повторы. Она делает это с помощью двух главных частей: белка, называемого обратной транскриптазой теломеразы (TERT), и встроенной молекулы РНК (hTR), выступающей в роли шаблона. Вместе эти компоненты формируют каталитическое ядро, которому помогают вспомогательные белки комплекса shelterin, включая тройку TPP1–POT1–TIN2. Ранее человеческая теломераза была визуализирована лишь в одном рабочем состоянии, поэтому оставался главный вопрос: как этот аппарат многократно добавляет новые повторы, не слетая с ДНК?
Заморозка теломеразы в действии
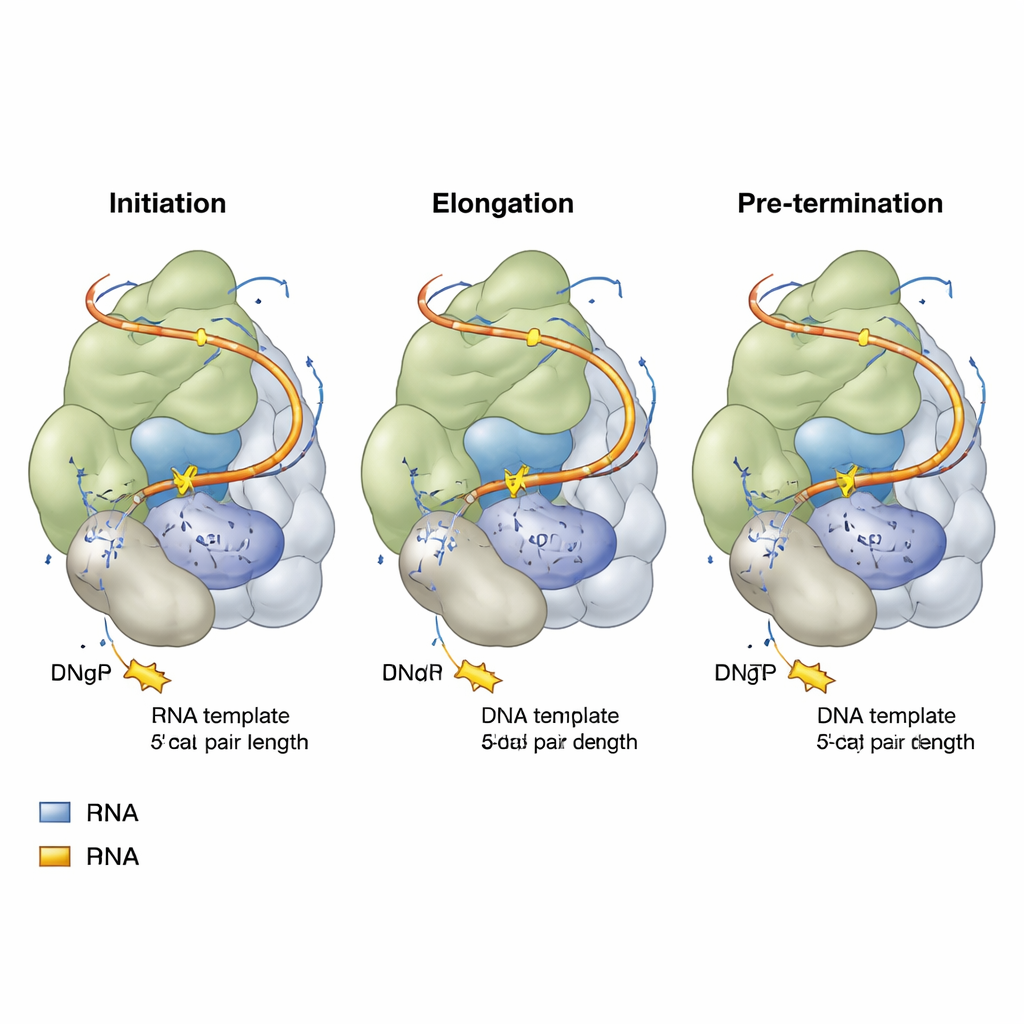
Исследователи воссоздали человеческую теломеразу в клетках человека и затем собрали её с тщательно подобранными кусочками теломерной ДНК и неактивными аналогами нуклеотидов — молекулами, похожими на буквы ДНК, но не способными быть полностью включёнными. С помощью высокоразрешающей криоэлектронной микроскопии они запечатлели снимки теломеразы на трёх ключевых этапах её цикла добавления повторов: на старте (инициация), в середине копирования (удлинение) и незадолго до завершения повтора (предзавершение). Каждый снимок показал каталитическое ядро теломеразы, охватывающее короткий гибрид ДНК–РНК, с входящим нуклеотидом, приготовившимся в активном центре, готовым быть добавленным к растущей цепи ДНК.
Крошечная «молния», контролирующая большой процесс
На всех трёх стадиях выявилась неожиданная закономерность: гибрид ДНК–РНК внутри теломеразы остаётся по сути одинаковой длины — всего четыре пары оснований, временно удлиняясь до пяти, когда входит новый нуклеотид. Конкретная аминокислота в TERT, прозванная «головкой‑молнией», последовательно отмечает конец этого короткого гибрида и предотвращает его дальнейший рост. По мере добавления новых «букв» ДНК одна пара оснований в дальнем конце размыкается, поэтому гибрид никогда не выходит за узкое окно в четыре‑пять пар. Такая компактная конструкция, вероятно, облегчает разделение и смещение цепей, позволяя ферменту сдвигаться и начинать следующий повтор, не теряя полностью захвата ДНК. Тонкие различия в том, какие именно основания ДНК и РНК занимают позиции в этом коротком гибриде, объясняют, почему некоторые оконечные последовательности теломер лучше связываются с теломеразой, чем другие.
Гибкие РНК‑связки и подвижные элементы
РНК‑шаблон в теломеразе не плавает свободно; он прикреплён гибкими участками с обеих сторон, называемыми 5′ и 3′ линкерами шаблона. По мере продвижения теломеразы от инициации к предзавершению верхний (5′) линкер натягивается как банджи‑шнур, в конце концов достигая полностью растянутого состояния, которое помогает сигнализировать о завершении повтора. Между тем нижний (3′) линкер выпячивается наружу и приближается к другой РНК‑структуре (стебель‑петля P6.1) и соседним областям белков. Если эти линкеры становятся слишком короткими или слишком длинными, или если P6.1 изменён, способность теломеразы добавлять повтор за повтором резко падает. Важно, что определённые белковые области — домен TEN и специфическая для теломеразы вставка, названная клином TRAP — действуют как регулируемые направляющие, контактируя и с ДНК, и с этими РНК‑линкерами. Мутации, уменьшающие объём клина TRAP, могут фактически повышать процессивность фермента, что указывает на то, что этот клин обычно служит контролируемым препятствием, которое задаёт темп движения шаблона.
Новые сведения о терапевтической мишени
Комбинируя структурные снимки с функциональными тестами целевых мутаций, исследование предлагает детальную механическую модель того, как человеческая теломераза многократно удлиняет теломеры. Фермент удерживает очень короткий гибрид ДНК–РНК, использует «молниеподобный» остаток для принудительного ограничения этой длины и опирается на гибкие РНК‑линкеры и подвижные белковые элементы для продвижения шаблона и удержания ДНК в процессе нескольких циклов копирования. Для неспециалистов ключевая мысль такова: теломераза работает не как статический копировальный аппарат, а как тонко настроенное, упруго‑натянутое устройство, чья геометрия и подвижные части определяют, как долго и насколько эффективно она поддерживает теломеры. Понимание этой хореографии открывает путь к препаратам, которые могли бы либо ослаблять теломеразу в раке, либо стабилизировать её функцию при заболеваниях преждевременного старения.
Цитирование: Balch, S., Franco-Echevarría, E., Ghanim, G.E. et al. Structures of nucleotide-bound human telomerase at several steps of its telomeric DNA repeat addition cycle. Nat Commun 17, 1847 (2026). https://doi.org/10.1038/s41467-026-68560-8
Ключевые слова: теломераза, теломеры, крио-ЭМ, стабильность генома, онкология