Clear Sky Science · ru
Метилирование ДНК и lncRNA контролируют асинхронную репликацию ДНК в отдельных импринтированных доменах генов
Почему важен график копирования ДНК в клетке
Каждый раз при делении клетке приходится копировать всю свою ДНК, но не все участки дублируются в один и тот же момент. Одни фрагменты копируются рано, другие поздно, следуя точному «расписанию» для генома. В этой работе исследуют, почему в нескольких особых кластерах генов, которые «помнят», от какого родителя они унаследованы, материнская и отцовская копии реплицируются в разное время. Понимание этой необычной кинетики проясняет, как химические метки на ДНК и длинные некодирующие РНК (lncRNA) помогают организовать геном и могут влиять на развитие и болезни.
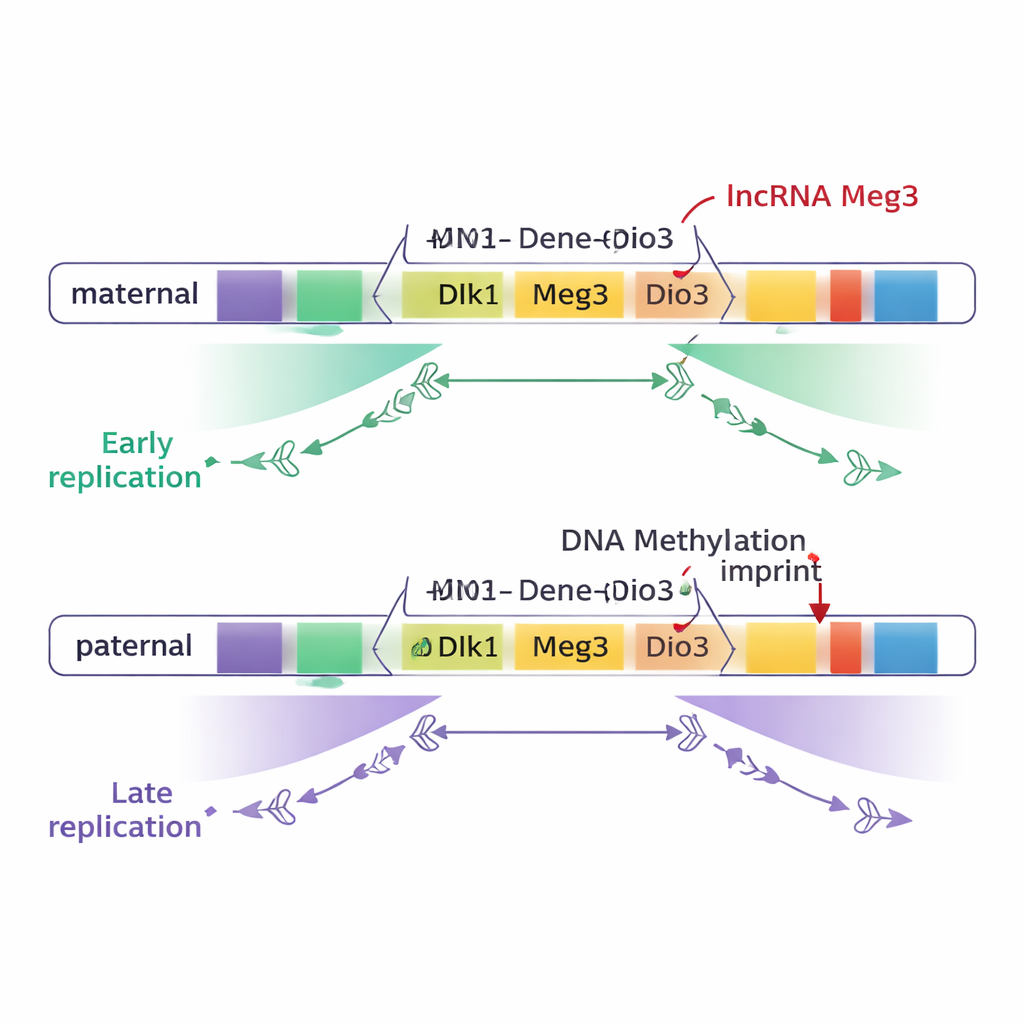
Родительские «воспоминания», записанные на ДНК
У млекопитающих небольшое число «импринтированных» доменов генов ведут себя по-разному в зависимости от того, от матери или отца они происходят. Этот эффект происхождения по родителю контролируется метилированием ДНК — крошечными химическими метками, добавляемыми в определённые участки, известные как дифференциально метилируемые регионы (DMR), — а также изменениями в укладке хромосом. Авторы изучали эмбриональные стволовые клетки мыши, которые напоминают очень ранние эмбриональные клетки. Они сравнивали клетки, содержащие только материнский геном, только отцовский, и обычные гибриды с обоими. Отслеживая, в какие моменты клеточного цикла копировались фрагменты ДНК, они картировали время репликации в масштабах всего генома и подробно исследовали известные импринтированные регионы.
Два импринтированных региона нарушают правила
Большая часть генома, включая большинство импринтированных доменов, реплицировалась одновременно на материнских и отцовских хромосомах. Однако два крупных импринтированных региона выделялись: домен Dlk1–Dio3 на хромосоме 12 и регион Snrpn на хромосоме 7. В этих зонах широкие участки ДНК — примерно три четверти миллиона нуклеотидов в Dlk1–Dio3 — копировались рано на одной родительской хромосоме и поздно на другой. Важно, что эта разница следовала за родительским происхождением, а не за фоновой линией: материнская копия ключевых генов, таких как Dlk1 и ген lncRNA Meg3, постоянно реплицировалась рано, тогда как отцовские копии — поздно.
Метилирование ДНК задаёт переключатель времени
Чтобы проверить причину этой разницы во времени, исследователи модифицировали стволовые клетки так, чтобы нормальная схема метилирования в DMR либо стиралась, либо навязывалась обеим родительским хромосомам. Когда обе родительские копии DMR в области Dlk1–Dio3 были метилированы, весь регион реплицировался поздно на обеих хромосомах. Когда метилирование было в значительной степени удалено с обеих копий, тот же регион реплицировался рано на обеих. Аналогичные эксперименты в Snrpn также приводили к исчезновению различий во времени. Эти результаты показывают, что специфичное для родителя метилирование ДНК необходимо для создания контраста «рано против поздно» между материнскими и отцовскими хромосомами, по крайней мере в этих двух доменах.
Длинная РНК тонко настраивает раннюю репликацию
Однако метилирование ДНК само по себе не было всей историей. В области Dlk1–Dio3 также синтезируется длинная некодирующая РНК Meg3 в составе большого РНК «полицитрона». На материнской хромосоме неметилированные DMR позволяют Meg3 экспрессироваться; на отцовской метилирование подавляет её. Создав точечные делеции, которые выключали Meg3 при сохранённом метилировании ДНК, авторы показали, что потеря Meg3 приводила к тому, что отдельные участки материнского домена сдвигались с ранней репликации на более позднюю. Иными словами, РНК Meg3 способствует раннему копированию соседних участков материнской хромосомы, добавляя второй уровень контроля поверх метилирования ДНК.
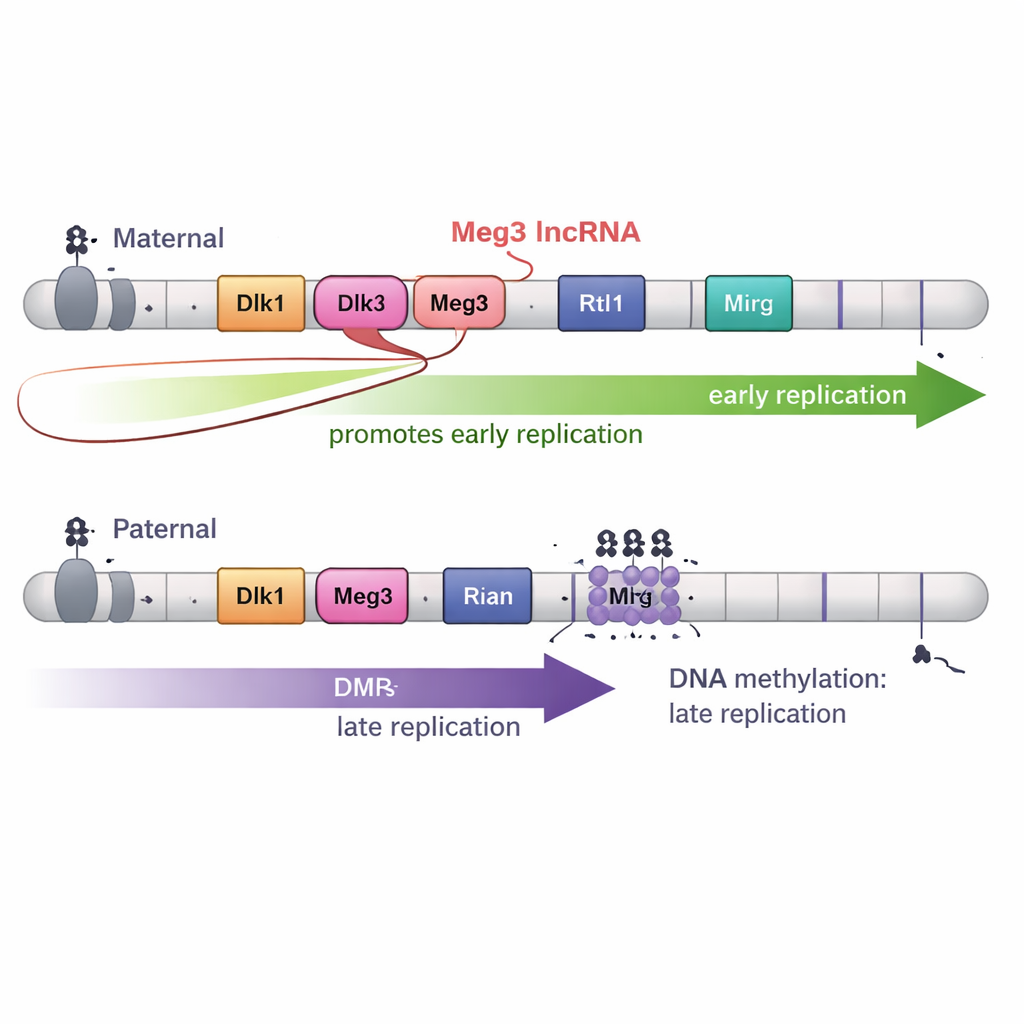
3D‑укладка и развитие вносят дополнительные нюансы
Поскольку укладка генома в трёхмерном пространстве часто связана со временем репликации, команда также подробно картировала 3D‑архитектуру хромосом. Удивительно, но в регионе Dlk1–Dio3 границы 3D‑доменов не совпадали с границами ранней и поздней репликации. Даже при изменении схем метилирования и времени репликации базовые единицы укладки — топологически ассоциирующиеся домены — изменялись иначе. Наконец, при дифференцировке стволовых клеток в нейрональные прогениторы выраженные различия во времени между материнскими и отцовскими копиями в основном исчезали, хотя метки импринтинга и многие аспекты 3D‑структуры сохранялись. Это указывает на то, что сигналы развития могут преодолевать особый паттерн «рано‑против‑поздно», наблюдаемый в стволовых клетках.
Что это значит простыми словами
Исследование показывает, что в нескольких особых полях генов, сохраняющих родительскую «память», расписание копирования ДНК контролируется сочетанием химических меток на ДНК и длинных некодирующих РНК. Метилирование ДНК в контрольных импринтированных регионах задаёт базовый ранний‑или‑поздний режим для каждой родительской хромосомы, а lncRNA Meg3 дополнительно подталкивает соседние материнские участки к более раннему копированию. Эти эффекты действуют в значительной степени независимо от трёхмерной укладки хромосомы. В ходе развития, по мере специализации клеток, эта необычная синхронизация угасает, что показывает: она характерна для состояния плюрипотентных стволовых клеток. В сумме работа объясняет, как родительские эпигенетические «воспоминания» и некодирующие РНК могут локально переопределять обычное расписание репликации генома.
Цитирование: Imaizumi, Y., Charon, F., Surcis, C. et al. DNA methylation and lncRNA control asynchronous DNA replication at specific imprinted gene domains. Nat Commun 17, 1844 (2026). https://doi.org/10.1038/s41467-026-68558-2
Ключевые слова: геномный импринтинг, метилирование ДНК, временные рамки репликации, длинные некодирующие РНК, эмбриональные стволовые клетки