Clear Sky Science · ru
Микробная активация GLP-2R смягчает воспаление желудочно-кишечного тракта
Почему важен «дружественный» белок для кишечника
Пока мир ищет устойчивые способы прокормить растущее население, учёные обращают внимание не только на поля и фермы, но и на огромные стальные ёмкости, где выращивают микробы для питания. В этом исследовании изучали, может ли один из таких микробных белков давать не только питание. Авторы задали вопрос: может ли белок, полученный из безвредных бактерий, одновременно удовлетворять диетические потребности и активно защищать кишечник от воспаления — ключевой проблемы при таких состояниях, как воспалительные заболевания кишечника и повреждения, вызванные химиотерапией?
Новый тип белка из микробов
Белок, в центре внимания этой работы, получен из почвенной бактерии Methylococcus capsulatus Bath (McB). Его не употребляли как живые бактерии: McB обрабатывали до микробного лизата — порошкообразной смеси разрушенных бактериальных клеток — коммерчески выпускаемой под названием FeedKind®. Мышей кормили диетами, в которых этот лизат обеспечивал большую часть белка, либо в простой, либо в более «человеко-подобной» сложной диете. Затем команда отслеживала, как такая диета меняет состав кишечных микробов, иммунные клетки, патрулирующие кишечник, и насколько хорошо кишечник сопротивляется разным видам повреждений.
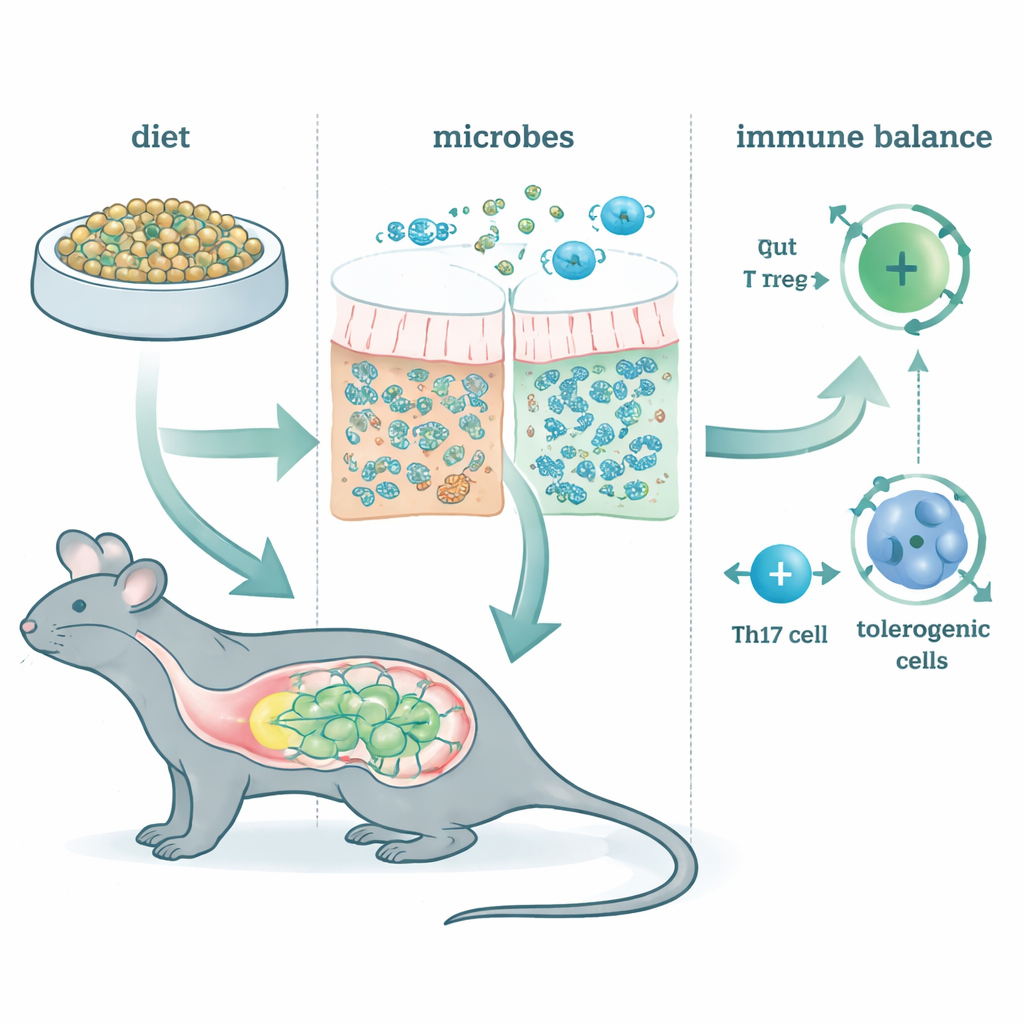
Перестройка микробного окружения
Питание McB быстро и устойчиво изменяло микробиоту кишечника, независимо от фоновой диеты животных. Сам McB почти не обнаруживался в фекалиях — материал почти полностью использовался в кишечнике. Взамен расцвели несколько родов бактерий из таких семейств, как Lachnospiraceae и Bacteroidaceae. Генетический анализ показал обогащение сообществ путями ферментации, производящими короткоцепочечные жирные кислоты — небольшие молекулы, уже известные тем, что питают клетки кишечника и влияют на иммунитет. Иными словами, McB вёл себя скорее как целенаправленное топливо, перенастраивающее функции местных микробов, чем как обычный источник белка.
Обучение иммунной системы толерантности
Авторы затем изучили ключевые типы T‑клеток, которые решают, будет ли кишечник реагировать спокойно или агрессивно на попадающее в него содержимое. Одна группа — переферически индуцированные регуляторные T‑клетки (pTregs) — помогает предотвратить чрезмерную реакцию на пищу и дружелюбные микробы. Другая группа, Th17‑клетки, в зависимости от «настроения» могут либо провоцировать повреждающее воспаление, либо поддерживать здоровый барьер. Питание McB сильно увеличивало число pTregs по всему кишечнику, даже когда большинство микробов было уничтожено антибиотиками. В то же время влияние McB на Th17 зависело от наличия и нормальной работы кишечной микробиоты. У микробиологически неповреждённых мышей McB сдвигал Th17 в более успокаивающее состояние — с выработкой IL‑10 и меньшей воспалительностью. Когда ферментация блокировалась, этот толерогенный сдвиг исчезал, что подчёркивает: часть эффекта McB достигается путём перенаправления диалога между микробами и иммунитетом.
Защита кишечника при повреждении
Чтобы выяснить, превращаются ли эти изменения в реальную защиту, исследователи подвергли мышей двум тяжёлым повреждениям кишечника. Одно — химиотерапевтический препарат 5‑фторурацил, вызывающий широкое разрушение и укорочение ворсинок, всасывающих питательные вещества. Другое — химическое вещество DSS, индуцирующее колит, модель воспаления толстой кишки. Мыши на диете McB теряли меньше веса, сохраняли более длинные ворсинки и длину толстой кишки, имели меньше кровоточащих поражений и более низкие микроскопические баллы поражения в обеих моделях. Эти преимущества сохранялись даже при экспериментальном удалении CD4 T‑клеток, что указывает на то, что защитные действия McB не сводятся лишь к адаптивным иммунным клеткам, но также включают прямое влияние на кишечную оболочку.
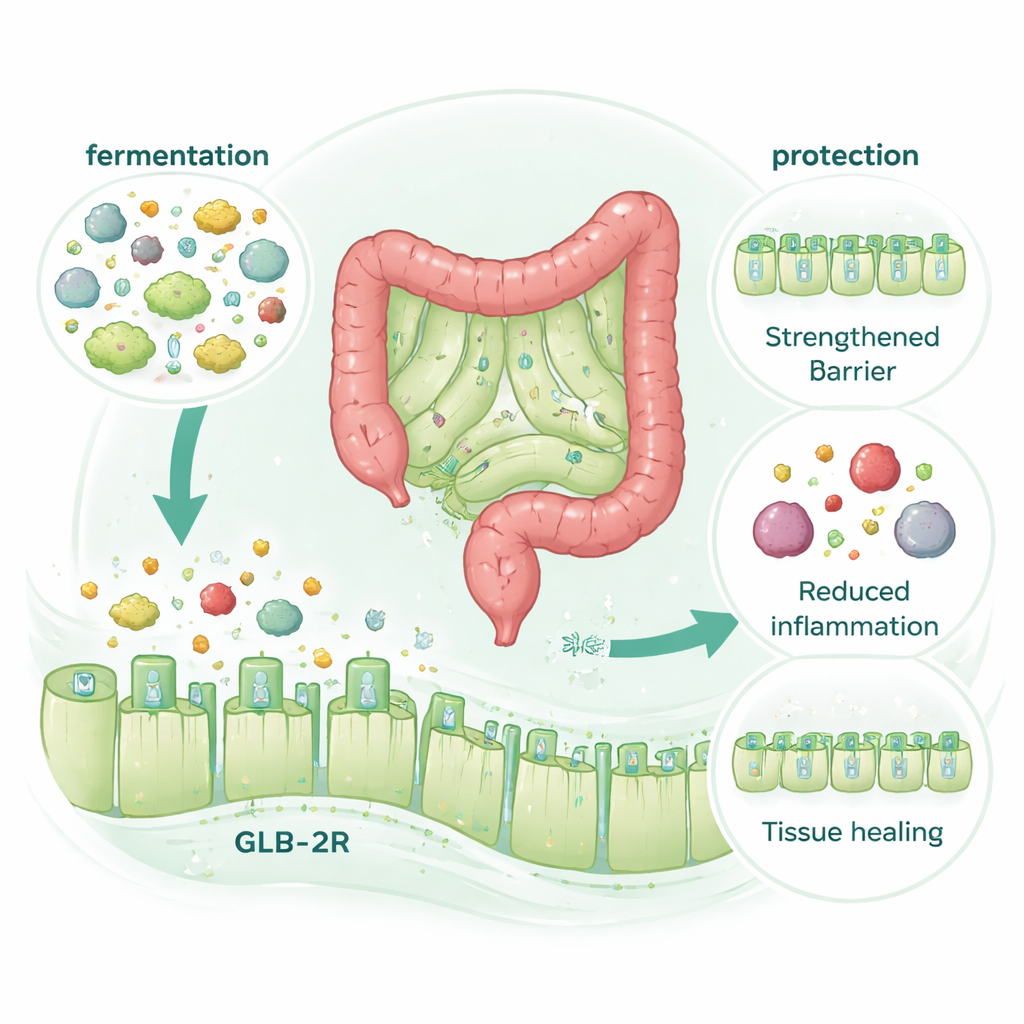
Рецептор гормона, но без дополнительного гормона
Неожиданным оказалось открытие, что защитный эффект McB абсолютно требовал наличия в кишечнике рецептора для гормона, способствующего восстановлению, называемого GLP‑2 (рецептор GLP‑2, GLP‑2R), но не связанных с ним рецепторов GLP‑1. У мышей без GLP‑2R McB переставал защищать от повреждений от химиотерапии или колита. При этом сам McB не повышал уровень GLP‑2 в крови, даже когда переваривание и распад гормона тщательно контролировали. Вместо этого преимущества исчезали при химическом блокировании ферментации в толстой кишке, хотя общий состав микробиоты менялся мало. Это указывает на механизм, при котором микробный распад McB порождает мелкие соединения, действующие как «мимики» GLP‑2, активирующие его рецептор для укрепления барьера и содействия восстановлению без дополнительного высвобождения гормона.
Что это может значить для будущих продуктов питания
Для непрофессионального читателя ключевая мысль такова: некоторые будущие источники белка могут быть спроектированы не только как климатически устойчивые, но и как активные помощники для здоровья кишечника. У мышей коммерчески масштабируемый лизат McB одновременно перенастраивал иммунитет в сторону толерантности и помогал кишечнику противостоять тяжёлым повреждениям двумя частично независимыми путями: прямым усилением регуляторных T‑клеток и ферментационно‑опосредованной активацией рецептора GLP‑2, способствующей восстановлению тканей. Хотя потребуются исследования на людях, работа указывает, что белки микробного происхождения могут стать новым классом «умной» пищи — способной кормить нас, сотрудничать с нашими собственными микробами и ненавязчиво укреплять естественные барьеры кишечника против воспаления.
Цитирование: Yang-Jensen, S.K., Choi, B.SY., Nägele, N.S. et al. Microbial activation of the GLP-2R mitigates gastrointestinal inflammation. Nat Commun 17, 1839 (2026). https://doi.org/10.1038/s41467-026-68551-9
Ключевые слова: воспаление кишечника, микробный белок, микробиом, рецептор GLP-2, регуляторные Т-клетки