Clear Sky Science · ru
Эндотелиальный FUNDC1 регулирует метаболическое перепрограммирование и переход от ожирения к диабету через ось SIRT3/GATA2/эндотелин-1
Почему клетки сосудистой стенки важны при ожирении и диабете
Ожирение и сахарный диабет 2 типа часто списывают на жировую ткань, печень или поджелудочную железу. Но это исследование выявляет неожиданного виновника: тонкий слой клеток, выстилающий кровеносные сосуды — эндотелиальные клетки. Авторы показывают, что небольшой митохондриальный белок в этих клетках, называемый FUNDC1, может способствовать переходу организма от простого набора веса к полноценному диабету, меняя способ, которым сосуды «договариваются» с метаболическими органами.
Стресс внутренней «кожи» организма
Эндотелиальные клетки формируют обширную и тонкую сеть, которая контролирует кровоток, доставку питательных веществ и сигналы к соседним тканям. В здоровом состоянии они балансируют расслабляющие факторы, такие как оксид азота, и сжимающие, например эндотелин-1 (ET-1). При ожирении и раннем диабете этот баланс смещается в сторону ET-1, который не только сужает сосуды, но и нарушает то, как жировые, мышечные и печёночные клетки обрабатывают сахар и жиры. Авторы начали с того, что показали на мышах: дисфункция сосудов появляется уже после двух месяцев на высокожировой диете, до выраженной инсулинорезистентности, что указывает на то, что повреждённый эндотелий может запускать метаболическое заболевание, а не просто реагировать на него.
Митохондриальный переключатель, формирующий жировую массу
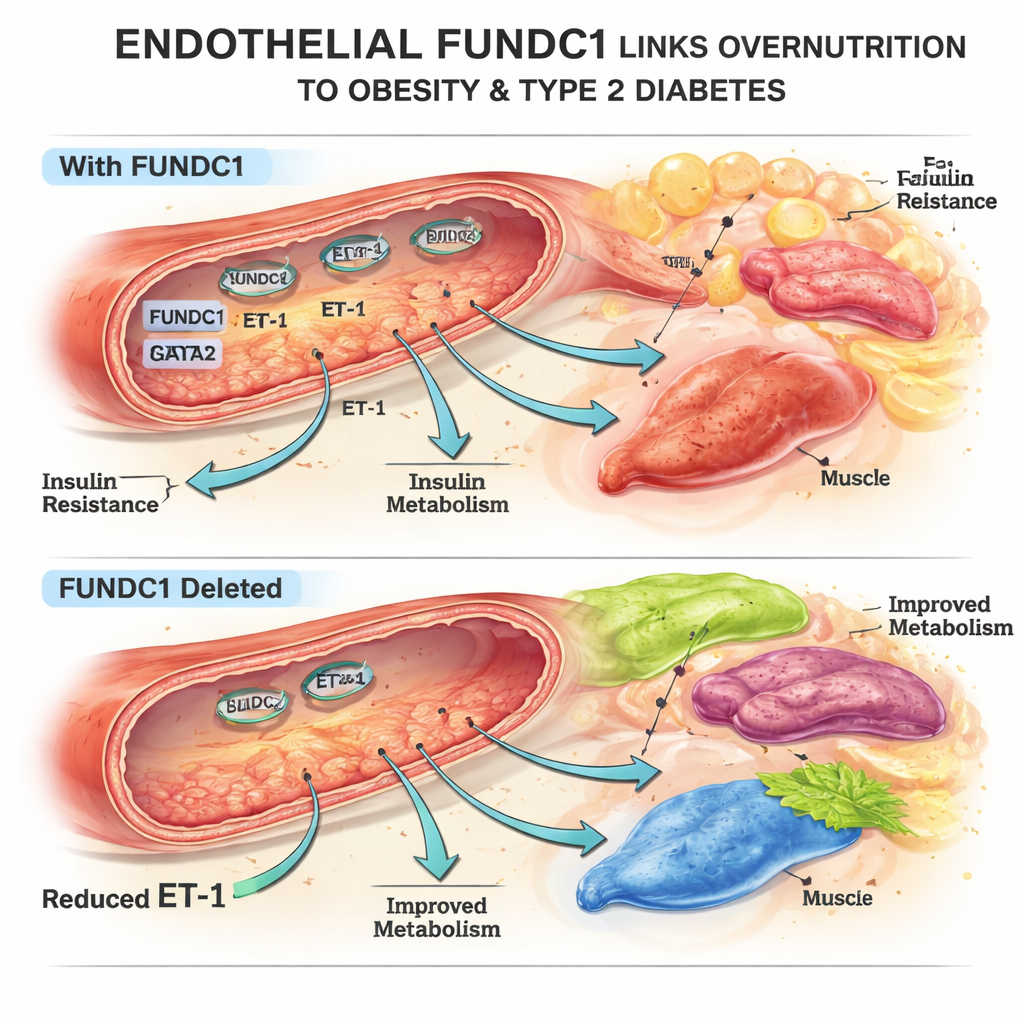
Команда сосредоточилась на FUNDC1 — белке на поверхности митохондрий, энергетических «фабрик» клетки. В эндотелиальных клетках мышей и человека, подвергнутых избытку жира, уровни FUNDC1 изменялись со временем: сначала падали, затем при длительном переедании резко повышались. На генетически модифицированных мышах, у которых FUNDC1 отсутствовал только в эндотелии, исследователи обнаружили, что эти животные в определённой степени были защищены от набора веса на высокожировой диете: у них было меньше жировой массы, крупность адипоцитов была меньше, и контроль уровня глюкозы был лучше. Их жировая ткань, печень и бурый жир сильнее реагировали на инсулин, несмотря на то что уровень инсулина сам по себе не повышался. Эти изменения нельзя было объяснить разницей в потреблении пищи или активности, что указывает на влияние сосудистой системы на метаболизм.
Химический посредник, ведущий к инсулинорезистентности
Чтобы выяснить, как эндотелиальный FUNDC1 влияет на отдалённые органы, авторы просcreenировали несколько веществ, секретируемых эндотелием. Выделялся один — ET-1. При удалении FUNDC1 в эндотелиальных клетках продукция ET-1 в сосудах и в крови значительно падала как в нормальных, так и в условиях высокожировой диеты. Эксперименты на культивируемых адипоцитах, гепатоцитах и мышечных клетках показали, что ET-1 стимулирует пролиферацию предшественников жировых клеток, изменяет запасание и расщепление жиров и усиливает накопление липидов в печени и мышцах при воздействии высокого жира — паттерн, известный как способствующий инсулинорезистентности. В живых мышах инфузия ET-1 в начале высокожировой диеты устраняла защитный эффект удаления эндотелиального FUNDC1: масса тела, жировая масса, контроль глюкозы и функция сосудов ухудшались, что подчёркивает роль ET-1 как ключевого звена между эндотелием и метаболическим заболеванием.
Внутреняя сигнальная ось: FUNDC1, SIRT3 и GATA2
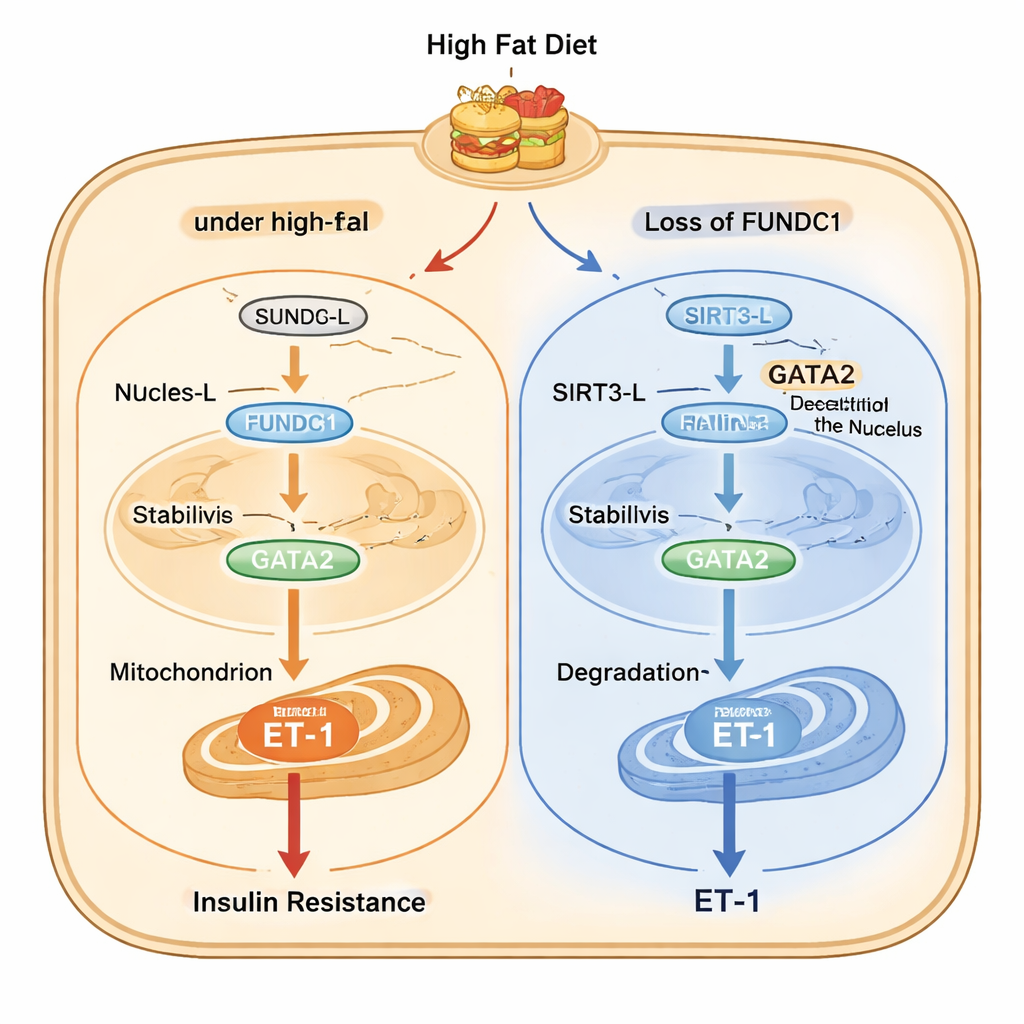
Далее исследование описывает подробную молекулярную цепочку внутри эндотелиальных клеток. При высокожировом стрессе длинная форма фермента SIRT3 (SIRT3-L), которая может находиться как в ядре, так и в митохондриях, с помощью FUNDC1 и шаперона HSC70 перемещается из ядра в митохондрии. Оказавшись в митохондриях, SIRT3-L в меньшей степени доступен в ядре для удаления ацетильных групп с GATA2 — фактора транскрипции, усиливающего активность гена ET-1. Более ацетилированный GATA2 более стабилен и стимулирует повышенную продукцию ET-1. Когда FUNDC1 отсутствует, SIRT3-L остаётся в ядре, где деацетилирует GATA2, что ведёт к распаду GATA2 и снижению продукции ET-1. Интригующе, SIRT3 в свою очередь способствует деградации FUNDC1, создавая петлю обратной связи, которая обычно сдерживает путь, но нарушается при хроническом переедании.
От модельных мышей к человеческому заболеванию
Чтобы проверить, релевантен ли этот механизм у людей, авторы изучали кровь и мелкие артерии у людей с ожирением и сахарным диабетом 2 типа и у здоровых добровольцев. У пациентов с обоими состояниями наблюдались повышенные уровни ET-1 в крови и повышенная экспрессия FUNDC1, GATA2 и гена ET-1 в эндотелии сосудов. Количество ET-1 в крови тесно коррелировало с индексом массы тела и показателем долгосрочного уровня глюкозы (HbA1c), а уровни гена ET-1 в сосудах сильно коррелировали с FUNDC1 и GATA2. Эти закономерности отражают результаты на мышах и поддерживают идею о том, что сверхактивная ось FUNDC1–SIRT3–GATA2–ET-1 действует в человеческой сосудистой ткани при метаболическом стрессе.
Новая мишень в борьбе с диабетом
Для неспециалистов основной вывод таков: ущерб от переедания может первично проявляться в клетках, выстилающих кровеносные сосуды. Там митохондриальный белок FUNDC1 перенаправляет регуляторный фермент SIRT3 из ядра, позволяя фактору GATA2 усилить производство ET-1 — мощного гормоноподобного сигнала, способствующего как ригидности сосудов, так и инсулинорезистентности. Блокирование этого пути — путем уменьшения активности эндотелиального FUNDC1 или снижения уровня ET-1 — может помочь предотвратить переход от ожирения к диабету и одновременно защитить сосуды.
Цитирование: Li, J., Li, D., Zhao, F. et al. Endothelial FUNDC1 regulates metabolic reprogramming and the obesity-diabetes transition through the SIRT3/GATA2/endothelin-1 axis. Nat Commun 17, 1836 (2026). https://doi.org/10.1038/s41467-026-68548-4
Ключевые слова: эндотелиальные клетки, митохондрии, эндотелин-1, ожирение, сахарный диабет 2 типа