Clear Sky Science · ru
Взаимодействие петли3 склеростина с LRP4 в адипоцитах необходимо склеростину для нарушения липидного и глюкозного обмена в организме
Почему кости важны для уровня сахара в крови
Большинство людей воспринимают кости как неживой каркас, но клетки кости тихо выделяют гормоны, которые связываются с остальными тканями тела. В этом исследовании показано, как один из таких костных белков — склеростин — связывает две очень распространённые проблемы у пожилых женщин: хрупкие кости (остеопороз) и сахарный диабет 2‑го типа. Раскрыв специфическое «пожатие руки» между склеростином и жировыми клетками, учёные описывают путь для укрепления костей и улучшения контроля сахара и холестерина без дополнительной нагрузки на сердце.
Костный сигнал, который идёт не так
Склеростин — белок, в основном синтезируемый клетками кости. В норме он замедляет образование кости и, что несколько неожиданно, частично защищает сосуды. Команда сосредоточилась на небольшом фрагменте этого белка, называемом петлёй3, и изучила, играет ли он роль в нарушениях обращения жиров и сахара. Они обнаружили, что у женщин с постменопаузальным остеопорозом и сопутствующим диабетом 2‑го типа, а также у недавно диагностированных пациентов уровень склеростина в крови был выше, чем у сопоставимых лиц без диабета. У мышей, кормлёных высокожировой диетой для моделирования метаболического стресса, уровень склеростина также повышался вместе с набором веса, увеличением кровяных жиров и ухудшением контроля гликемии. Эти закономерности указывают на то, что избыток склеростина может быть не просто попутным явлением при нарушениях обмена.
Разбор крошечной петли с большими эффектами
Чтобы понять роль петли3, исследователи модифицировали мышей так, чтобы склеростин был изменён или чтобы из него была удалена петля3. Мыши, перепроизводившие нормальный склеростин, накапливали больше жира в белой жировой ткани, имели более крупные адипоциты, повышенные уровни циркулирующих жирных кислот и худшую толерантность к глюкозе и инсулиновый ответ по сравнению с нормальными мышами. Когда петля3 была генетически удалена или точечно изменена, эти проблемы ослабевали: жировые депо уменьшались, адипоциты сокращались, уровни кровяных липидов снижались, а обмен глюкозы улучшался. Примечательно, что похожие преимущества наблюдались при лечении мышей специально разработанным ДНК‑подобным препаратом (аптамером), который захватывает петлю3 и блокирует её функцию, не изменяя при этом общего уровня склеростина в крови.
Как жировые клетки «слышат» костный сигнал
Далее группа подробно изучила адипоциты, чтобы понять, как петля3 передаёт вредный сигнал. Они сосредоточились на рецепторном белке на поверхности адипоцитов — LRP4, ранее известном своей ролью в работе склеростина на кости. В клеточных культурах показали, что петля3 физически связывается с конкретной частью LRP4 на жировых клетках. Этот контакт вызывал изменения, которые увеличивали способность клеток синтезировать и расщеплять жиры и захватывать больше глюкозы из крови, что приводило к увеличенным, сверхактивным адипоцитам. Когда учёные тонко меняли ключевые структуры в LRP4 так, чтобы петля3 больше не могла пристать, или добавляли небольшой блокирующий пептид, имитирующий сайт стыковки LRP4, влияние склеростина на накопление жира и поглощение сахара значительно уменьшалось. Как в клетках, так и у мышей блокирование взаимодействия петля3–LRP4 восстанавливало более нормальный размер адипоцитов и улучшало толерантность к глюкозе.
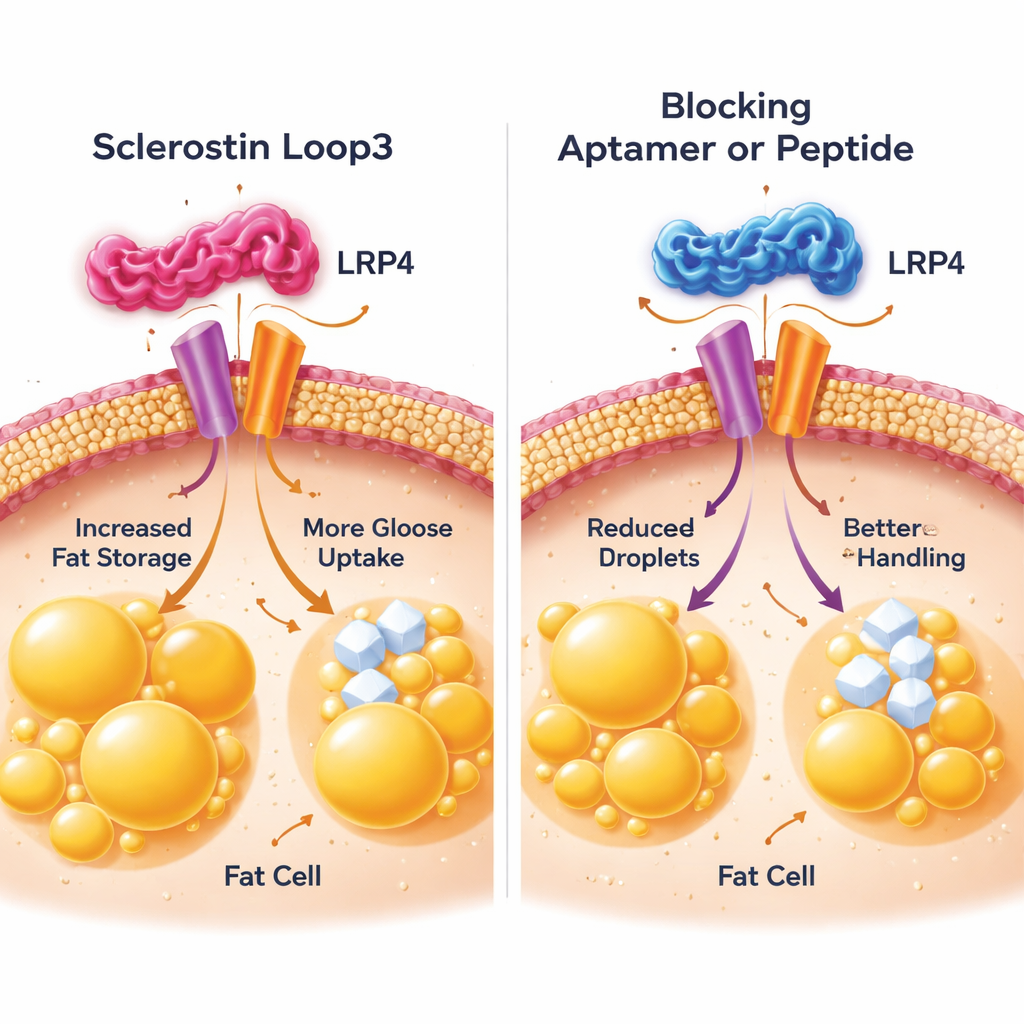
Крепче кости, здоровее обмен веществ
Важная проблема существующих препаратов, блокирующих склеростин при остеопорозе, заключается в том, что хотя они укрепляют кость и улучшают метаболизм, регуляторы обеспокоены повышенным риском серьёзных сердечно‑сосудистых событий. Ранее эта группа показала, что петля3 критична для торможения образования кости склеростином, но не для его защитных эффектов на сердце. Здесь они дополнительно демонстрируют, что нацеливание на петлю3 — либо генетическими изменениями, либо препаратами, ориентированными на петлю3 — улучшает липидный и глюкозный обмен в организме в нескольких моделях мышей, одновременно увеличивая массу и прочность кости. В отличие от существующих лекарств, эта стратегия не вызывала компенсаторного повышения другого костно‑связанного ингибитора DKK1, которое может ослаблять длительные преимущества.
Что это может значить для пациентов
Проще говоря, в исследовании утверждается, что очень маленькая часть одного костного гормона способствует как ухудшению здоровья костей, так и метаболическим нарушениям, напрямую общаясь с жировыми клетками. Прерывая «разговор» между сегментом петли3 склеростина и рецептором LRP4 на адипоцитах, возможно создать терапии, которые укрепляют кости и нормализуют кровяные жиры и уровень сахара, сохраняя при этом сердечно‑защитные функции склеростина. Для постменопаузальных женщин, часто сталкивающихся одновременно с остеопорозом и диабетом 2‑го типа, такие препараты, нацеленные на петлю3, в будущем могут предложить более безопасный и долгосрочный способ одновременно контролировать оба состояния.
Цитирование: Jiang, H., Tao, X., Yu, S. et al. Adipocytic sclerostin loop3-LRP4 interaction required by sclerostin to impair whole-body lipid and glucose metabolism. Nat Commun 17, 1812 (2026). https://doi.org/10.1038/s41467-026-68526-w
Ключевые слова: склеростин, петля3, LRP4, остеопороз, сахарный диабет 2 типа