Clear Sky Science · ru
Пальмитиновая кислота инициирует палмитоилацию B7H3 и способствует уклонению от иммунитета
Почему это исследование важно для онкологических пациентов
Большинство людей слышали, что новые препараты для иммунотерапии могут помочь иммунной системе бороться с раком, но многие пациенты с распространённым раком толстой (кишечника) получают мало пользы. В этом исследовании выявлён скрытый биохимический приём, который используют колоректальные опухоли, чтобы защититься от иммунной атаки, и предложен новый тип лекарства — короткий пептид — который может сделать иммунотерапию эффективнее для таких пациентов.
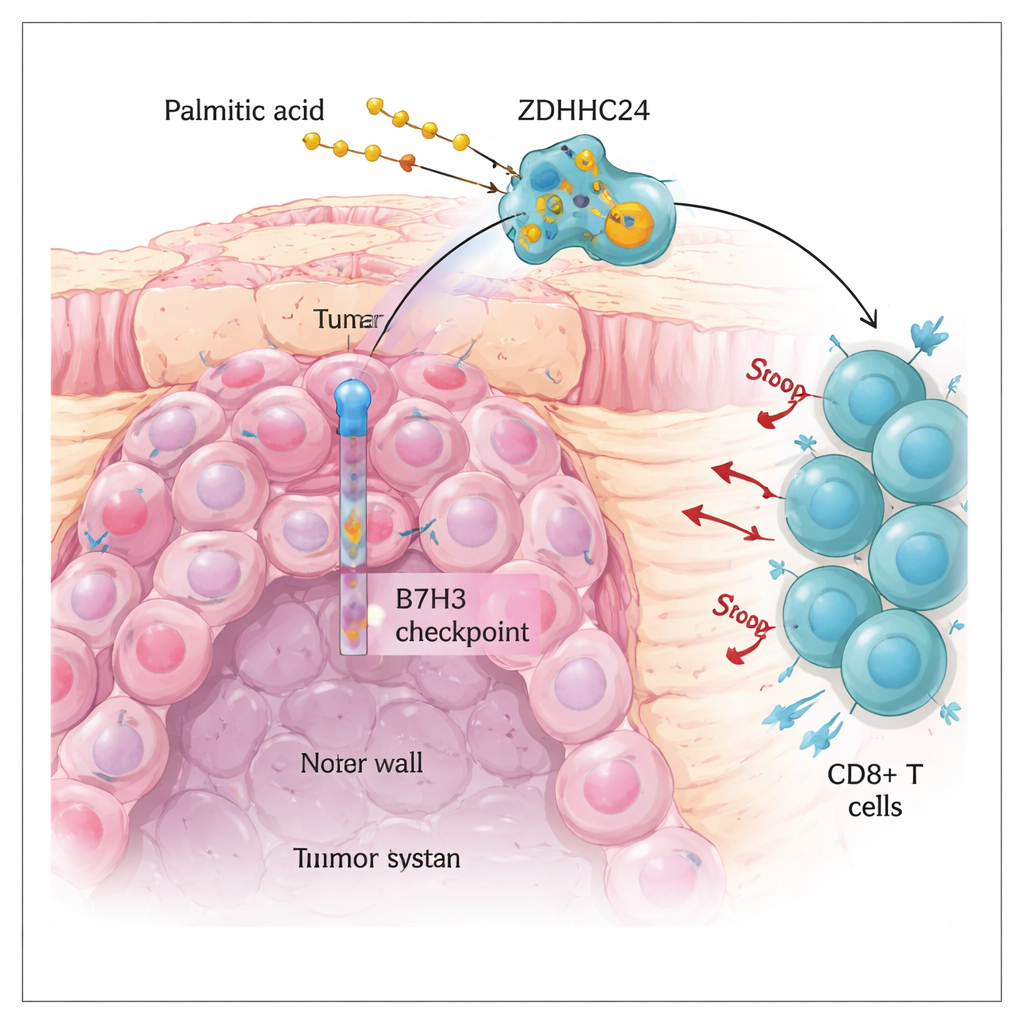
Препятствие в текущей иммунотерапии рака кишечника
Рак толстой кишки — одно из наиболее распространённых онкологических заболеваний в мире. Препараты иммунотерапии, снимающие «тормоза» иммунитета, такие как ингибиторы PD-1 и PD-L1, кардинально изменили ведение болезни у части пациентов, чьи опухоли имеют множество ошибок в ДНК (так называемые MSI-H опухоли). К сожалению, большинство колоректальных опухолей микросателлитно-стабильны (MSS) и плохо реагируют на эти препараты. Авторы сосредоточились на другом «тормозном» молекуле — B7H3, которая располагается на поверхности опухолевых клеток и подавляет активность киллерных иммунных клеток, особенно CD8+ T-клеток. Они обнаружили, что белок B7H3 сильно повышен в MSS-опухолях и связан с худшей выживаемостью, хотя активность самого гена B7H3 не увеличена. Такое несоответствие навело на важный вопрос: что поддерживает высокий уровень белка B7H3 на опухолевых клетках?
Как обычный жир помогает опухолям прятаться
Исследователи заподозрили, что метаболизм опухоли может стабилизировать B7H3. Сравнив активность генов и профили малых молекул в MSS и MSI-H опухолях толстой кишки, они обнаружили различия во многих жировых путях, причём одна жирная кислота — пальмитиновая — выделялась особенно. При обработке клеток колоректального рака несколькими продуктами распада жиров в лаборатории лишь пальмитиновая кислота явно повышала уровень белка B7H3. Дальнейшие эксперименты показали причину: пальмитиновая кислота входит в химическую модификацию, называемую палмитоилированием, при которой цепочка жира присоединяется к определённым участкам белков. Эта модификация, осуществляемая ферментом ZDHHC24 в одной цистеиновой позиции в B7H3, делала белок более стабильным и более многочисленным на поверхности опухолевой клетки.
Блокирование маршрута утилизации «иммунного тормоза»
Клетки обычно удаляют ненужные или повреждённые белки с помощью систем, работающих как переработка и вывоз мусора. Исследователи показали, что B7H3 преимущественно разрушается через путь «самопоедания» — аутофагию, где рецепторный белок SQSTM1/p62 маркирует грузы для уничтожения. Когда B7H3 был палмитоилирован, он слабо связывался с этим рецептором и избегал аутофагического разрушения, что приводило к стойко высокому уровню «иммунного тормоза». Если место палмитоилирования мутировали так, чтобы оно не могло принимать жировой ярлык, или удалили фермент ZDHHC24, B7H3 более эффективно направлялся в клеточные «мусорные пакеты» и разрушался. У мышей опухоли без палмитоилированного B7H3 развивались медленнее, при этом их собственная скорость деления в иммунодефицитных животных не менялась, и наблюдалось значительно больше CD8+ T-клеток и усиленная киллерная активность. Это показало, что модификация в основном действует через подавление иммунитета, а не через изменение скорости деления раковых клеток.
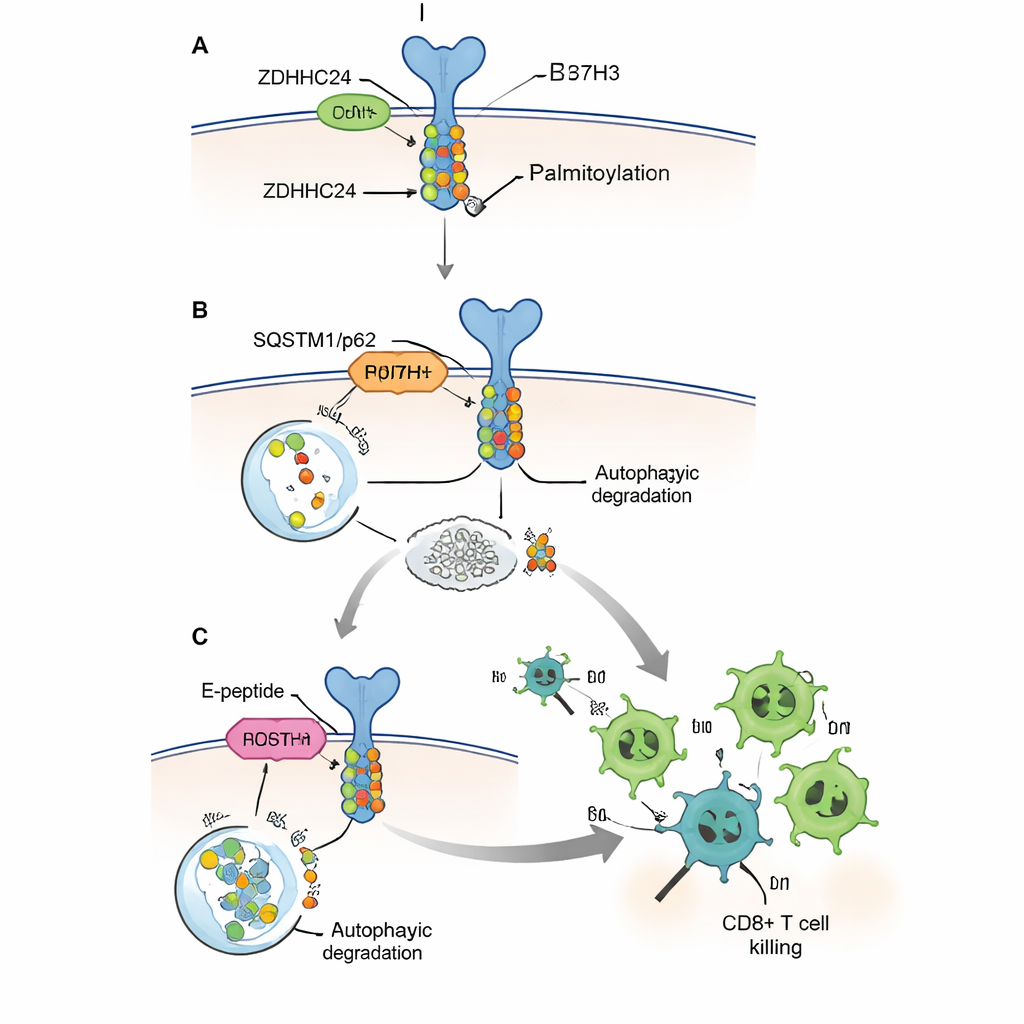
Ослабление щита и усиление T-клеток
Поскольку полное удаление ZDHHC24 или B7H3 с помощью генетики непрактично как терапия у пациентов, авторы разработали короткий проникающий в клетки пептид, который назвали E-пептидом. Он имитирует небольшой фрагмент белка B7H3, который обычно связывается с ZDHHC24, действуя как мишень‑подделка и мешая ферменту модифицировать настоящие молекулы B7H3. В культурах клеток E-пептид снижал палмитоилирование и уровни белка B7H3, восстанавливал его распознавание аутофагической системой и позволял человеческим CD8+ T-клеткам более эффективно убивать опухолевые клетки. В нескольких мышиных моделях, включая гуманизированную модель с человеческими иммунными клетками и человеческими колоректальными опухолями, инъекции E-пептида уменьшали опухоли, увеличивали число CD8+ T-клеток в опухолях и усиливали выработку ключевых киллерных молекул, таких как гранзим В и интерферон‑гамма.
Новый партнёр для существующей иммунотерапии
Наконец, исследователи проверили, можно ли сочетать эту стратегию со стандартной блокадой PD‑1. В мышиных моделях рака толстой кишки и E-пептид в одиночку, и анти‑PD‑1‑антитело в одиночку обеспечивали частичный контроль опухоли. Но при комбинированном применении оба подхода давали гораздо более сильное и длительное подавление опухолей, в некоторых случаях приводя к их исчезновению и более чем удваивая среднюю выживаемость по сравнению с контролем. Это указывает на то, что отключение щита B7H3 путём снятия его жирового «якоря» может дополнять существующие ингибиторы контрольных точек, направленные на путь PD‑1.
Что это значит для будущего лечения рака
Проще говоря, в этом исследовании показано, что обычный пищевой жир — пальмитиновая кислота — может быть захвачен колоректальными опухолями для химического «броневания» иммуноподавляющего белка (B7H3) и помощи опухоли в уклонении. Блокируя это единичное химическое присоединение, авторы сумели снять броню, позволить собственным системам утилизации клетки удалить B7H3 и вновь открыть доступ CD8+ T-клеткам для атаки. Хотя сам E-пептид — экспериментальный инструмент ранней стадии, работа выделяет палмитоилирование B7H3 и его фермент ZDHHC24 как перспективные лекарственные мишени. Если аналогичные агенты окажутся безопасными и эффективными у людей, они однажды могут превратить больше колоректальных опухолей из «холодных», игнорирующих иммунотерапию, в «тёплые», которые иммунная система способна распознавать и уничтожать.
Цитирование: Rao, Z., Huang, C., Wu, Q. et al. Palmitic acid-triggered B7H3 palmitoylation promotes immune escape. Nat Commun 17, 1810 (2026). https://doi.org/10.1038/s41467-026-68525-x
Ключевые слова: иммунотерапия рака толстой кишки, контролирующий белок B7H3, метаболизм пальмитиновой кислоты, палмитоилирование белков, опухолевый иммунитет CD8 T-клеток