Clear Sky Science · ru
Макрофаги прусалки преобразуют физические сигналы раны в быструю проницаемость сосудов
Чему маленькая рыбка учит нас о припухлости ран
Когда вы ссадите колено, участок кожи быстро краснеет, становится опухшим и пропускает жидкость. Это быстрое изменение в соседних кровеносных сосудах важно для борьбы с инфекцией и запуска восстановления, но то, как тело за доли секунды ощущает повреждение и реагирует, трудно было увидеть в реальном времени. Используя прозрачных личинок пестробрюхой рыбки и современные методы живой визуализации, исследование раскрывает, как специализированные иммунные клетки, охватывающие сосуды, превращают физический шок от раны в почти мгновенное протекание сосудов, давая новое понимание воспаления, заживления и даже повреждения легких у человека.
Наблюдая, как травма распространяется по телу
Ученые работали с молодыми рыбками, чьи прозрачные тела позволяли наблюдать клетки и сосуды под микроскопом. Они отрезали кончик хвостового плавника и наполнили кровообращение светящимся красителем, который остается внутри здоровых сосудов. Когда пострадавших рыбок возвращали в обычную пресную воду, внезапный приток воды в ткани создавал вокруг раны «осмотический шок». В течение нескольких минут ближайшие сосуды расширялись и начинали пропускать флуоресцентный краситель в окружающие ткани, имитируя отек и сочивость, которые происходят вокруг ран у человека. Переводя рыб между обычными и специально сбалансированными солевыми или сахарными растворами, команда показала, что это быстрое увеличение проницаемости сосудов сильно зависит от осмотических изменений, а не только от механического разрыва тканей.
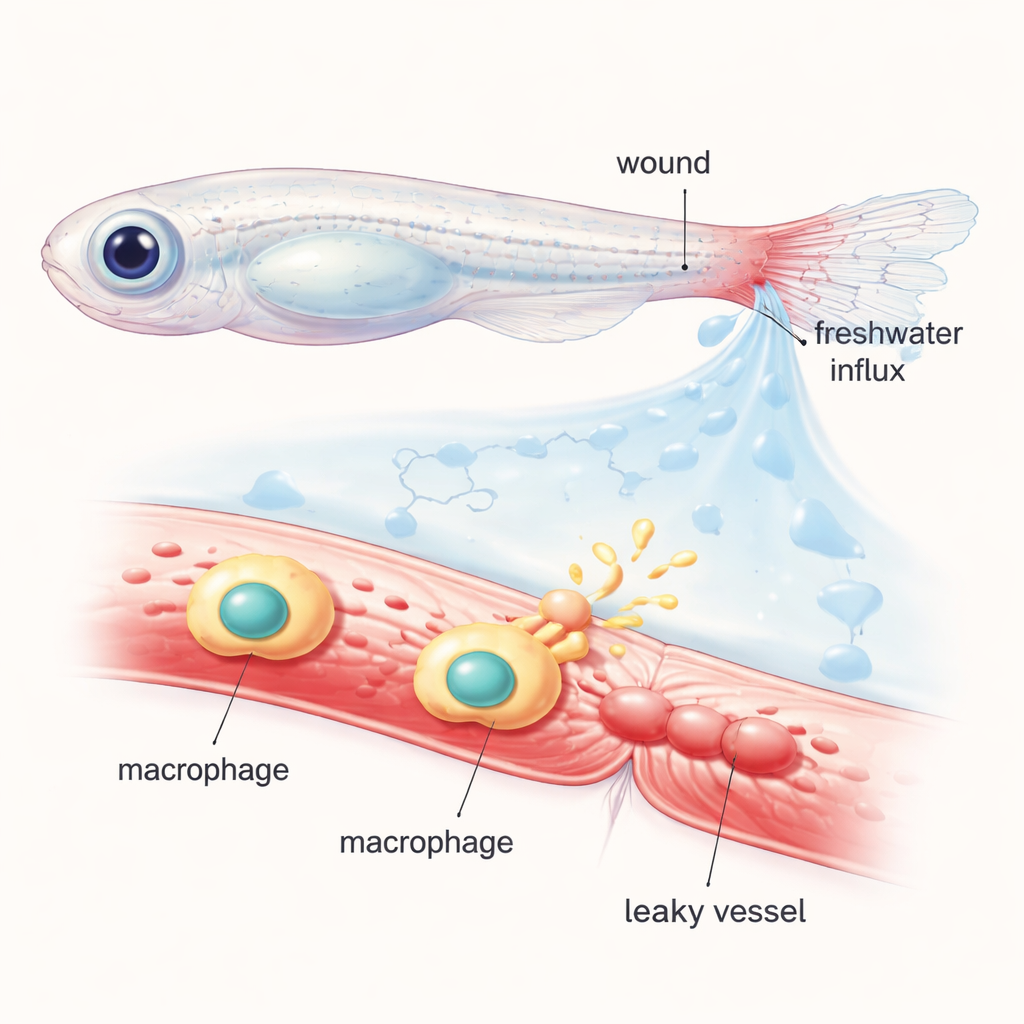
Отслеживание химических посредников, ответственных за протекание
Чтобы выяснить, какие молекулы превращают физический шок в сигнал протекания, ученые исследовали семейство жирных соединений — эйкозаноидов, образующихся из арахидоновой кислоты. Эти липиды хорошо известны своей ролью во воспалении и регуляции кровотока. Используя генетические мутанты и препараты, они избирательно подавляли отдельные ферменты в пути синтеза эйкозаноидов. Блокирование ключевого фермента Alox5a (5-липоксигеназа) или его партнера Lta4h резко снижало количество красителя, выходящего из сосудов после осмотического шока, не останавливая при этом закрытие раны. Напротив, вмешательство в другие связанные ферменты имело мало эффекта. Это указывало на конкретную ветвь липидного пути как основной драйвер быстрого ответа протекания, действующий почти как химический клапан, который можно открыть или закрыть по требованию.
Неожиданная роль иммунных клеток, обхватывающих сосуды
В крови есть разные типы иммунных клеток, и у личинок пестробрюхой рыбки основную роль играют нейтрофилы и макрофаги. Команда использовала хитрый генетический прием, чтобы избирательно уничтожить либо нейтрофилы, либо макрофаги до нанесения раны. Удаление нейтрофилов мало повлияло на протекание сосудов. Но когда макрофаги были уничтожены, реакция протекания снизилась примерно наполовину, повторяя эффект блокирования липидного пути Alox5a–Lta4h. Важно, что эти вмешательства не препятствовали быстрому закрытию раны, показывая, что привлечение лейкоцитов и сосудистое протекание могут контролироваться в значительной степени независимо. Это выявило перивascularные макрофаги — макрофаги, плотно прилегающие к внешней стороне сосудов — как ключевых переводчиков между физическим повреждением и поведением сосудов.
От растяжения ядра до химического сигнала
Как эти периваскулярные макрофаги обнаруживают рану, которая может находиться на некотором расстоянии? Ответ кроется в том, как их ядра реагируют на механическое напряжение. Когда осмотический шок от раны распространяется по окружающим тканям, поступление воды вызывает тонкое набухание клеток и деформацию ядер. Исследователи пометили механо-чувствительный фермент cPla2 флуоресцентным маркером и экспрессировали его специфически в макрофагах. После травмы в нормальной пресной воде cPla2 быстро перемещался на внутреннюю поверхность ядерной мембраны в макрофагах по волне, прокатывающейся через ткань со скоростью примерно 50 микрометров в секунду, что соответствовало скорости распространения растворенных солей. Эта транслокация зависела от гипотонических условий и была значительно слабее в изотонических растворах. Макрофаги, находящиеся рядом с сосудами, демонстрировали особенно резкие обратимые импульсы связывания cPla2 с ядром, которые, в свою очередь, высвобождают арахидоновую кислоту для превращения в липиды, индуцирующие протекание.
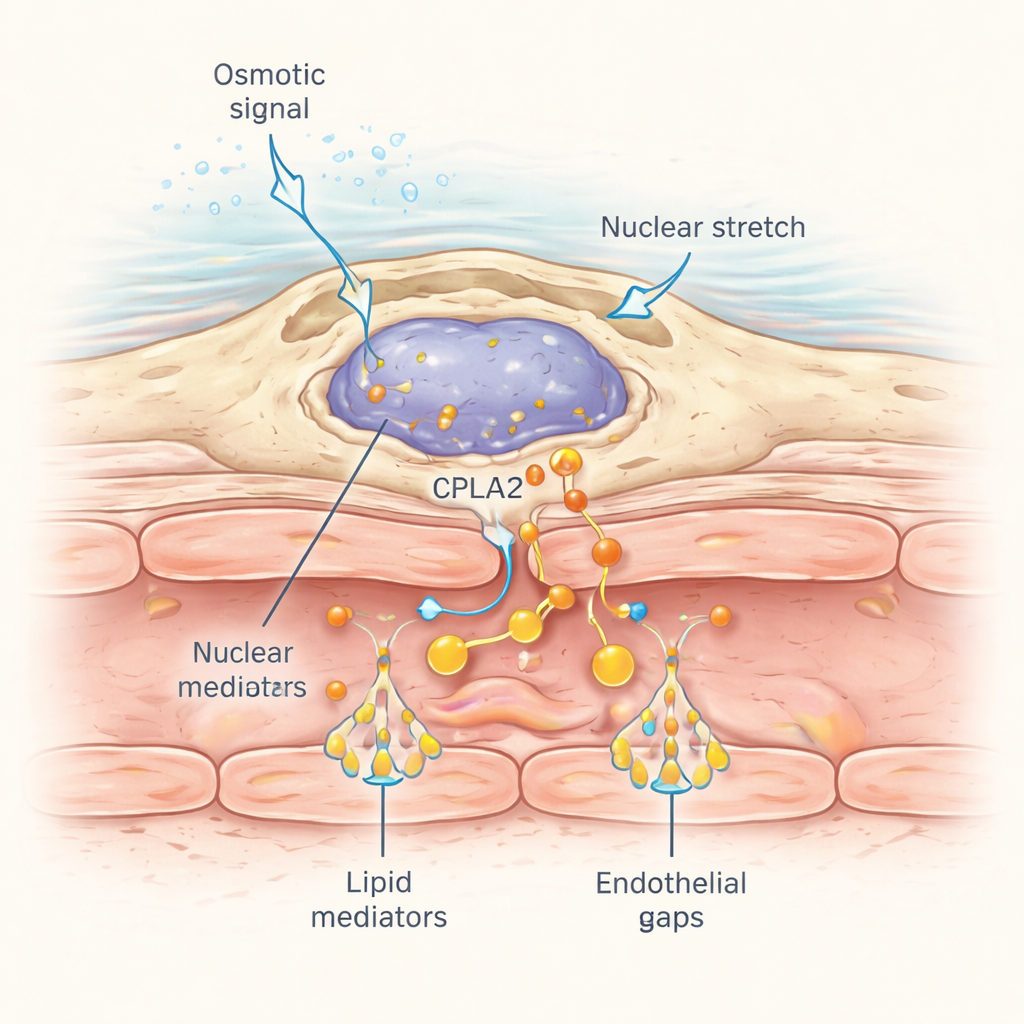
Почему это важно не только для рыб
Проще говоря, это исследование показывает, что определенные макрофаги действуют как физические часовые: они ощущают растяжение тканей и ядерных мембран, вызванное осмотическими изменениями при ранении, активируют cPla2 на ядерной поверхности и быстро производят липидные посредники, которые приказывают ближайшим сосудам «открыть ворота», впуская жидкость и иммунные факторы. Хотя пестробрюхие рыбки живут в пресной воде и сталкиваются с уникальными осмотическими вызовами, аналогичные механо-чувствительные пути, вероятно, действуют и в тканях человека, подвергающихся изменениям давления и потока, например в легких при механической вентиляции. Понимание того, как растяжение ядра и липидные сигналы контролируют проницаемость сосудов в реальном времени, в конечном счете может помочь в разработке методов лечения, которые тонко регулируют воспаление — либо снижая вредное протекание при таких состояниях, как острое повреждение легких, либо усиливая полезные реакции для ускорения заживления тканей.
Цитирование: Gelashvili, Z., Shen, Z., Ma, Y. et al. Zebrafish macrophages convert physical wound signals into rapid vascular permeabilization. Nat Commun 17, 1807 (2026). https://doi.org/10.1038/s41467-026-68520-2
Ключевые слова: заживление ран, кровеносные сосуды, макрофаги, воспаление, пестробрюхая рыбка