Clear Sky Science · ru
Механические силы, возникающие при внутриклеточной самоассамблее пептидов, приводят к образованию сфероидов
Создание крошечных тканей в лаборатории
Ученые стремятся создать миниатюрные версии человеческих тканей, которые ведут себя как настоящие. Эти живые модели позволяют безопаснее тестировать противораковые препараты и приближают новые методы лечения диабета и других заболеваний. В данном исследовании представлен изящный способ подтолкнуть клетки к формированию реалистичных трехмерных скоплений, оснащенных собственными примитивными «псевдососудистыми» сетями, улучшающими доставку питательных веществ и функциональность.
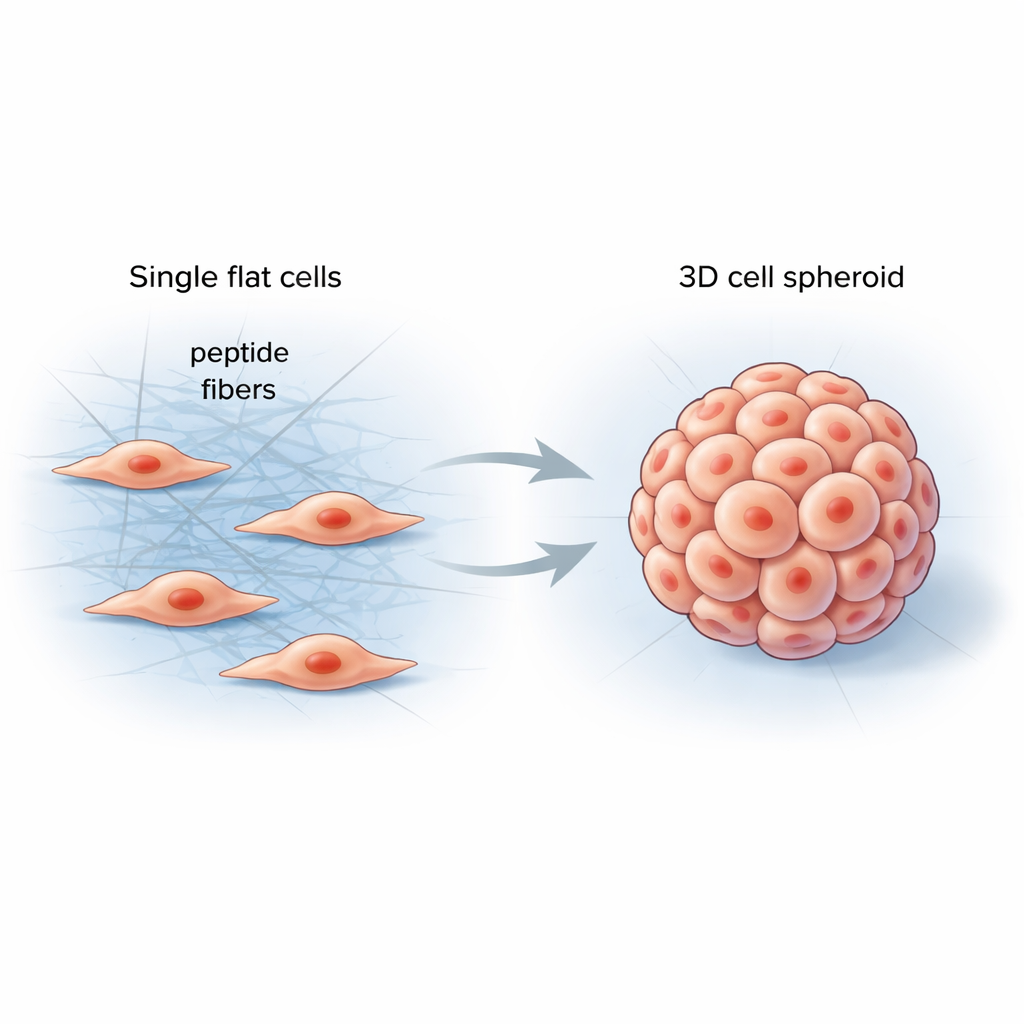
Помощь клеткам в ощущении окружения
Внутри нашего тела клетки обитают в мягкой, но упорядоченной среде, называемой внеклеточным матриксом — сети белков, поддерживающей ткани и постоянно передающей механические сигналы клеткам. Обычные лабораторные материалы с трудом имитируют эту сложность, часто давая плоские слои клеток, которые ведут себя очень иначе, чем настоящие органы или опухоли. Исследователи поставили цель разработать простой программируемый материал, который образовывался бы прямо между клетками, контролируемо менял жесткость их окружения и подталкивал их к более естественным трехмерным формам.
Умные пептиды, собирающиеся между клетками
Команда создала короткие фрагменты белков — пептиды, — которые могут связываться друг с другом в длинные тонкие волокна при встрече с определенными ферментами на поверхности клеток. Когда эти пептиды добавляли к раковым клеткам, они сначала оставались неактивными, словно прозрачный раствор. После того как собственные ферменты клеток отрезали часть молекулы, пептиды быстро самоассемблировали в волокнистую сеть, оплетающую и заполняющую пространство между соседними клетками. Эта новая волоконная сеть изменила локальные механические силы, побуждая клетки тянуть друг на друга, перестраивать внутренний каркас и собираться в округлые 3D-сфеоиды вместо того, чтобы расползаться в пласт.
От клеточных скоплений к сосудоподобным сетям
Чтобы приблизиться к реальной ткани, ученые затем ввели человеческие эндотелиальные клетки — те, что выстилают кровеносные сосуды — вместе со вторым пептидом, несущим небольшую «адресную бирку», привлекающую эти клетки. Вместе оригинальный и модифицированный пептиды образовали общий нанофибриллярный каркас. Эндотелиальные клетки использовали этот каркас, чтобы отрастать в трубчатые ответвления, оплетавшие и проникавшие в сфероиды, создавая капилляроподобные структуры. Когда команда пропускала вокруг этих структур флуоресцентные сахароподобные молекулы, они наблюдали значительно более глубокое проникновение в ядро сфероида по сравнению со сфероидами без внутренних трубок, что показало заметное улучшение транспорта питательных веществ и сигналов.
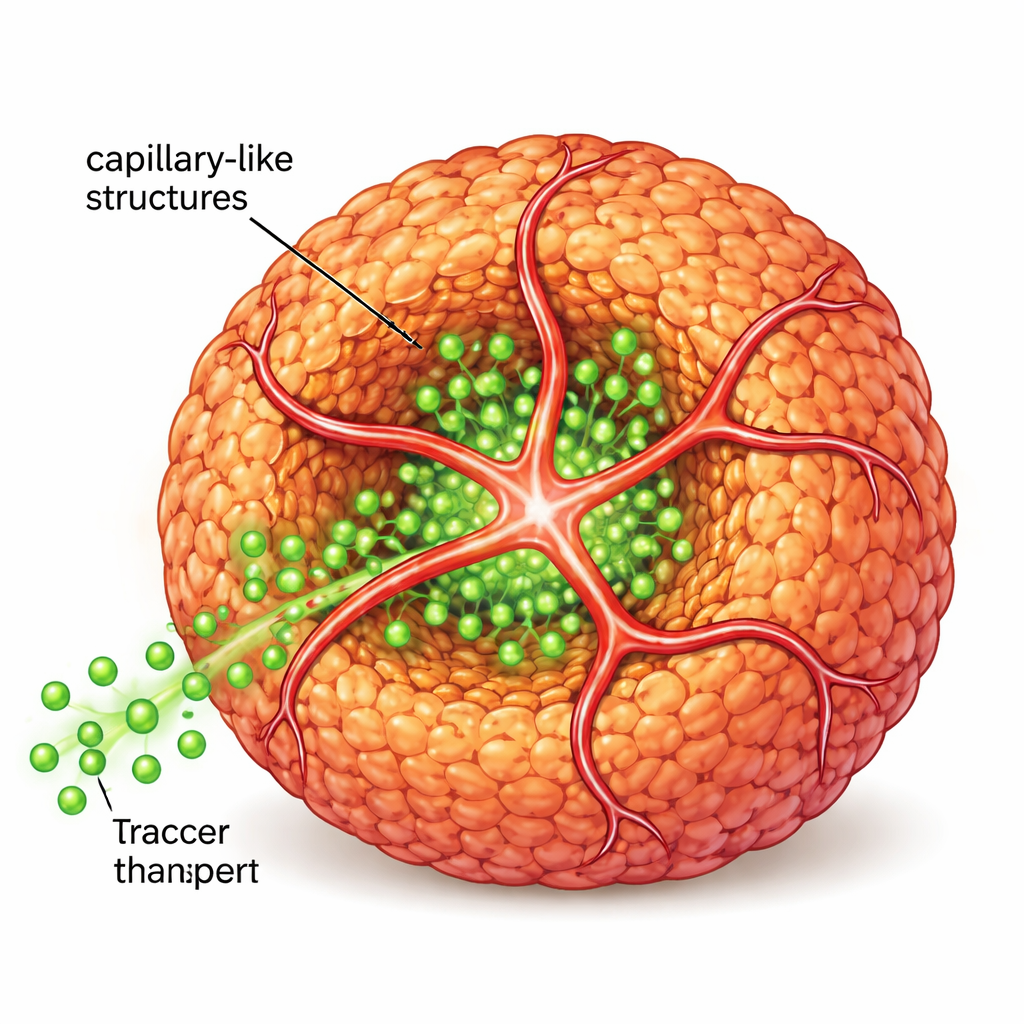
Ближе к реальным опухолям и работающим островкам
Профилирование активности генов показало, что опухолевые сфероиды с капилляроподобными структурами больше походили на образцы глиобластомы пациентов, чем традиционные плоские культуры или невосчерщенные сфероиды. В экспериментах на мышах сфероиды с этими примитивными сосудистыми сетями развивались в более крупные, лучше васкуляризованные опухоли, что свидетельствует о том, что модель in vitro захватывает ключевые черты поведения реальной опухоли. Та же стратегия применялась к панкреатическим бета-клеткам, которые в норме живут в интенсивно васкуляризованных островках и секретируют инсулин в ответ на глюкозу. Когда сфероиды бета-клеток оснащали капилляроподобными структурами с помощью пептидной системы и эндотелиальных клеток, они демонстрировали значительно более сильный и тонко регулируемый выброс инсулина, что предлагает мощный инструмент для исследований диабета и регенеративной медицины.
Почему это важно для будущих терапий
Позволив простым пептидам самоассамблироваться между живыми клетками, эта работа предлагает универсальный рецепт создания миниатюрных васкуляризованных тканей, которые по ощущениям и функциям ближе к тем, что внутри организма. Получившиеся сфероиды лучше отражают опухоли пациентов и работающие островки, делая их ценными для тестирования препаратов, изучения механизмов заболеваний и разработки новых клеточных терапий. Для неспециалистов главный вывод таков: обеспечение выращиваемым в лаборатории клеткам «правильного ощущения» и крошечных сосудоподобных сетей может резко повысить их сходство с человеческими тканями и потенциально ускорить путь от базовых исследований к эффективным лечениям.
Цитирование: Lu, H., Li, Y., Yang, X. et al. Mechanical forces from intercellular peptide self-assembly drive spheroid formation. Nat Commun 17, 1801 (2026). https://doi.org/10.1038/s41467-026-68513-1
Ключевые слова: тканевая инженерия, модели рака, ангиогенез, органоиды, самоассамблея пептидов