Clear Sky Science · ru
Прерывистое голодание тормозит глиому, управляемую Tp53, через регуляцию метионина и m6A, опосредованную микробиотой кишечника
Почему дача «перерыва» кишечнику может замедлить смертоносные опухоли мозга
Глиобластома — один из наиболее агрессивных видов рака мозга, и нынешние методы лечения — операция, лучевая терапия и химиотерапия — часто добавляют пациентам лишь немного времени. В этом исследовании поставлен простой, но важный вопрос с крупными последствиями для повседневной жизни: может ли наш режим питания, в частности прерывистое голодание, изменить состав кишечных бактерий и состав крови настолько, чтобы существенно замедлить развитие некоторых опухолей мозга?
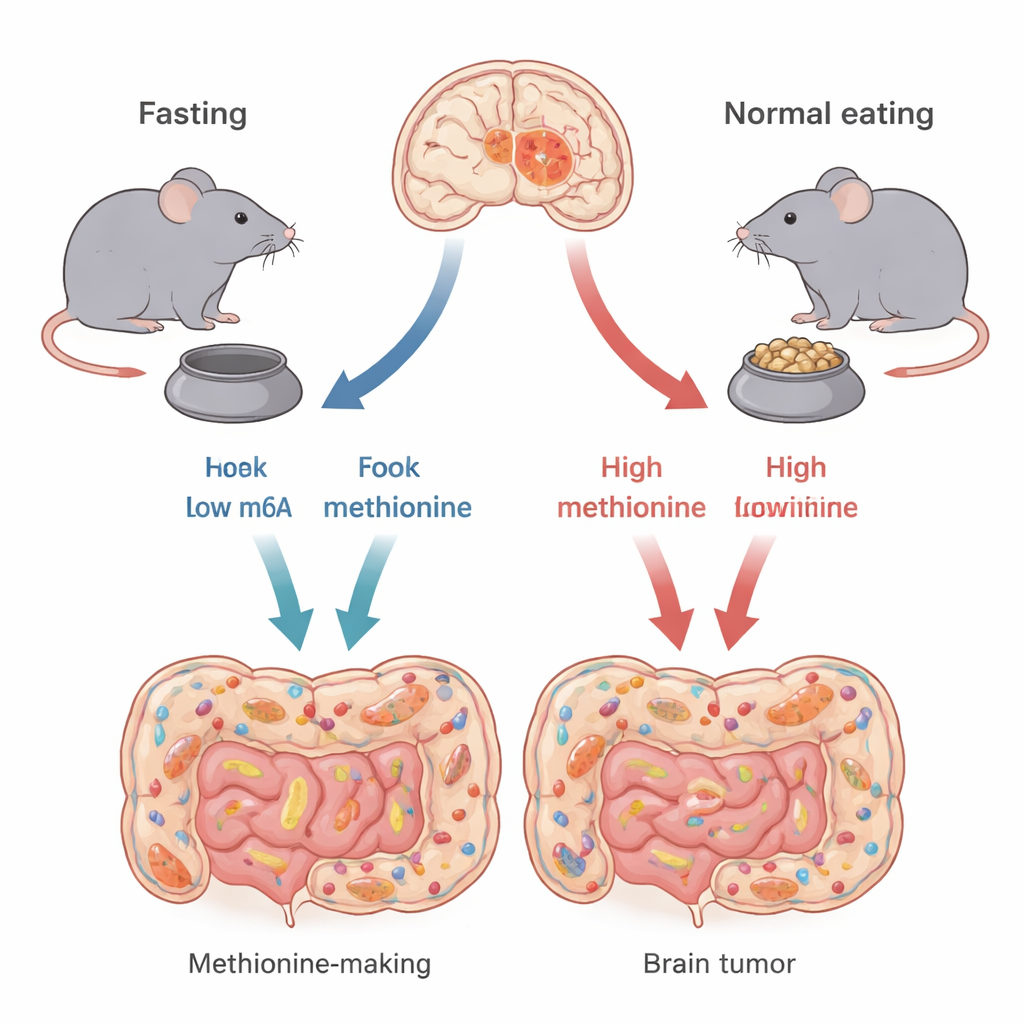
Разные варианты «одного» рака мозга
Не все глиобластомы одинаковы. Авторы сосредоточились на двух основных генетических типах, определяемых изменениями в генах TP53 и CDKN2A. Эти гены помогают контролировать рост и гибель клеток. На мышиных моделях, которые хорошо имитируют каждый человеческий подтип, исследователи показали, что прерывистое голодание — 24 часа без пищи с последующими 24 часами приема пищи — помогает не всем опухолям одинаково. Мыши с опухолями типа TP53 жили дольше и имели меньшие опухоли при голодании, тогда как у мышей с опухолями типа CDKN2A наблюдалось мало пользы. Это указывает на то, что эффект голодания может в значительной степени зависеть от генетической схемы опухоли.
От режима питания к кишечным бактериям к химии мозга
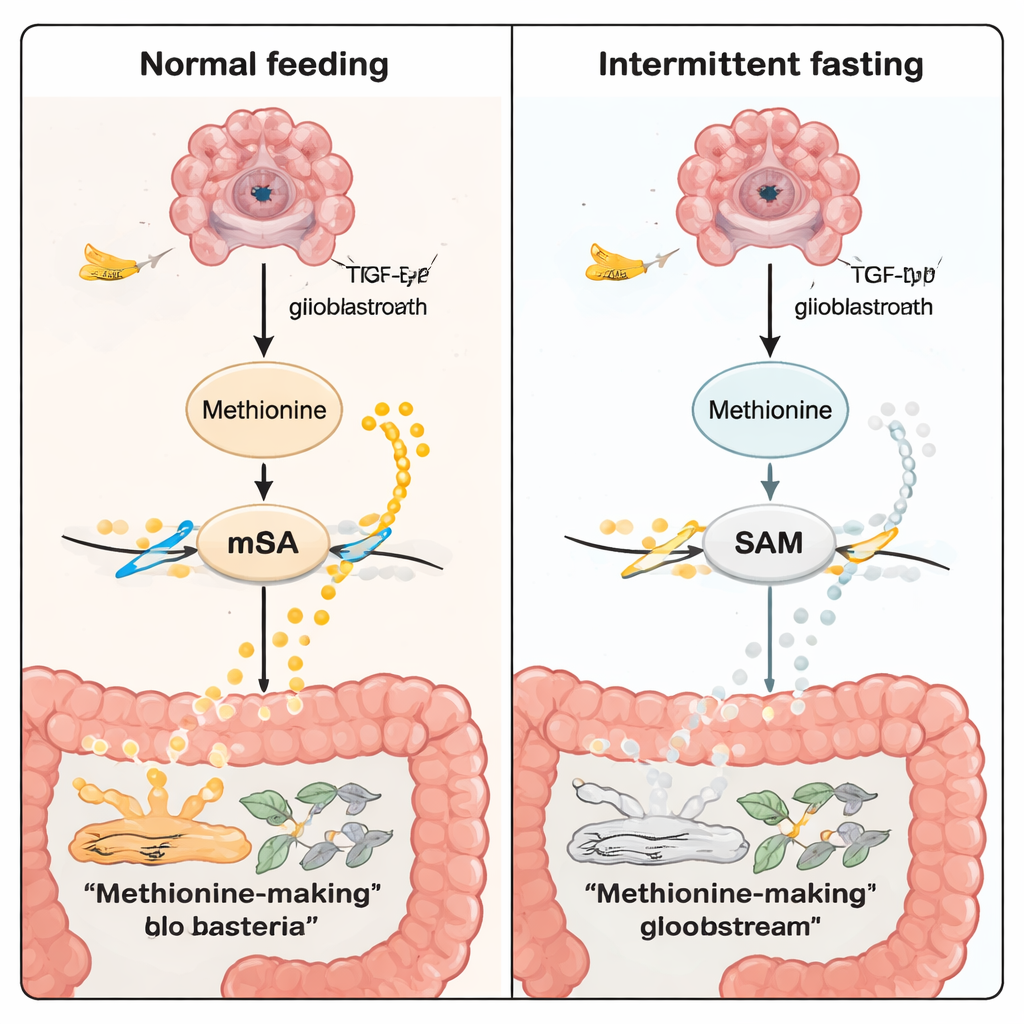
Далее команда задала вопрос, как именно голодание оказывает выборочное влияние. Поскольку общее количество пищи между группами поддерживалось одинаковым, ключевым отличием оказался только режим приема пищи. Этот режим сильно перестроил микробиоту кишечника — обширное сообщество бактерий в кишечнике. У голодающих мышей с типом TP53 сократилась численность определенных групп бактерий, эффективно синтезирующих аминокислоту метионин, например некоторые штаммы родов Alistipes и Prevotella. Поскольку метионин — незаменимый строительный блок, который животные должны получать из пищи или от микробов кишечника, такое микробное смещение означало меньше метионина, поступающего из кишечника в кровь и, в конечном счете, в мозг.
Как одна питательная молекула настраивает сигналы, ведущие к раку
Метионин — это не просто питательное вещество; он также исходный материал для S-аденозилметионина (SAM), универсального «донорa метильных групп» в клетке. SAM питает процесс химической метки РНК, называемый m6A. Эти метки помогают регулировать силу экспрессии определенных генов. В модели опухоли TP53 голодание снижало уровни метионина и SAM в крови и в областях опухоли мозга. С применением нескольких уровней омникс-технологий — стандартного РНК-секвенирования, профилирования РНК по отдельным клеткам и пространственных карт как активности генов, так и метаболитов — исследователи обнаружили меньше меток m6A на ключевых РНК, связанных с раком, при голодании. Важной целью оказался ген TGFB2, входящий в сигнальный путь TGF‑β, известный тем, что стимулирует рост и инвазию опухолей. При голодании и фермент METTL3 (который «записывает» метки m6A), и TGFB2 были понижены, а сигналы TGF‑β ослабли.
Доказательство причинно-следственной связи с помощью целевых вмешательств
Чтобы выйти за пределы корреляции, ученые провели «восстановительные» эксперименты. Они блокировали METTL3 с помощью препарата или переносили кишечную микробиоту от голодающих мышей к обычно кормимым мышам, и наблюдали замедление роста опухолей даже без голодания — что подтверждает идею о том, что и микробиота, и машина m6A являются ключевыми участниками. Наоборот, когда голодающим мышам давали дополнительный метионин или лечили препаратами, усиливающими метки m6A, их опухоли развивались подобно опухолям у обычно кормимых мышей, и преимущество по выживаемости исчезало. Важно, что нарушение кишечной микробиоты широким спектром антибиотиков стирало многие изменения, связанные с голоданием, подчеркивая, что сообщество кишечных бактерий является центральным узлом в этой цепочке событий.
Что это значит для людей и будущих терапий
Для неспециалиста основной вывод таков: не все виды рака, и даже не все глиобластомы, будут одинаково реагировать на диетическую стратегию вроде прерывистого голодания. При глиомах типа TP53 голодание, по-видимому, «общается» с мозгом через кишечник: оно перестраивает кишечные бактерии, что в свою очередь снижает продукцию метионина, уменьшает химическую маркировку РНК и ослабляет мощные сигналы роста внутри опухолевых клеток. Хотя эти результаты получены на мышах и требуют аккуратной клинической трансляции, они указывают на будущее, в котором простые схемы образа жизни, терапии, основанные на микробиоте кишечника, и препараты, нацеленные на метионин или пути m6A, могут быть адаптированы к генетическому подтипу опухоли пациента.
Цитирование: Lin, Y., Li, S., Xu, X. et al. Intermittent fasting inhibits Tp53-driven glioma through gut microbiota-mediated methionine-m6A regulation. Nat Commun 17, 1804 (2026). https://doi.org/10.1038/s41467-026-68512-2
Ключевые слова: прерывистое голодание, глиобластома, микробиом кишечника, метаболизм метионина, модификация РНК m6A