Clear Sky Science · ru
Одновременное окисление сульфида и восстановление сульфата для внутриклеточного редокс-гомеостаза в сильно кислых условиях
Почему уборка токсичных газов требует хитрых микроорганизмов
Множество отраслей выбрасывают сероводород — ядовитый газ с запахом тухлых яиц, который может разъедать оборудование, загрязнять воздух и вредить работникам. Для его очистки инженеры всё чаще полагаются на микроорганизмы, превращающие сульфид в более безопасные формы серы. В этой работе показана неожиданная микробная стратегия: недавно обнаруженный вид Mycobacterium одновременно запускает два обычно противоположных химических пути, чтобы быстро детоксицировать сульфид и при этом защищать себя от внутреннего повреждения, даже в крайне кислой среде.
Тянучка в серном цикле
В природе серный цикл поддерживается двумя противоположными реакциями. Одни микроорганизмы окисляют сульфид (наиболее восстановленную и токсичную форму) в менее вредные продукты, такие как элементная сера или сульфат, при этом извлекая энергию. Другие идут в обратном направлении, восстанавливая сульфат обратно до сульфида, чтобы синтезировать важные клеточные компоненты, например серосодержащие аминокислоты. Поскольку эти реакции взаимно исключают друг друга, биологи долгое время считали, что одна и та же клетка избегает их одновременного протекания; это казалось расточительным, как обогрев и охлаждение дома с открытыми окнами. 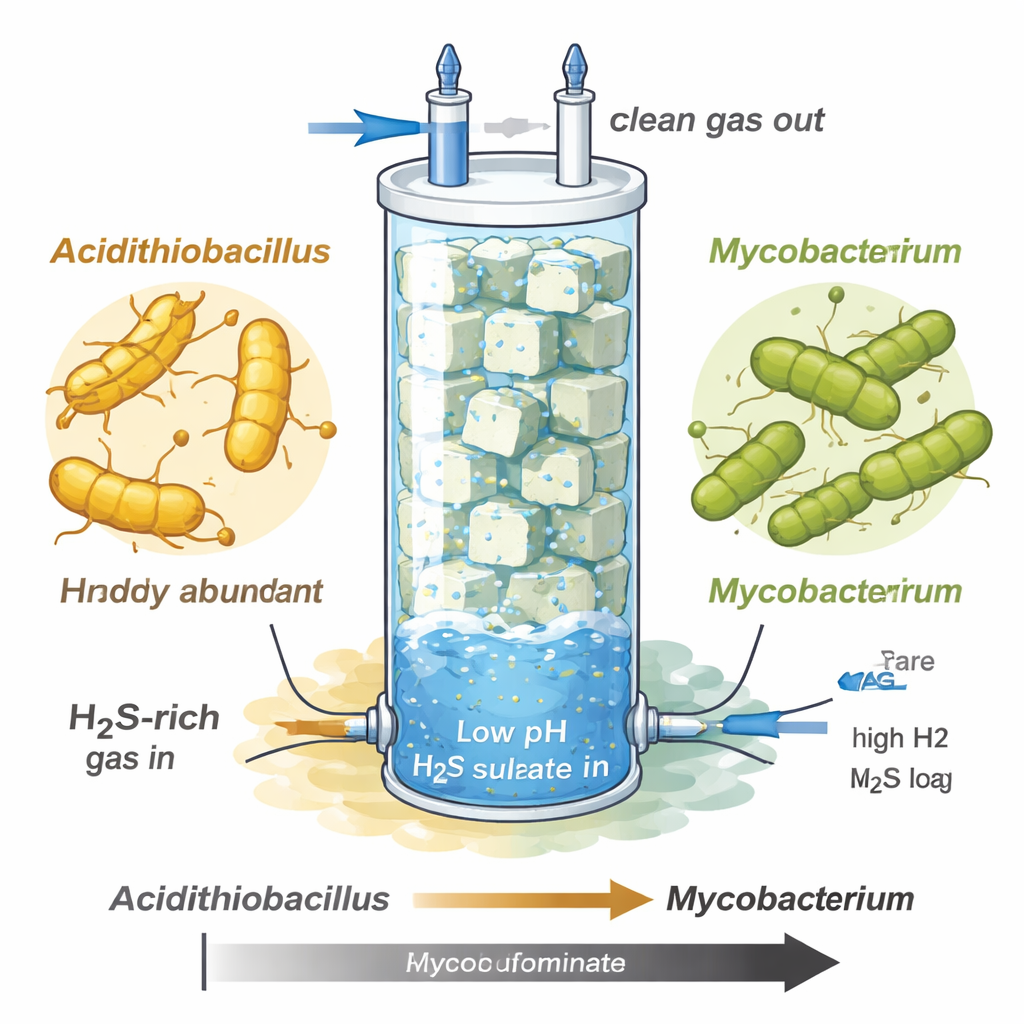
Нахождение выжившего в экстремальном реакторе
Исследователи изучали биофильтр-колонну — высокий стеклянный столб, заполненный пористыми кубиками — предназначенный для очистки сероводорода из газовых потоков, похожих на сырый биогаз или природный газ. По мере увеличения нагрузки сульфидом и поддержания очень кислой среды (pH около 1–1,5) микробное сообщество резко изменилось. Сначала преобладал хорошо известный окислитель сульфида Acidithiobacillus, который превращал большую часть сульфида в сульфат, но позже он рухнул под экстремальным сульфидным стрессом. На его месте почти всё сообщество занял ранее неохарактеризованный вид Mycobacterium, обозначенный MAG-M116, несмотря на то что в начальной, более мягкой фазе он рос медленнее.
Микроб, нарушающий обычные правила
Генетический и протеомный анализы показали, что у MAG-M116 необычная метаболическая организация. Он содержит ключевой фермент сульфид:хинон оксидоредуктазу, который окисляет сульфид лишь до твертой элементной серы, накапливающейся в виде крошечных частиц. Одновременно микроорганизм обладает полным набором генов для ассимиляционного восстановления сульфата — пути, который захватывает сульфат внутрь клетки и восстанавливает его для синтеза аминокислот, таких как цистеин и метионин. При высоких концентрациях сульфида оба пути включались одновременно. Окисление сульфида подавало электроны в энергетическую цепь клетки, тогда как восстановление сульфата забирать часть этого электронного потока, связывая два направления серного цикла внутри одной клетки.
Превращение «расточительного» цикла в предохранительный клапан
Запуск обоих путей одновременно теоретически мог бы быть бесполезным — расходованием энергии без чистой выгоды. Но команда показывает, что для MAG-M116 это работает как предохранительный клапан для избытка электронов. Окисление больших количеств сульфида высвобождает прилив электронов в дыхательную цепь клетки, которые могут утекать и вести к образованию реактивных форм кислорода (ROS) — вредных молекул, разрушающих ДНК, белки и мембраны. Активно восстанавливая сульфат до аминокислот, клетка перенаправляет 10–14% этих электронов на конструктивные процессы, снижая накопление чрезмерно восстановленного, склонного к утечкам состояния. Эксперименты в условиях с сульфатом и без него показали, что активное восстановление сульфата сокращало производство ROS примерно до 60% и предотвращало накопление восстановленных кофакторов, которые в противном случае подпитывали бы окислительное повреждение. 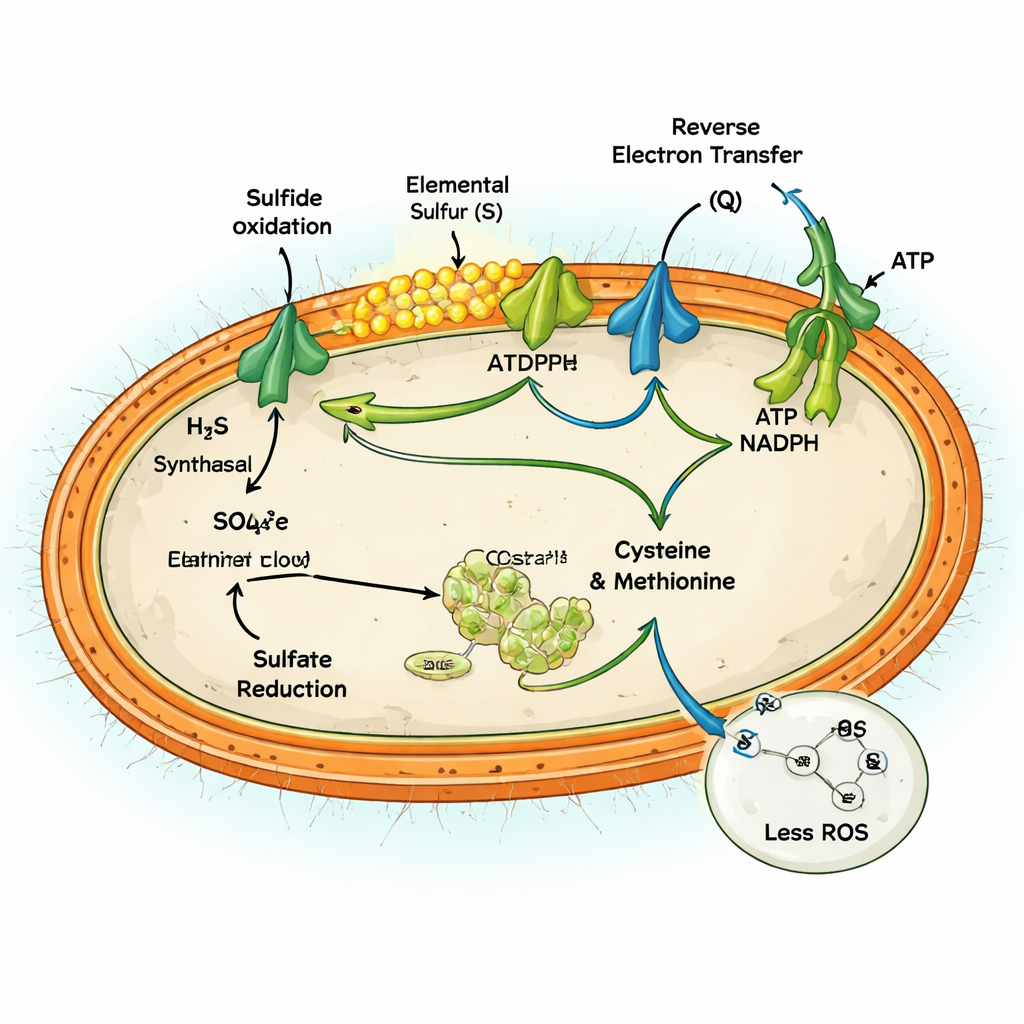
От токсичного газа к полезным продуктам
На поздних этапах работы реактора, когда MAG-M116 доминировал, почти весь поступающий сероводород превращался в твердую элементную серу, а не в сульфат. Одновременно исследователи фиксировали рост концентраций цистеина и метионина в жидкой фазе, что говорит о том, что микроорганизм выделял избыточные серосодержащие аминокислоты в окружение. Такая комбинация — стабильная элементная сера плюс ценные органические серосодержащие соединения — превращает ранее опасный загрязнитель в смесь восстанавливаемых продуктов, применимых в сельском хозяйстве, материалах и энергетике.
Что это значит для здоровья и технологий
Для неспециалиста главный вывод в том, что этот Mycobacterium решил двойную задачу: он может убирать высокие концентрации токсичного газа и одновременно поддерживать собственную внутреннюю химию в равновесии. Он делает это, запуская «тянуто-толкающие» серные реакции, которые обычно держали раздельно, используя кажущийся расточительным цикл как встроенный амортизатор для избытка электронов и вредных кислородных радикалов. Это открытие не только предлагает новые подходы к проектированию устойчивых биореакторов для работы при низком pH с целью удаления сульфида и сульфата, но и намекает, что родственные микроорганизмы, включая патогенные виды Mycobacterium, могут использовать похожие трюки для выживания при окислительном стрессе в организме человека.
Цитирование: Jia, T., Peng, Y., Niu, L. et al. Simultaneous sulfide oxidation and sulfate reduction for intracellular redox homeostasis under highly acidic conditions. Nat Commun 17, 1797 (2026). https://doi.org/10.1038/s41467-026-68508-y
Ключевые слова: серный цикл, сероводород, Mycobacterium, редокс-гомеостаз, биодесуфуризация