Clear Sky Science · ru
Пространственно-временное контролируемое высвобождение лекарств с помощью click-release системы на основе моноалкилгидроксиламина и циклooктиновой химии
Включение мощных препаратов только там, где они нужны
Многие современные лекарства чрезвычайно сильны — это полезно против рака или для снятия боли, но опасно для остального организма. В этой работе описана основанная на химии «включающая/выключающая» система, которая позволяет переводить препараты в неактивную, безвредную форму и затем активировать их только в выбранном месте и в нужное время — например внутри опухоли или в небольшой области, требующей местной анестезии.
Новый тип химического переключателя
Исследователи развивают концепцию «click-химии», семейства реакций, ценимых за скорость, точность и способность безопасно протекать в живых системах. Классические click-реакции прочно соединяют два молекулярных фрагмента. Здесь команда меняет логику: их click-реакция непосредственно связана с разрывом связи и освобождением лекарства или сигнальной молекулы. Ключевые участники — кольцеобразная молекула циклooктин (cyclooctyne) и небольшая молекула моноалкилгидроксиламин. При их встрече они быстро схватываются и затем перестраиваются так, что связанный «груз» отрубается и освобождается. Прикрепляя в качестве груза разные лекарства или флуоресцентные красители, ту же базовую реакцию можно использовать для многих задач. 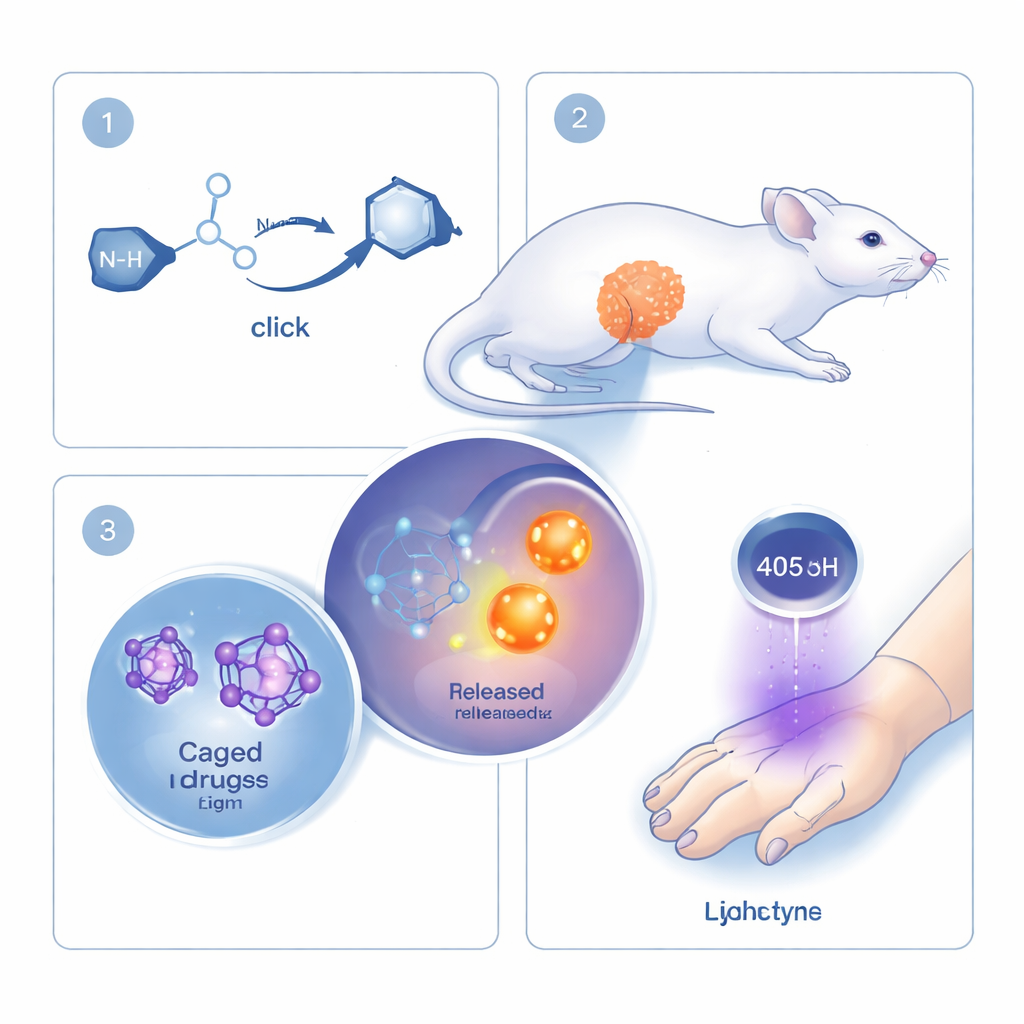
Быстрое, чистое высвобождение внутри и вне клеток
Чтобы оценить практическую пригодность переключателя, команда измерила скорость реакции и степень освобождения присоединённого груза. Они обнаружили, что тщательно подобранные моноалкилгидроксиламины реагируют значительно быстрее простого гидроксиламина, достигая почти полного превращения в течение минут — часов, в зависимости от структуры. Важно, что химические шаги, непосредственно приводящие к освобождению груза, настолько быстры и селективны, что почти весь связанный фрагмент отрывается с минимальными побочными продуктами. Авторы протестировали ряд грузов, включая флуоресцентные красители и даже ион фтора, и показали, что система способна разрывать несколько обычных типов связей, применяемых в дизайне лекарств, таких как карбаматы и эфиры.
Подсвечивание клеток и активация противораковых препаратов по требованию
Далее исследователи перешли к живым клеткам. Они сначала скрыли яркие флуоресцентные красители за химическим переключателем и добавили эти «запертые» зонды в раковые клетки. Сами по себе зонды оставались тёмными, что показало отсутствие случайной активации клетками. После добавления партнёра — моноалкилгидроксиламина — красители освобождались, и клетки «зажигались» в синем, зелёном или ближнем инфракрасном диапазоне, подтверждая, что реакция надёжно протекает в биологической среде. Затем тот же подход применили к доксорубицину, широко используемому химиотерапевтическому препарату. В заточённой (пропрепаратной) форме доксорубицин был существенно менее токсичен для клеток. Но при наличии click-партнёра активный препарат эффективно высвобождался, восстанавливая способность убивать раковые клетки почти столь же сильно, как свободный доксорубицин.
Создание умных триггеров для места и времени
Ограничение многих существующих click-систем в том, что реактивные фрагменты постоянно «включены», что затрудняет точный контроль места и момента активации. Чтобы это обойти, команда временно блокировала реактивность моноалкилгидроксиламина малыми защитными колпачками, которые удаляются только специфическими триггерами. Они создали версии, реагирующие на высокие уровни глутатиона (молекулы, обильно представленной во многих опухолях), на ферменты и на вспышки фиолетового света. В клетках и у мышей с опухолями версия, чувствительная к глутатиону, оставалась неактивной в нормальных условиях, но включалась в химически восстановительной среде опухоли, высвобождая флуоресцентные красители или активируя доксорубицин-пропрепарат прямо в месте роста рака. Мыши, получавшие комбинацию пропрепарата и триггера, демонстрировали более выраженное уменьшение опухолей по сравнению с теми, кому давали стандартный доксорубицин, при этом испытывая меньшую экспозицию препарата в чувствительных органах, таких как сердце.
Удалённая локальная анестезия под управлением света
Чтобы продемонстрировать контроль по времени, авторы разработали ещё одно применение: светоуправляемую местную анестезию. Они прикрепили обезболивающее тетракаин к своей циклooктиновой матрице, сделав его неактивным, и смешали этот пропрепарат с фоточувствительной версией гидроксиламина в температурочувствительном геле. Введение смеси в лапу крысы не давало эффекта до тех пор, пока кожу не освещали светом с длиной волны 405 нм. Освещение запускало click-release реакцию, освобождая тетракаин и вызывая онемение, сопоставимое с прямой инъекцией тетракаина. Изменяя длительность и интенсивность освещённости, исследователи могли регулировать длительность блокады нерва и даже многократно вызывать волны анестезии после одной инъекции. 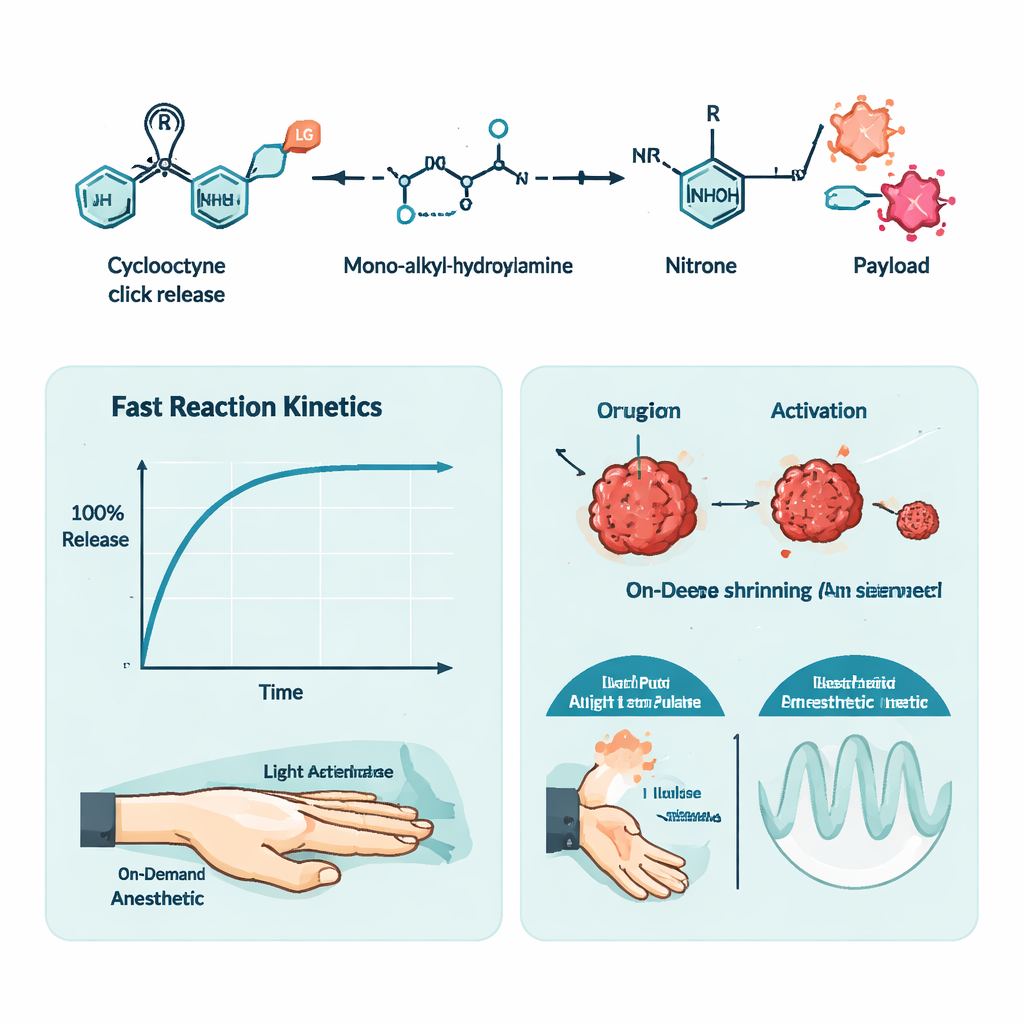
Что это может значить для будущих терапий
Для неспециалистов ключевая мысль в том, что работа предлагает гибкий химический «дистанционный пульт» для лекарств: препараты можно доставлять в безопасной, неактивной форме и затем активировать только в нужном месте и в нужный момент, используя сигналы, исходящие из организма или внешний источник света. Хотя перед клиническим применением требуется больше испытаний, подход в перспективе может сделать лечение рака более целевым и менее токсичным, обеспечить настраиваемый контроль боли после операций и поддержать другие терапии, выигрывающие от точного пространственно-временного управления.
Цитирование: Xu, X., Tong, X., Shi, Y. et al. Spatiotemporally controlled drug release via a click-release system utilizing mono-alkyl-hydroxylamine and cyclooctyne chemistry. Nat Commun 17, 1794 (2026). https://doi.org/10.1038/s41467-026-68502-4
Ключевые слова: click-химия, целевое доставление лекарств, пропрепараты, микроокружение опухоли, светоконтролируемая анестезия