Clear Sky Science · ru
Таргетирование каскада UFL1–AKT подавляет прогрессирование тройного негативного рака молочной железы
Почему это исследование важно
Тройной негативный рак молочной железы (TNBC) — одна из самых смертоносных форм рака молочной железы, потому что в ней отсутствуют гормональные и фактор-роста переключатели, на которые нацелены многие современные препараты. Пациентам часто назначают только традиционную химиотерапию, которая со временем может перестать действовать из‑за развития резистентности опухолей. В этом исследовании выявлен ранее скрытый молекулярный «двигатель», который помогает клеткам TNBC расти и противостоять химиотерапии, и предложен новый тип препарата, который прямо «заклинивает» этот двигатель.
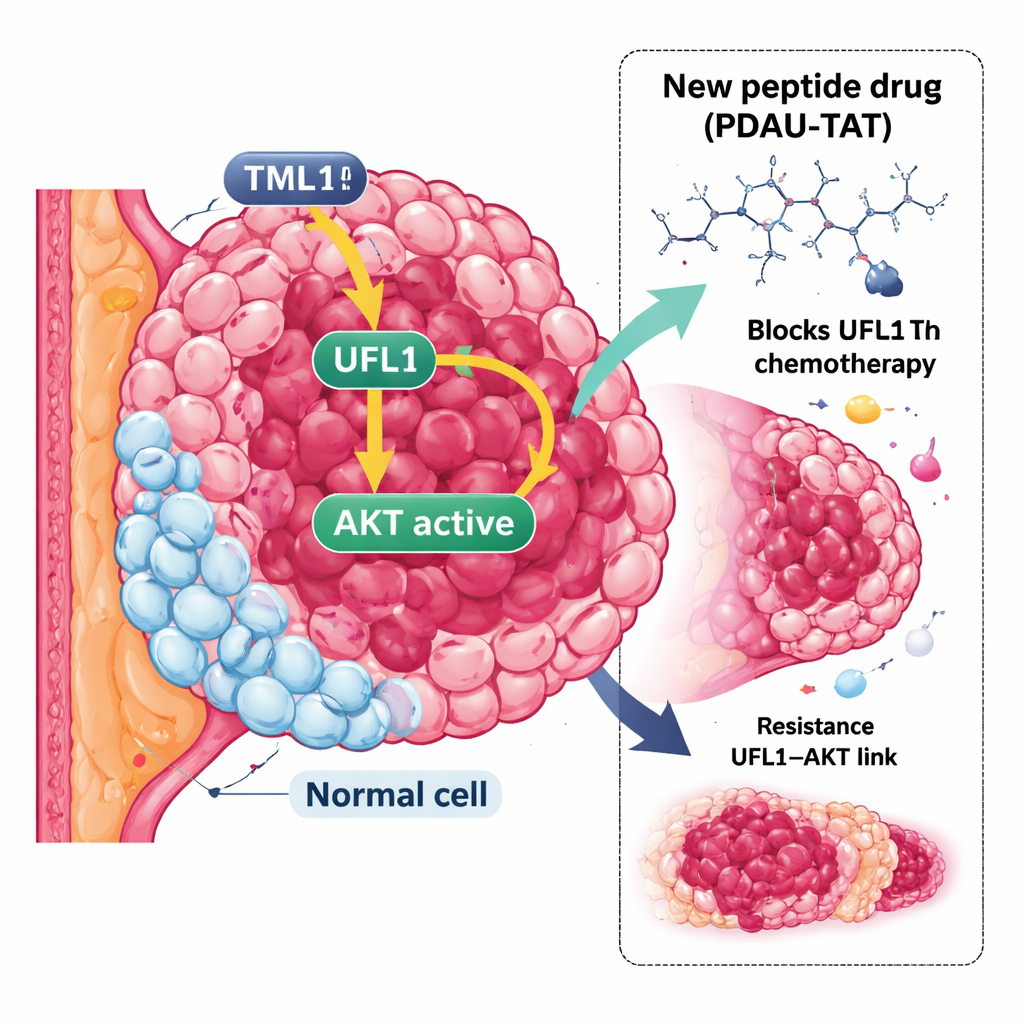
Упрямый тип рака молочной железы
TNBC определяется отсутствием трёх распространённых маркёров: эстрогенового рецептора, прогестеронового рецептора и рецептора роста HER2. Без этих маркёров многие эффективные таргетные терапии неприменимы. Вместо них используются стандартные препараты, такие как цисплатин и доксорубицин, но опухоли TNBC часто проявляют резистентность или быстро адаптируются к этим лечением и имеют большую склонность к метастазированию. Это создаёт острую необходимость в новых стратегиях, выходящих за рамки привычных целей и ищущих другие уязвимые места в системах контроля опухоли.
Малоизвестный белок с большим влиянием
Учёные сосредоточились на UFL1 — белке, который присоединяет маленькую метку, называемую UFM1, к другим белкам в процессе, известном как UFMylation. Эта система меток была открыта сравнительно недавно, и её роль в онкологии оставалась неясной и иногда противоречивой. Анализ данных пациентов и образцов опухолей показал, что уровень UFL1 заметно повышен в TNBC по сравнению с нормальной тканью молочной железы. При снижении уровня UFL1 в клеточных линиях TNBC и в мышиных моделях опухолей клетки рака размножались медленнее и становились значительно чувствительнее к химиотерапии, что указывает на проопухолевую роль UFL1 в этом контексте.
Связывание UFL1 с центральным переключателем роста
Глубже изучив механизм, исследователи обнаружили, что UFL1 напрямую связывается с AKT — ключевым сигнальным белком, управляющим ростом, выживанием и метаболизмом клеток, часто гиперактивным при раке. В TNBC AKT часто оказывается сверхактивным даже при отсутствии типичных мутаций выше по цепочке сигнализации. Команда показала, что UFL1 ковалентно отмечает AKT в трёх конкретных позициях, что облегчает его активацию партнёрами и защищает от ферментов, которые обычно его выключают. Клетки без UFL1 или экспрессирующие модифицированную форму AKT, неспособную получать эти метки, демонстрировали значительно пониженную активность AKT, замедленный рост и повышенную уязвимость к химиотерапии как в культурах клеток, так и в животных моделях.
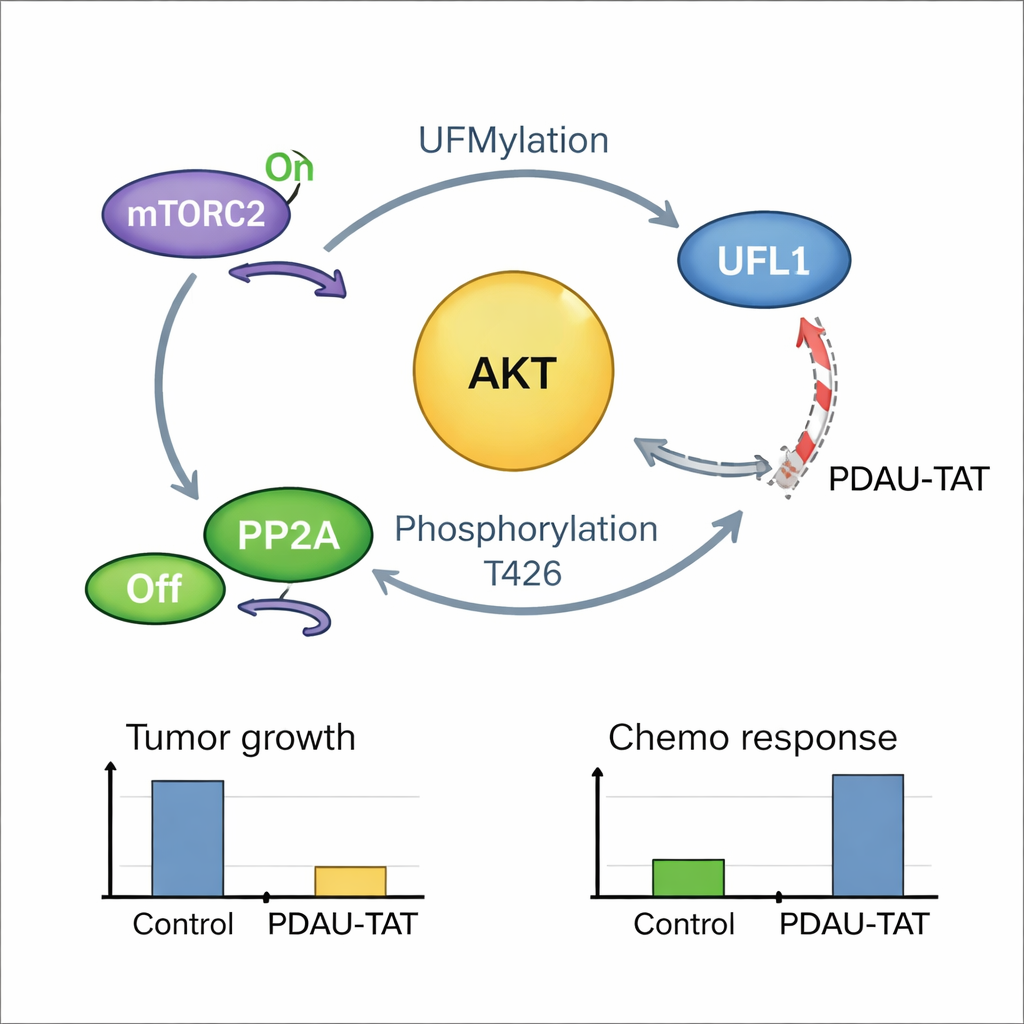
Самоподдерживающаяся онкологическая петля и способ её разорвать
Оказалось, что взаимоотношения ещё теснее: активированный AKT в свою очередь модифицирует UFL1 в одной ключевой позиции, повышая тагирующую активность UFL1 в отношении AKT и других мишеней. Это создаёт положительную петлю обратной связи, в которой UFL1 активирует AKT, а активный AKT усиливает UFL1. Образцы опухолей пациентов показали сильную корреляцию между высоким уровнем модифицированного UFL1 и активным AKT, что подтверждает существование этой петли при человеческом заболевании. Чтобы воспользоваться этой уязвимостью, исследователи разработали короткий проникающий в клетки пептид PDAU‑TAT, который имитирует небольшой участок UFL1 и вклинивается между UFL1 и AKT. Этот пептид нарушает их взаимодействие, снижает активацию AKT, замедляет рост опухолей и делает клетки TNBC и опухоли, полученные от пациентов, более отзывчивыми на химиотерапию, при этом явных повреждений основных органов у мышей не наблюдалось.
Что это может означать для пациентов
Проще говоря, исследователи выявили скрытую схему управления в клетках TNBC: UFL1 и AKT находятся в самоусиливающейся петле, которая удерживает сигналы роста во включённом состоянии и помогает опухолям сопротивляться лечению. Создав небольшой пептид, разрывающий эту петлю и разъединяющий UFL1 и AKT, они показали правдоподобный новый подход к ослаблению TNBC при относительно малом воздействии на нормальные клетки, у которых, как правило, уровни UFL1 ниже. Хотя работа всё ещё на доклинической стадии, она указывает на новую категорию таргетных терапий, направленных не на обычные рецепторы, а на белок–белковые взаимодействия, подпитывающие некоторые из самых агрессивных форм рака молочной железы.
Цитирование: Yang, X., Wen, Y., Ma, X. et al. Targeting the UFL1-AKT cascade suppresses triple-negative breast cancer progression. Nat Commun 17, 613 (2026). https://doi.org/10.1038/s41467-026-68493-2
Ключевые слова: тройной негативный рак молочной железы, AKT-сигналинг, UFMylation, UFL1, пептидная противораковая терапия