Clear Sky Science · ru
Положительная петля обратной связи UFL1–AKT способствует прогрессированию рака молочной железы за счёт усиления синтеза липидов
Почему раковым клеткам так важны жиры
Клетки рака молочной железы, как и любые быстро делящиеся клетки, нуждаются в постоянном запасе строительных блоков для создания новых мембран и сигнальных молекул. Жиры, или липиды, — ключевая часть этого запаса. В этом исследовании показано, как малоизвестная белковая система переводит раковые клетки в режим «сверхпроизводства жира», помогая опухолям расти и уклоняться от лечения. Понимание этой скрытой топливной линии может открыть новые пути для замедления или «голодания» рака молочной железы.
Скрытая белковая метка с серьёзными последствиями
Наши клетки постоянно регулируют поведение белков с помощью небольших химических меток. Одна из таких меток, называемая UFM1, добавляется ферментом UFL1. Модификация UFM1 (UFMylation) уже связывалась с репарацией ДНК и ответом на стресс, но её роль в раке была неясна. Авторы показывают, что UFL1 значительно активнее в опухолях молочной железы человека по сравнению с нормальной тканью молочной железы, во всех основных подтипах. У пациентов с опухолями, в которых уровень UFL1 выше, выживаемость хуже. Когда исследователи снижали уровень UFL1 в клетках рака молочной железы или в опухолях у мышей, рост рака замедлялся, деление клеток уменьшалось, а гибель клеток увеличивалась, что указывает на то, что UFL1 ведёт себя как фактор, способствующий раку.
Как сигнальный узел переключается в режим производства жира
Чтобы понять, как UFL1 помогает опухолям, команда искала его молекулярных партнёров и обнаружила ключевой сигнальный белок AKT1. AKT1 — центральный переключатель, который приказывает клетке расти и синтезировать новые липиды. Исследование показывает, что UFL1 физически связывается с AKT1 и помечает его UFM1 в нескольких определённых местах. Эта модификация меняет конформацию AKT1, ослабляя внутренний «тормоз», который обычно удерживает его в неактивном состоянии. Она также способствует перемещению AKT1 в мембранный компартмент внутри клетки — эндоплазматический ретикулум, где другие ферменты могут полностью активировать его путём фосфорилирования. Без меток UFM1 в этих позициях AKT1 гораздо труднее активировать.
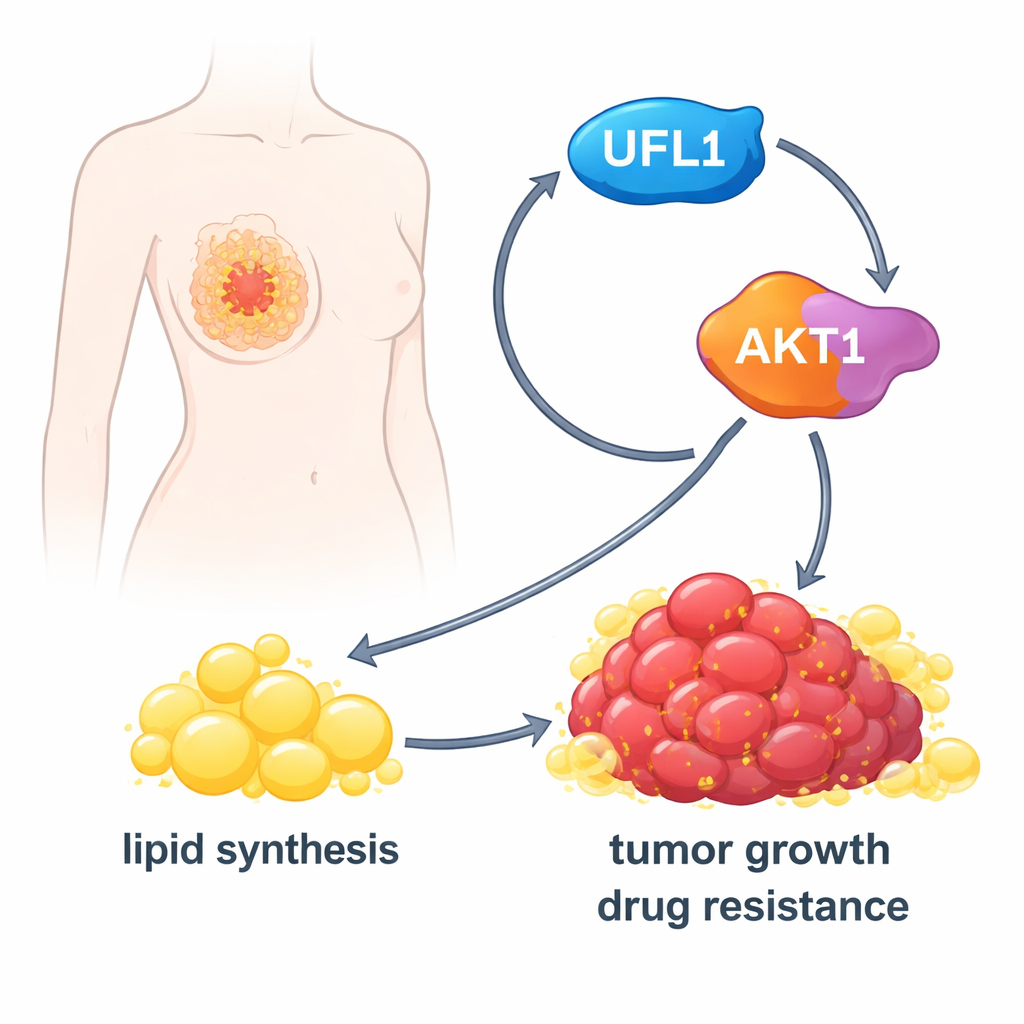
Включение фабрики жира в опухоли
Активированный AKT1 заставляет клетки наращивать синтез жиров. Он усиливает активность ключевого метаболического фермента ACLY и повышает уровни главных регуляторов, таких как SREBP1, которые включают множество генов, ответственных за липогенез. В культурах клеток рака молочной железы UFL1 вызывал накопление жировых капель, свободных жирных кислот и холестерина. Удаление UFL1 резко снижало эти запасы липидов как в культурах, так и в опухолях у мышей. Подкормка клеток внешними жирными кислотами во многом восстанавливала рост клеток, лишённых UFL1, что свидетельствует о том, что основная функция UFL1 — обеспечивать достаточный запас липидов для поддержания расширения опухоли.
Самоподдерживающаяся петля, стимулирующая рост опухоли
Удивительно, но связь между UFL1 и AKT1 двунаправленная. Исследователи обнаружили, что активированный AKT1, в свою очередь, фосфорилирует UFL1 в определённой позиции. Эта модификация ещё больше усиливает способность UFL1 помечать AKT1 UFM1, создавая положительную петлю обратной связи: UFL1 активирует AKT1, а AKT1 активирует UFL1. Мутация либо сайтов UFM1 на AKT1, либо фосфорилируемой позиции на UFL1 разрывает эту петлю. У мышей опухоли с такими мутантными вариантами росли хуже, содержали меньше липидов и демонстрировали больше погибающих клеток. В образцах пациентов с тройным отрицательным раком молочной железы более высокие уровни активированного UFL1 и активированного AKT1 часто встречались вместе, что подтверждает, что эта петля работает в реальных опухолях.
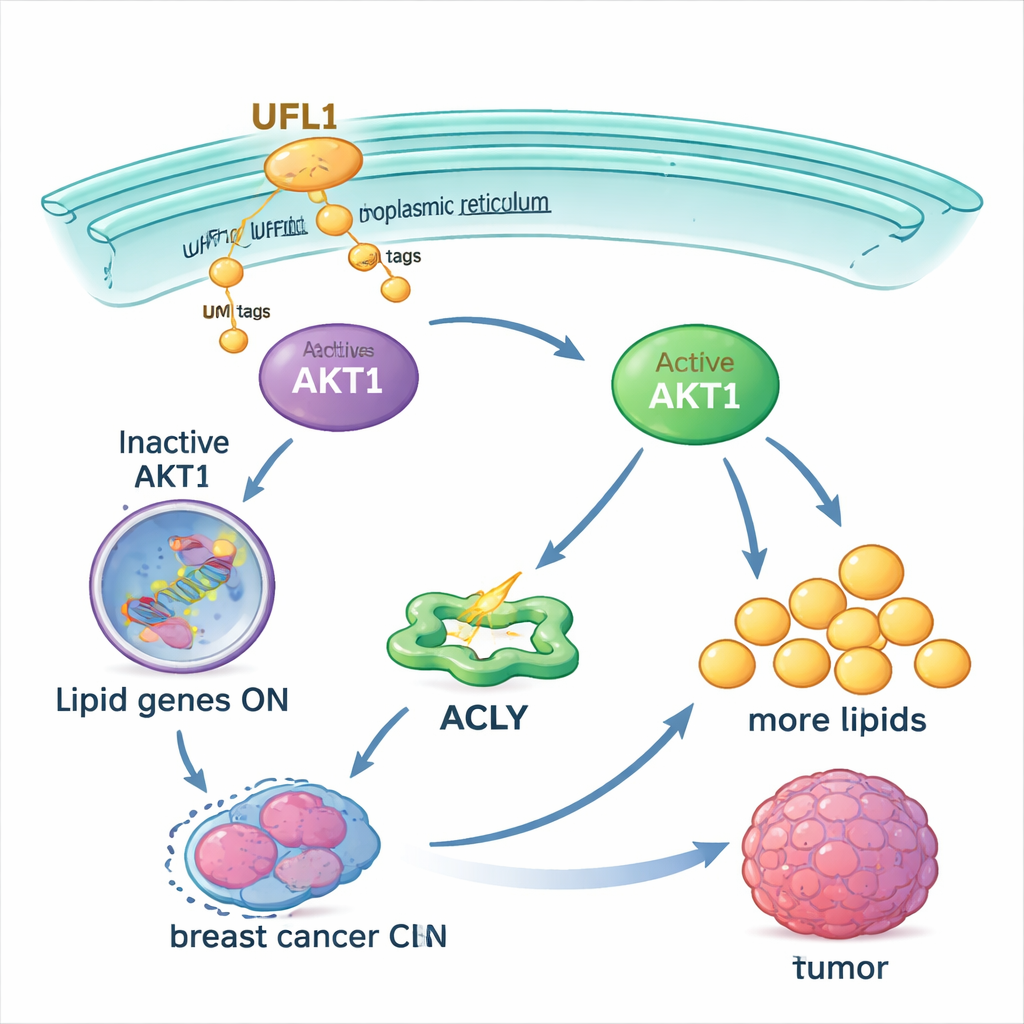
Ослабление петли для повышения эффективности лечения
Поскольку многие клинические исследования уже нацелены на AKT, авторы проверили, может ли блокирование UFMylation повысить эффективность таких лечений. В клетках рака молочной железы небольшой молекулярный ингибитор UFMylation и ингибитор AKT снижали активность AKT1 и накопление липидов, но их совместное применение работало значительно лучше, чем каждый из препаратов по отдельности. Комбинация также замедляла рост опухолей и сокращала содержание жиров в опухолях у мышей без заметной потери веса у животных. Блокада UFMylation дополнительно повышала чувствительность раковых клеток к стандартным химиотерапевтическим препаратам, таким как цисплатин и этопозид, которые часто оказываются неэффективны при высокой активности AKT.
Что это значит для пациентов
Для непрофессионального читателя исследование показывает, что определённые раки молочной железы настраивают себя с помощью самоподдерживающейся петли, которая подпитывает и их рост, и их жировой запас. UFL1 и AKT1 работают вместе, словно два нажимаемых одновременно педаля: один помечает, другой сигнализирует, и вместе они запускают синтез липидов и расширение опухоли. Поиск препаратов, мешающих этой петле — либо блокируя UFMylation, AKT1, либо их взаимодействие — может позволить в будущем замедлять рост опухолей и повышать эффективность существующих методов лечения, особенно при агрессивных типах рака молочной железы.
Цитирование: Meng, F., Du, Y., Liang, J. et al. The UFL1-AKT positive feedback loop promotes breast cancer progression by enhancing lipid synthesis. Nat Commun 17, 614 (2026). https://doi.org/10.1038/s41467-026-68492-3
Ключевые слова: рак молочной железы, липидный обмен, сигнализация AKT, UFMylation, таргетная терапия