Clear Sky Science · ru
Масштабная визуализация кислотности, обусловленной протонными насосами, для оценки прогрессирования и метастазирования опухолей
Почему кислотность опухоли важна
Рак не развивается в изоляции. Опухолевые клетки перестраивают свое окружение, создавая суровую, кислую «среду», которая помогает им распространяться и сопротивляться лечению. В этой работе сосредоточены на раке печени и показано, что измерение этой кислотности в живой ткани позволяет выявлять опухоли раньше, отслеживать их эволюцию и даже направлять новые терапевтические стратегии, нацеленные как на сами раковые клетки, так и на кислую среду, которую они создают.
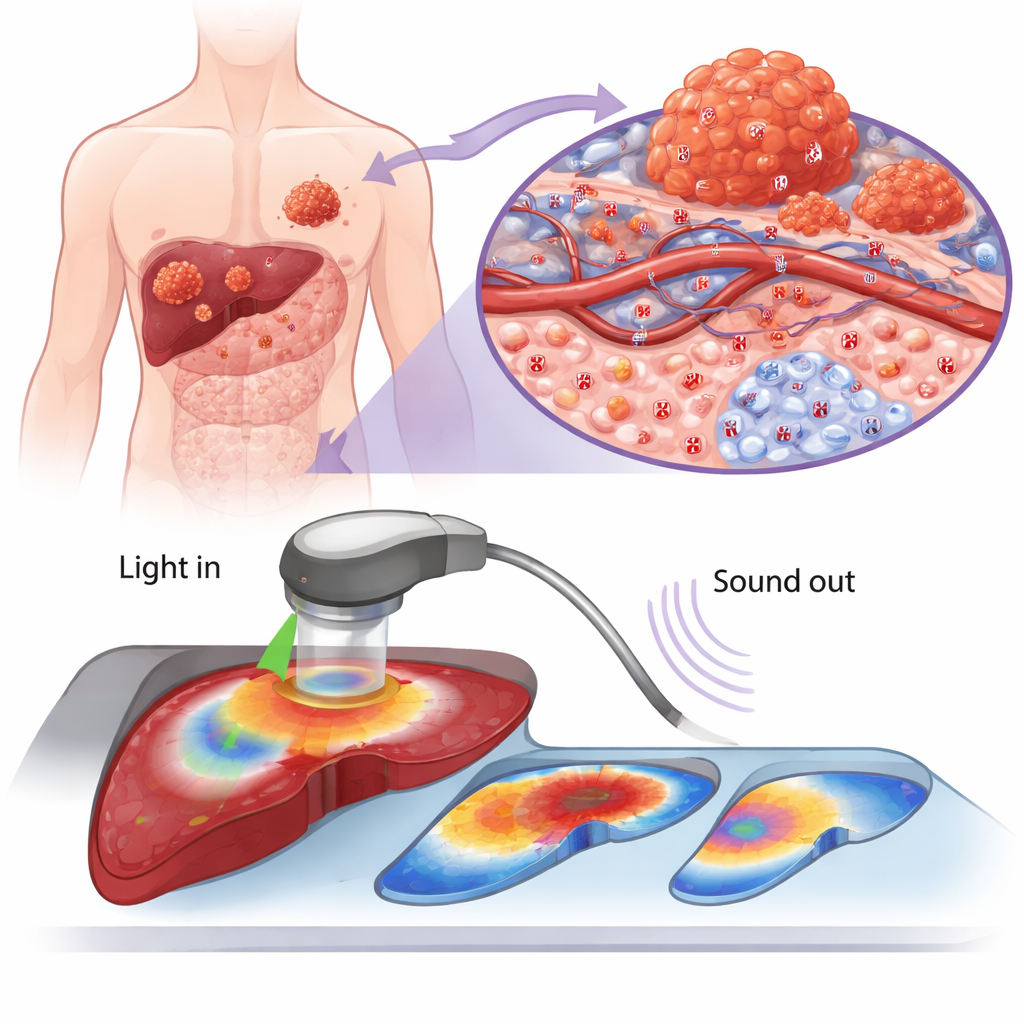
Скрытый химический признак рака
Многие опухоли, включая гепатоцеллюлярную карциному (распространённый рак печени), зависят от обмена веществ, усиленно потребляющего сахар и производящего избыток кислоты. Раковые клетки используют протонные насосы в мембранах, чтобы выталкивать эти лишние ионы водорода (H+), делая пространство вокруг опухоли более кислым, чем нормальная ткань. Авторы выделяют один из компонентов такого насоса, ATP6V0C, как особенно важный. В больших наборах данных пациентов и в реальных опухолевых образцах уровни ATP6V0C были выше в тканях печени с опухолью по сравнению с прилежащей здоровой тканью, повышались по мере прогрессирования рака и ассоциировались с худшей выживаемостью. Это указывает на то, что производство кислоты, управляемое ATP6V0C, является не просто побочным эффектом рака, а фактором, стимулирующим рост, инвазию и метастазирование.
Преобразование кислотности в изображение
Чтобы сделать это невидимое химическое изменение видимым для врачей, команда создала крошечный датчик под названием PPS (рН-чувствительный фотоакустический сенсор). PPS состоит из проводящего полимера, который меняет свои оптические свойства в зависимости от кислотности. В нейтральных условиях PPS относительно «тих»; в кислой среде, подобной той, что окружает опухоли, он меняет структуру и сильно поглощает ближний инфракрасный свет. Когда импульсный свет попадает на PPS, он кратковременно нагревается и расширяется, создавая ультразвуковые волны, улавливаемые вне тела. Измеряя сигналы на двух длинах волн и вычисляя их отношение, исследователи создали карту кислотности, которая одновременно чувствительна и меньше подвержена фоновому шуму.
Наблюдение за эволюцией опухолей в живой ткани
Используя этот сенсор у мышей, авторы отслеживали, как опухоли печени кислотообразуют свое микроокружение со временем. Даже когда опухоли были слишком малы, чтобы их можно было заметить невооруженным глазом, фотоакустическая визуализация на основе PPS фиксировала постепенное снижение местного pH по мере размножения раковых клеток, искажения кровеносных сосудов и падения уровня кислорода. В моделях как имплантированных опухолей печени, так и метастазов в печени от рака поджелудочной железы PPS выделял кислые участки, которые соответствовали местоположению опухолей на стандартных изображениях и в гистологических срезах. Тот же подход позволял отличать доброкачественные лимфатические узлы от метастатических в мышиной модели и четко очерчивал границы человеческих опухолей печени в хирургических образцах, что намекает на возможное будущее применение для помощи хирургам при полном удалении злокачественной ткани.
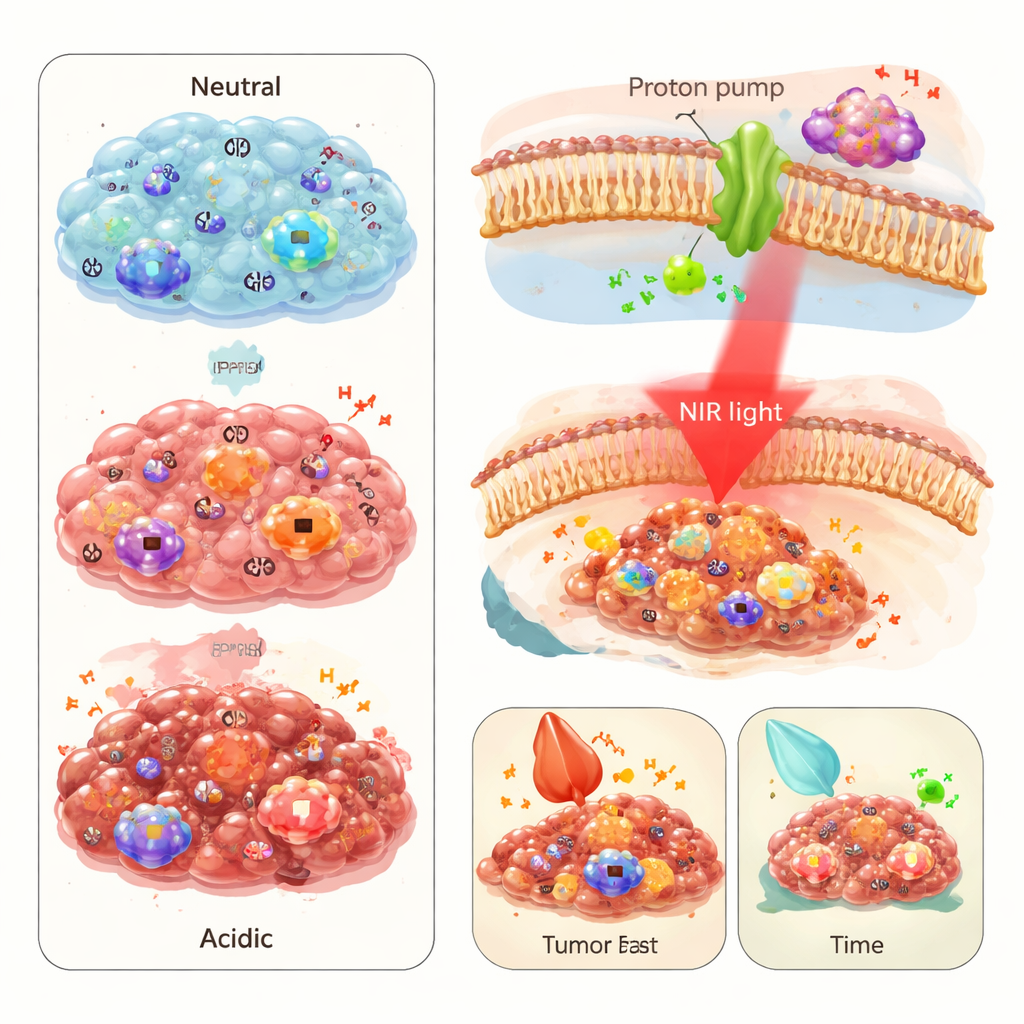
Блокирование кислотных насосов и «подогрев» опухолей изнутри
Исследование выходит за рамки визуализации и проверяет, как вмешательство в протонную откачку может замедлить рак. Исследователи показали, что эзомепразол, широко используемый блокатор кислотности для желудочных заболеваний, может связываться с ATP6V0C, снижать его активность в клетках рака печени и временно делать опухолевую среду у мышей менее кислой. Раковые клетки, подвергшиеся действию этого препарата, становились менее подвижными и менее способными к инвазии. В то же время сам PPS ведет себя как крошечный нагреватель в кислой среде: при облучении ближним инфракрасным светом он сильнее нагревается в кислых опухолях, чем в нормальной ткани, повреждая соседние раковые клетки. В моделях на мышах комбинированная терапия фототермически активированным PPS и эзомепразолом приводила к более заметному сокращению опухолей, чем любая из этих методик по отдельности.
Значение для будущей онкологической помощи
Для неспециалистов ключевое сообщение таково: кислотность — ранний и практически применимый сигнал активности рака. Эта работа демонстрирует, что теперь возможно картировать эту кислотность в живой ткани с высоким разрешением, отслеживать её изменения по мере роста опухолей или ответа на терапию и разрабатывать методы лечения, активируемые той самой кислотностью, которая делает опухоли опасными. Хотя методы все ещё находятся на экспериментальной стадии и сосредоточены на раке печени, подход визуализации и нацеливания на «кислую почву», питающую опухоли, в перспективе может помочь обнаруживать рак раньше, точнее планировать операции и оптимизировать комбинации лекарств для лучших исходов.
Цитирование: Zeng, S., Chen, J., Ren, Y. et al. Multiscale imaging on proton pump-driven acidity for assessing tumor progression and metastasis. Nat Commun 17, 1785 (2026). https://doi.org/10.1038/s41467-026-68491-4
Ключевые слова: микроокружение опухоли, рак печени, фотоакустическая визуализация, кислотность опухоли, ингибиторы протонных насосов