Clear Sky Science · ru
Самосборный гидрогель-резервуар клеток in situ для управления многоступенчатой радиоиммунотерапией
Превращение радиации в более продвинутое оружие против рака
Лучевая терапия — одно из наиболее широко используемых методов лечения рака, но опухоли часто выживают, скрываясь от иммунной системы и развиваясь в условиях низкого кислородного снабжения (гипоксии), что снижает эффективность облучения. В этом исследовании описан инъецируемый «умный» гидрогель, который формируется прямо внутри опухоли и действует как миниатюрная фабрика лекарств и генератор кислорода. Подавая к опухоли одновременно радиацию и точно скоординированные иммунно-стимулирующие сигналы, система нацелена на то, чтобы превратить трудноизлечимую опухоль в структуру, которую собственные защитные силы организма смогут распознать и уничтожить.
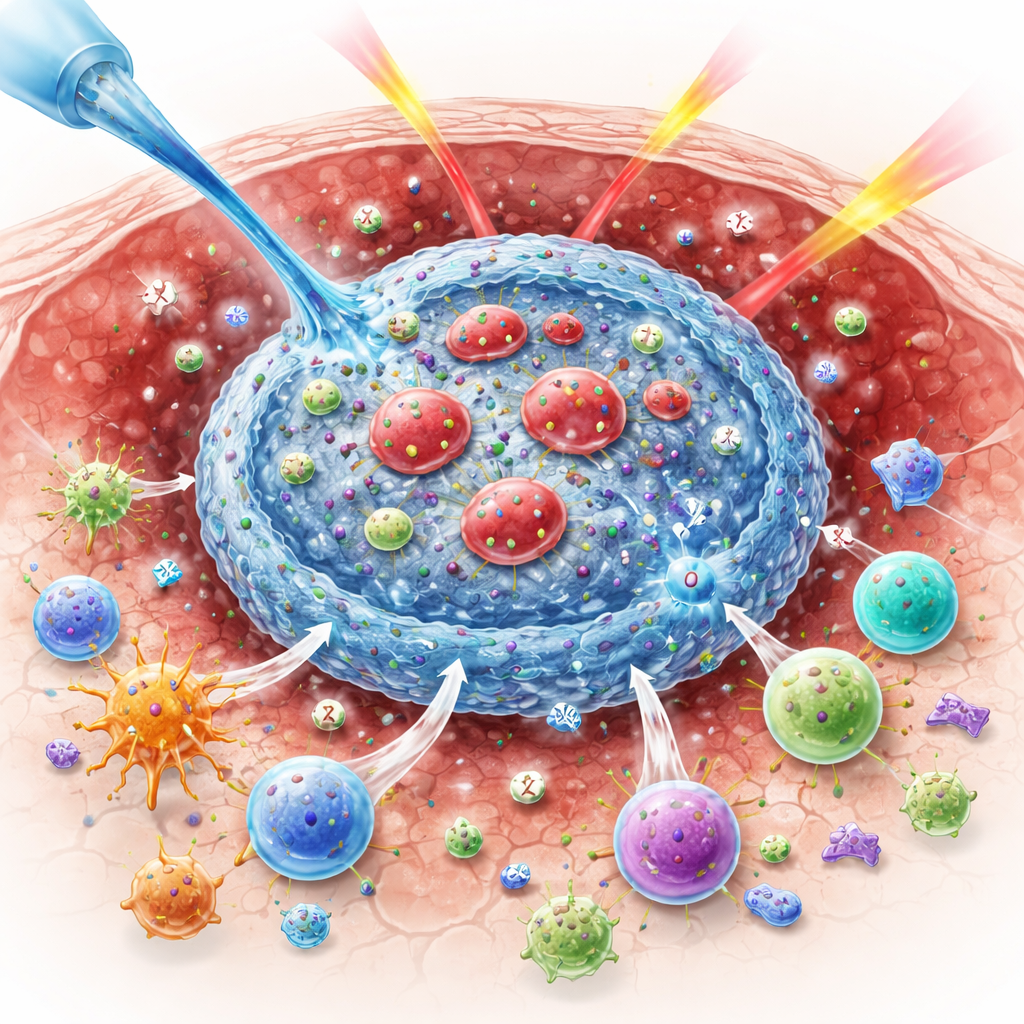
Почему кислород важен для борьбы с опухолями
Радиация убивает раковые клетки отчасти за счёт образования высокореактивных кислородсодержащих молекул, разрушающих ДНК. Когда опухоли лишены кислорода, эта химия работает хуже, и больше раковых клеток выживает. Одновременно радиация посылает иммунной системе смешанные сигналы. Она может обнажать опухолевые белки, помечая рак как опасность, но также усиливать «тормоза» на иммунных клетках — например, контрольный белок CTLA-4 — и способствовать активности регуляторных Т-клеток, подавляющих атаку. Эти противоположные эффекты помогают объяснить, почему сочетание облучения с иммунными препаратами не всегда приносило в клинике такие же результаты, как в опытах на мышах.
Живой гель, сформированный внутри опухоли
Исследователи разработали материал, который самособирается только в кислой среде опухоли. Он состоит из трёх ключевых компонентов: природного полимера на основе сахаров — альгината, неорганического порошка пероксида бария и эритроцитов, мягко модифицированных для доставки двух иммунных препаратов. При инъекции в опухоль кислотные условия вызывают разложение пероксида бария с выделением ионов бария и перекиси водорода. Ионы бария мгновенно сшивают альгинат в мягкий гидрогель, запирая модифицированные эритроциты на месте и предотвращая вымывание препаратов. Одновременно ферменты, естественно присутствующие в эритроцитах, преобразуют перекись водорода в кислород, помогая снизить гипоксию опухоли и подготовить её к более эффективному облучению.
Тайминг — ключ к двойному иммунному сигналу
Настоящая сила системы заключается в том, как она расслаивает высвобождение двух иммунных агентов: антитела, блокирующего CTLA-4, и цитокина интерлейкина-12 (IL-12). Антитело загружено внутрь эритроцитов, тогда как IL-12 закреплён на их поверхности. По мере генерации кислорода в мембране эритроцитов образуются поры, что позволяет антителу против CTLA-4 быстро выйти наружу. Этот ранний выброс снимает иммунное подавление, стимулирует дендритные клетки переносить опухолевые антигены в ближайшие лимфоузлы и способствует активации их-специфичных Т-клеток. IL-12, напротив, просачивается медленно по мере постепенного ослабления структуры гидрогеля. Поздний сигнал побуждает Т-клетки и натуральные киллеры вырабатывать интерферон-γ, усиливает приток убийственных иммунных клеток в опухоль и укрепляет положительную обратную связь между сенсорами иммунной системы и эффекторными клетками.
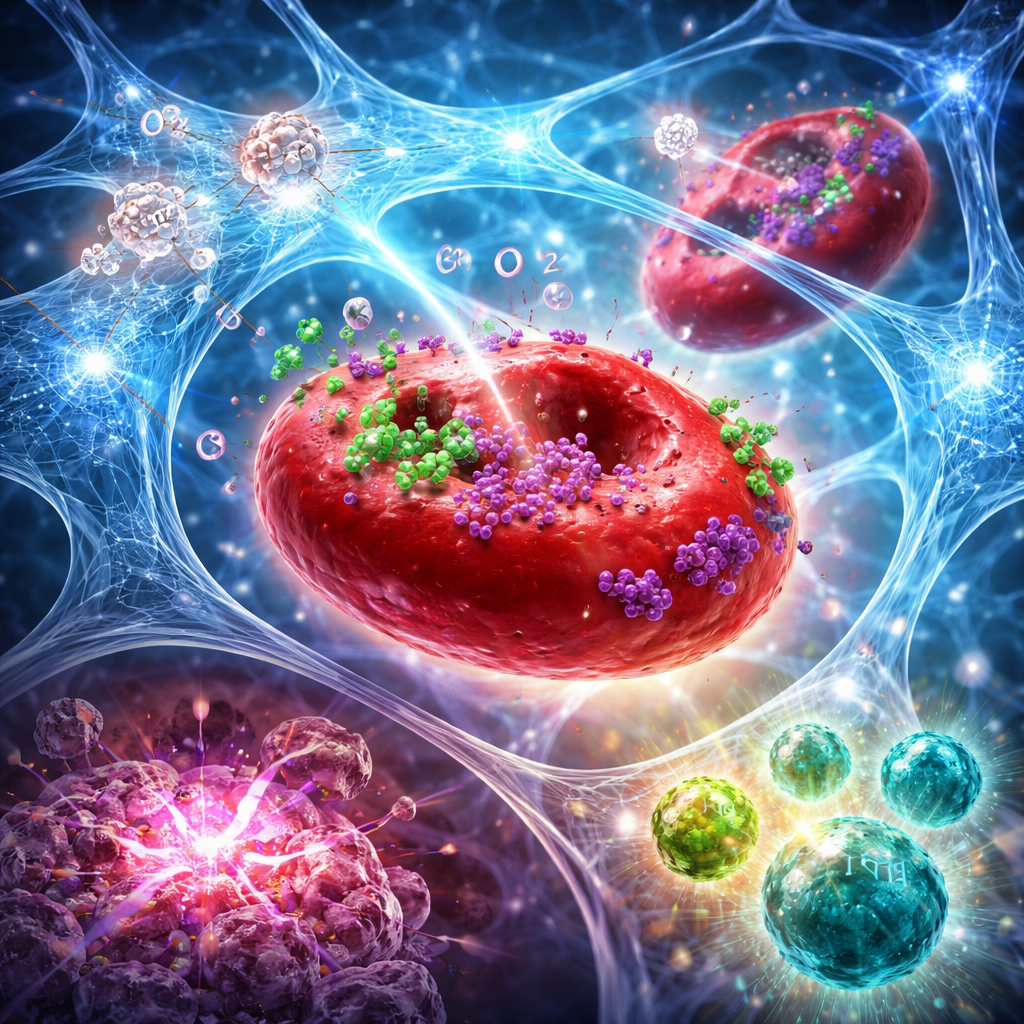
От локальной инъекции к системной иммунной атаке
В моделях агрессивных раков молочной и поджелудочной желез головы у мышей сочетание этого гидрогеля с фокусированным облучением делало не только местное сокращение леченой опухоли. Комбинация повышала уровень кислорода в опухолях на протяжении нескольких дней, усиливала радиационно-индуцированные повреждения ДНК и запускала более выраженную форму клеточной гибели, которая естественно помечает опухоль для иммунного распознавания. Поточная цитометрия и окрашивание тканей показали заметный сдвиг в микроокружении опухоли: больше цитотоксических CD8+ Т-клеток и натуральных киллеров, меньше регуляторных Т-клеток и более высокий баланс «эффекторных» к «супрессивным» клеткам. Специализированные дендритные клетки в лимфоузлах тоже увеличились, что указывает на улучшенное представление антигенов. У многих мышей наблюдалась полная регрессия опухоли, а у некоторых появлялась защита от повторного роста при повторном введении раковых клеток спустя недели, что свидетельствует о формировании стойкой иммунной памяти.
Безопасность, практичность и направления развития
Поскольку гель формируется локально и удерживает свой груз, лишь небольшие количества IL-12 и анти-CTLA-4 попадают в кровоток, что снижает риск серьёзных побочных эффектов, таких как цитокиновый шторм или повреждение органов, ограничивавшие применение этих агентов ранее. Компоненты — альгинат, эритроциты и пероксид бария — относительно недорогие и масштабируемые, что повышает надежду на адаптацию этой стратегии для разных типов рака. Хотя остаются трудности в производстве, контроле качества и доставке геля в глубокие или широко распространённые опухоли, работа демонстрирует перспективный способ синхронизировать радиацию с точно дозированными иммунными сигналами, превращая физическое лечение рака в мощный триггер для системного антитуморного иммунитета.
Что это может значить для пациентов
Проще говоря, это исследование предлагает вместо раздельного введения облучения и иммунных препаратов и надежды на их совместную работу упаковывать их в «умный» материал, который находится внутри опухоли, вырабатывает собственный кислород и выпускает иммунные сигналы по тщательно срежессированному сценарию. На животных такой подход не только делал радиацию более губительной для раковых клеток, но и обучал иммунную систему распознавать и запоминать опухоль, помогая предотвратить её возвращение. Если в людях удастся получить похожие результаты, такие гидрогели могут со временем превратить трудноизлечимые опухоли в цели, которые собственные защитные силы организма смогут надёжно находить и уничтожать.
Цитирование: Chen, Y., Chen, Q., Ma, Y. et al. In situ self-assembled cell reservoir hydrogel for maneuvering multistage radioimmunotherapy. Nat Commun 17, 1784 (2026). https://doi.org/10.1038/s41467-026-68490-5
Ключевые слова: радиоиммунотерапия, гидрогель, иммунотерапия рака, микроокружение опухоли, радиотерапия