Clear Sky Science · ru
Непрерывно настраиваемая мультистабильность в сетях расщепления ДНК
От простых переключателей к множеству возможных состояний
Биологические системы — от делящихся клеток до развивающихся зародышей — редко работают как простые выключатели «вкл/выкл». Чаще они удерживают множество устойчивых состояний, скорее как диммер, который можно поставить в бесчисленное число положений. В этой работе описана химическая сеть на основе ДНК, которая ведёт себя именно как такой диммер: она может стабильно поддерживать не просто несколько отдельных состояний, а практически любую комбинацию вдоль непрерывного спектра. Такая способность может стать мощной основой для будущих «умных» материалов, молекулярных запоминающих устройств и биохимических компьютеров, обрабатывающих аналоговую, а не только цифровую информацию.
Почему важна множественная устойчивость
Многие клеточные решения — станет ли стволовая клетка зрелой, запустит ли клетка программу самоуничтожения или запомнит ли генетическая сеть прошлый сигнал — зависят от «мультистабильности», то есть способности находиться в более чем одном устойчивом режиме при тех же условиях. Традиционные синтетические реализации таких систем строились на генетических схемах, ферментах или нитях ДНК, которые включают и выключают друг друга. Эти конструкции обычно дают ограниченное число дискретных исходов, как в классических бистабильных переключателях с двумя устойчивыми состояниями. Масштабирование такой идеи сложно: для системы из N состояний обычно требуется порядка N×(N−1) тщательно настроенных ингибирующих связей, и при этом система всё равно скачет лишь между немногими фиксированными точками, а не образует плавный континуум вариантов.
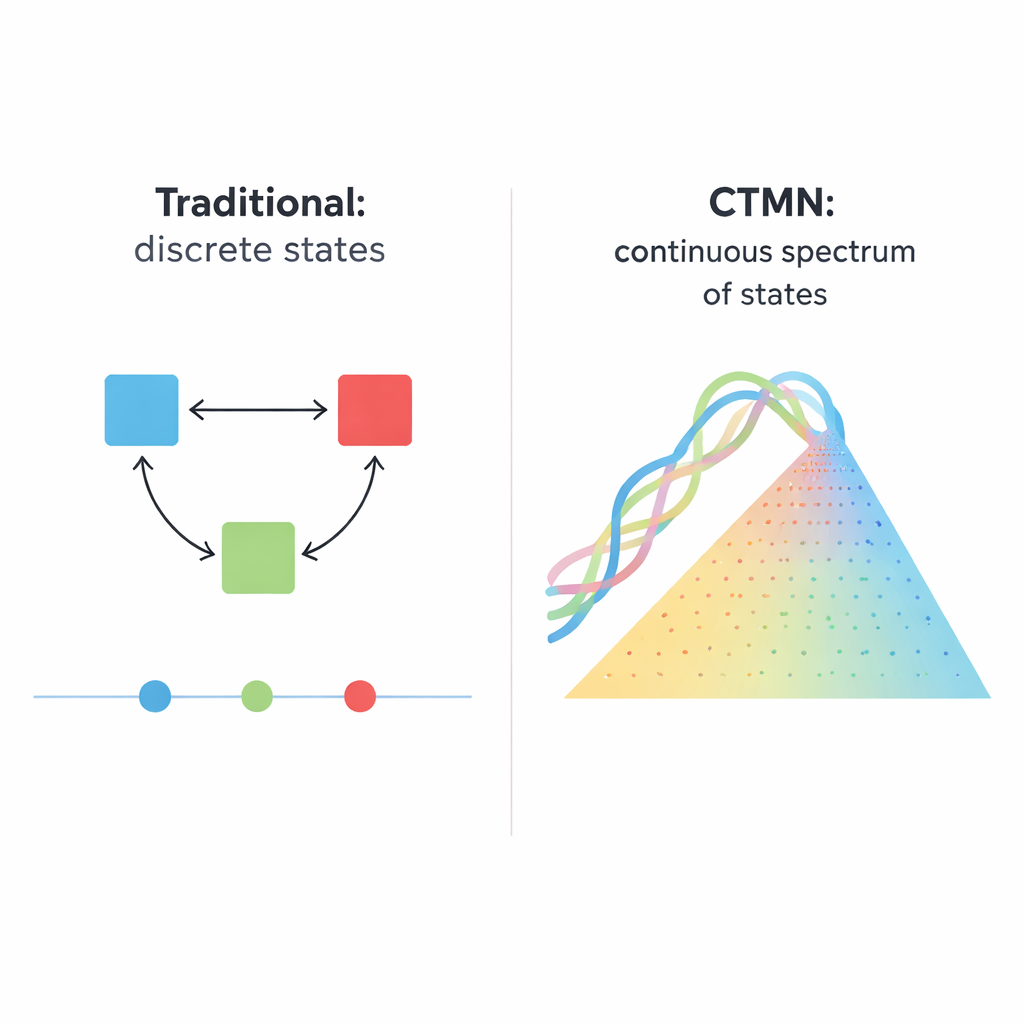
Новый тип сети ДНК: непрерывно настраиваемая
Авторы предлагают иной принцип проектирования, реализованный в так называемых сетях непрерывно настраиваемой мультистабильности (CTMN). Вместо опоры на множество отдельных ингибирующих сигналов они используют прямую конкуренцию между модулями репликации ДНК, соединёнными обратимыми реакциями обмена нитями. Каждый модуль состоит из дизайнерских дуплексов ДНК, которые могут участвовать в замещении нитей и одновременно служить матрицами для ДНК‑полимеразы, при участии никейз‑фермента, разрезающего и регенерирующего ключевые сегменты. Химическое топливо — нуклеотидные строительные блоки dNTP — обеспечивает непрерывную полимеразацию и никование, поддерживая систему далеко от равновесия. При этих условиях конкурирующие модули фактически «замораживаются» в тех относительных долях, с которыми они стартовали, давая не просто пару исходов, а целую непрерывную линию (или, для большего числа модулей, плоскость) долго живущих состояний.
Как молекулярный механизм фиксирует память
В самом простом двухмодульном варианте CTMN‑1 команда демонстрирует экспериментально и с помощью подробного кинетического моделирования, что система может устанавливать семейство стабильных смесей, охватывающих почти весь диапазон от «в основном модуль A» до «в основном модуль B». Полимеразация преобразует активные дуплексы в удлинённые формы, временно выведенные из конкуренции по обмену нитями; никование затем восстанавливает их, замыкая авторегуляторную петлю. Когда оба модуля разделяют эту петлю, они настолько подавляют взаимное превращение, что система остаётся закреплённой близко к исходному составу в течение многих часов при наличии топлива. Линейный анализ устойчивости лежащих в основе уравнений выявляет целое многообразие — фактически континуум — стационарных состояний, в отличие от единственной фиксированной точки, наблюдаемой при удалении ферментов или топлива.
Программируемые ответы и молекулярная память
Поскольку состояние сети хранится в составах ДНК, им можно управлять и считывать программируемыми способами. Авторы разрабатывают короткие РНК «триггеры», которые временно связываются с определёнными нитями ДНК, смещая конкуренцию и переводя сеть в новый состав. Даже после деградации РНК ферментом новое состояние сохраняется, функционируя как форма молекулярной памяти. Повторные или более сильные стимулы плавно смещают систему вдоль континуума состояний, а не просто переключают её между простыми положениями вкл/выкл. Более того, сами продукты репликации ДНК можно настроить так, чтобы они служили сигналами для последующих процессов: в демонстрациях разные состояния CTMN‑1 селективно активируют один из двух ДНК‑катализаторов или смещают транскрипцию РНК в сторону одного из двух матричных молекул, не нарушая при этом основной мультистабильности.
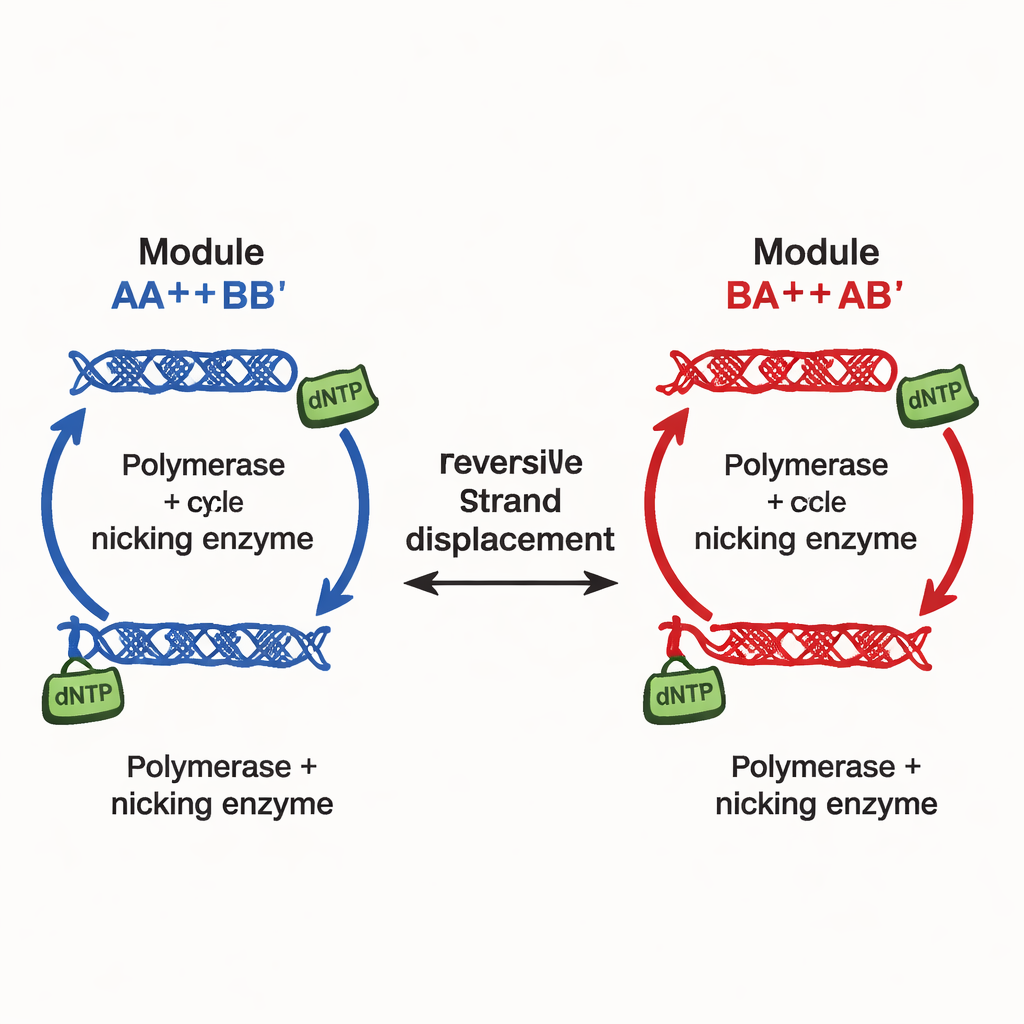
Масштабирование до сложных молекулярных «диммеров»
Чтобы показать, что стратегия масштабируема, исследователи построили трёхмодульную сеть CTMN‑2, добавив ещё разработанные дуплексы ДНК, которые разделяют общий домен обмена, но кодируют разные репликационные матрицы. Теперь возможные стационарные состояния заполняют двумерную область, как точки на треугольной фазовой диаграмме, а не выстраиваются вдоль простой линии. Эксперименты снова подтверждают, что многие различные композиции остаются стабильными при наличии топлива и ферментов, и что все они сворачиваются в единую точку равновесия при удалении источника энергии. Поскольку добавление новых модулей требует лишь новых конструкций ДНК, подключаемых в ту же схему замещения, общая сложность проводки не раздувается так, как в традиционных подходах.
Что это значит для будущих молекулярных технологий
Для неспециалиста основная мысль такова: авторы превратили сеть репликации ДНК в чрезвычайно гибкое аналоговое запоминающее устройство. Вместо выбора среди нескольких заранее заданных вариантов их система может надёжно удерживать одно из десятков экспериментально различимых состояний, каждое определяемое относительным содержанием каждого ДНК‑модуля, и преобразовывать кратковременные химические импульсы в долгоживущие сдвиги вдоль этого континуума. Поскольку выходные ДНК‑нити программируемы и отделены от механизма стабилизации, та же платформа, по сути, может регулировать широкий спектр последующих биохимических реакций или свойств материалов с тонким градуированным контролем. Эта работа указывает на молекулярные устройства, которые вычисляют, запоминают и адаптируются скорее как нейронные или механические аналоговые системы, нежели как простые цифровые переключатели.
Цитирование: Zhong, R., Fu, Y., Jiang, S. et al. Continuously tunable multistability in DNA replication networks. Nat Commun 17, 1782 (2026). https://doi.org/10.1038/s41467-026-68488-z
Ключевые слова: мультистабильность ДНК, молекулярная память, синтетические биохимические сети, замещение нитей ДНК, аналоговые молекулярные вычисления