Clear Sky Science · ru
Надёжное и интерпретируемое прогнозирование генетических маркёров и типов клеток по данным пространственной транскриптомики
Преобразование обычных срезов ткани в молекулярные карты
Когда берут биопсию, врачи обычно видят лишь то, что показывают микроскоп: формы и рисунки клеток в розово-фиолетовых окрасках. Однако под этими цветами скрывается мир генов, которые включаются и выключаются, влияя на то, как растёт рак и как он реагирует на лечение. В этом исследовании представлена STimage — новая система искусственного интеллекта (ИИ), которая стремится читать этот молекулярный сценарий прямо со стандартных патоморфологических изображений, потенциально предоставляя более быстрые и дешёвые сведения без дополнительных лабораторных тестов.
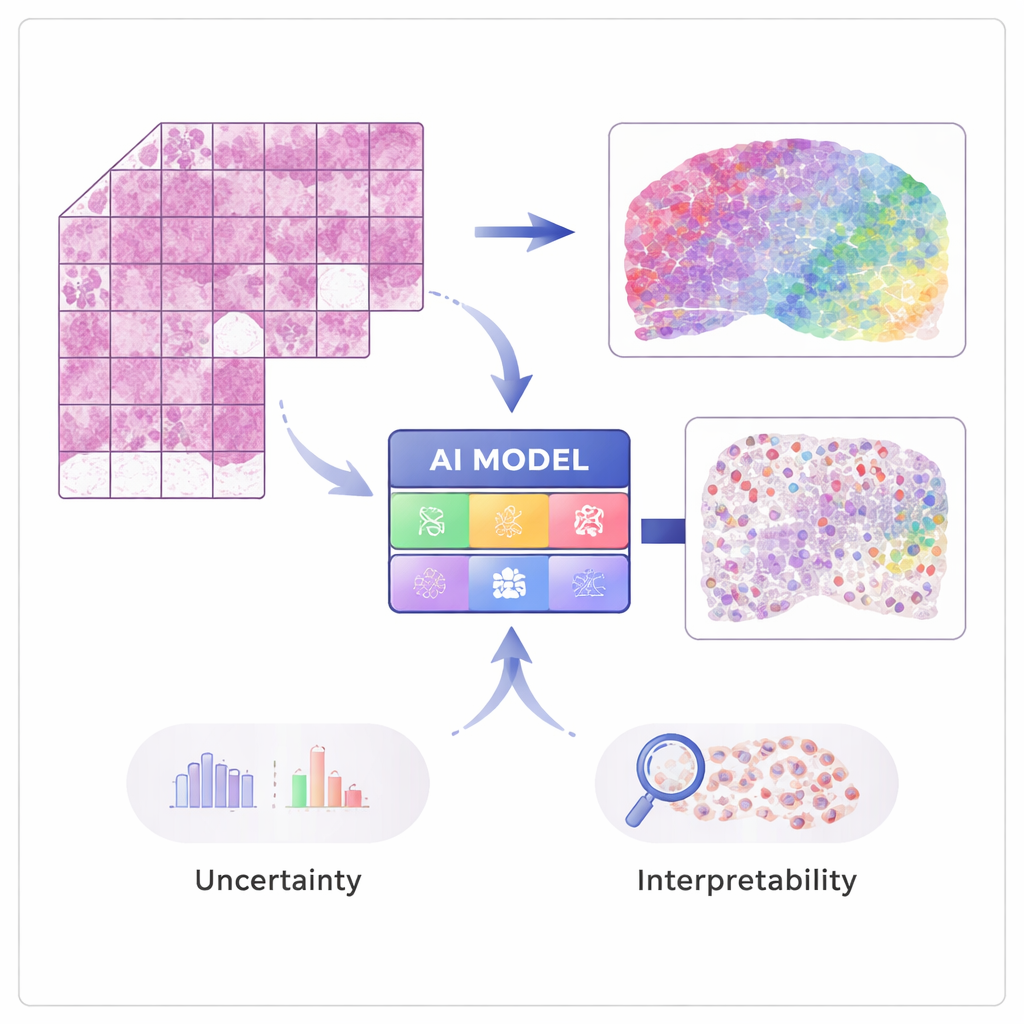
От изображений к активности генов
Современные методы «пространственной транскриптомики» позволяют измерять активность десятков тысяч генов с сохранением их пространственной привязки в ткани. Эти подходы мощны, но дороги и ещё не стали рутинными в больницах. STimage обучали на ограниченном числе таких пространственных наборов данных, где каждое изображение ткани сопоставлено с подробными измерениями экспрессии генов в множестве крошечных точек. ИИ учится связывать локальные визуальные паттерны на гистологическом препарате с гематоксилином и эозином (H&E) — например, плотность или неправильность формы ядер — с лежащей в их основе генетической активностью, чтобы затем уметь предсказывать экспрессию генов и типы клеток по обычным изображениям.
Построение более надёжного и интерпретируемого ИИ-патолога
Ключевая цель работы — не только точность, но и надёжность и объяснимость. Вместо выдачи одного числа для каждого гена STimage прогнозирует полное вероятностное распределение, описывающее вероятный диапазон активности гена в каждой точке. Система также разделяет два вида неопределённости: одну, вызванную шумом или вариабельностью данных, и другую, отражающую собственное незнание модели. Обучая множество слегка отличающихся версий модели и усредняя их — так называемый ансамблевый подход — исследователи одновременно повышают производительность и получают более ясное представление о том, где система уверена, а где — нет, что критично для клинических решений.
Тестирование на разных видах рака, технологиях и в разных больницах
Команда оценивала STimage на разнообразных наборах данных по раку молочной железы, кожи и почки, а также на образцах с иммунно-связанным заболеванием печени. Система научилась предсказывать важные онкологические и иммунные маркёры, часто соответствующие истинным пространственным паттернам, наблюдавшимся в независимых экспериментах. Модель сохраняла работоспособность при проверке на данных из разных лабораторий, при различных методах подготовки образцов и даже при использовании различных базовых технологий, включая платформы с разрешением до отдельных клеток и более старые, низкоразрешающие системы. В очных сравнениях с несколькими существующими ИИ-инструментами STimage и её ансамблевые варианты обычно оказывались впереди, особенно когда оценивали, насколько предсказанные паттерны совпадают с реальным распределением активности генов по ткани.
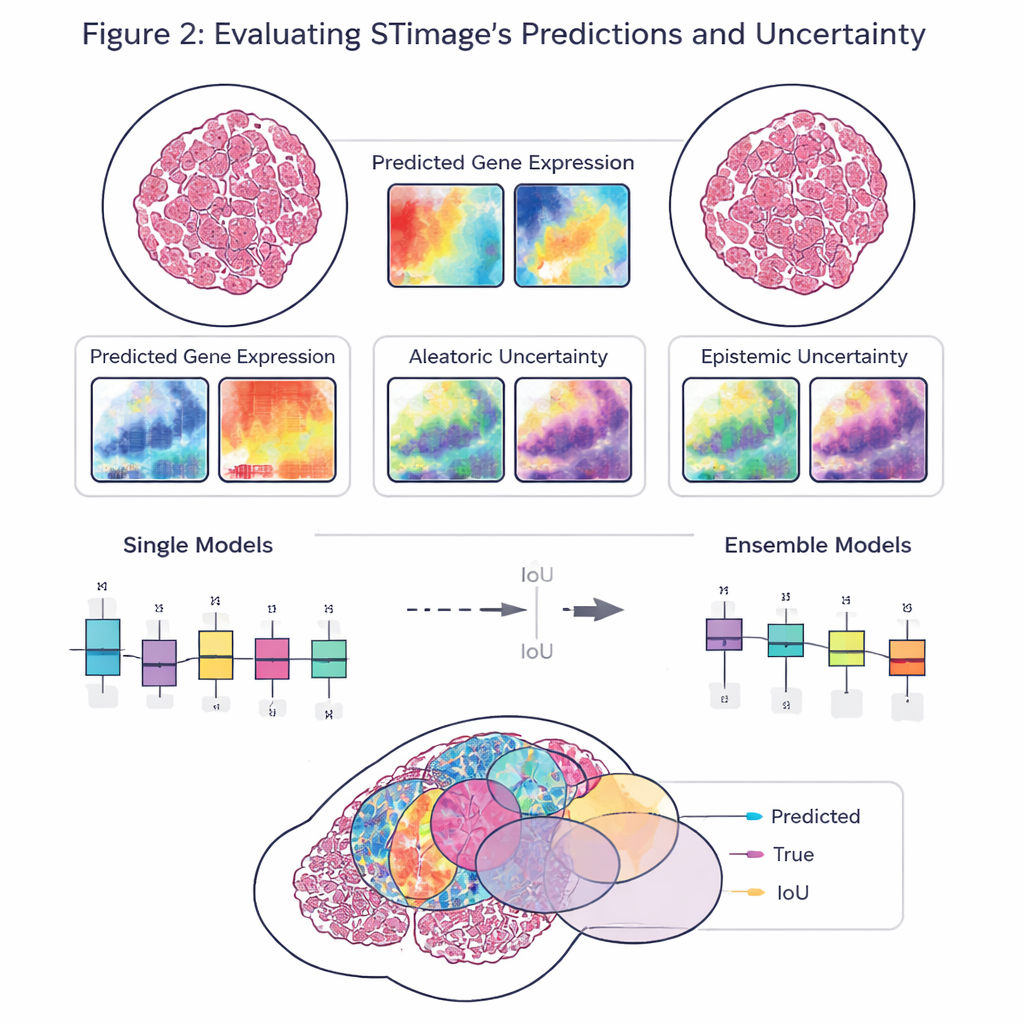
Взгляд внутрь опухолей: клетки, выживаемость и ответ на препараты
STimage выходит за рамки прогнозирования генов и делает выводы о том, какие типы клеток занимают каждую область, используя высокоразрешающие наборы данных, где идентичность каждой клетки известна. Модель умела различать раковые клетки, иммунные клетки и клетки-опорные компоненты и отображать их расположение на срезе. Авторы затем применили STimage к большим коллекциям рутинных изображений опухолей из The Cancer Genome Atlas. Даже без пространственных измерений предсказанные ИИ профили экспрессии генов тесно коррелировали с реальными совокупными (bulk) генетическими данными. Эти предсказания были достаточно информативны, чтобы разделять пациентов на группы с более высоким и более низким риском и помогать выделять тех, у кого выше вероятность полного ответа на определённые терапии при раке молочной железы.
Почему это важно для будущих пациентов
Для пациентов и клиницистов обещание STimage — это своего рода «молекулярный наложение» на привычный патоморфологический слайд. Вместо назначения множества дорогостоящих тестов один отсканированный срез однажды может показать, где активны агрессивные генетические программы, как распределены иммунные клетки и какие маркёры указывают на более благоприятный или неблагоприятный прогноз или на различную чувствительность к лекарствам. Хотя метод всё ещё дорабатывается и корреляции с истинными измерениями не идеальны, его способность улавливать пространственные паттерны, оценивать собственную неопределённость и выделять клетки, формирующие его предсказания, делает его практичным шагом к более информативной и прозрачной цифровой патологии.
Цитирование: Tan, X., Mulay, O., Xie, J. et al. Robust and interpretable prediction of gene markers and cell types from spatial transcriptomics data. Nat Commun 17, 1781 (2026). https://doi.org/10.1038/s41467-026-68487-0
Ключевые слова: цифровая патология, пространственная транскриптомика, онкологические биомаркеры, глубокое обучение, микроокружение опухоли