Clear Sky Science · ru
PTRAMP, CSS и Ripr образуют сохраняющийся комплекс, необходимый для инвазии мерозоитов Plasmodium в эритроциты
Почему это важно для борьбы с малярией
Паразиты малярии должны проникнуть внутрь наших красных кровяных клеток, чтобы вызвать болезнь. В этом исследовании обнаружен небольшой набор белков, которые образуют общий «путевой мост», используемый несколькими основными видами малярии, включая те, что поражают людей. Раскрывая, как этот мост собирается и как антитела иногда могут блокировать его, работа указывает на новые подходы к созданию вакцин, которые могли бы защищать от более чем одного типа малярии одновременно. 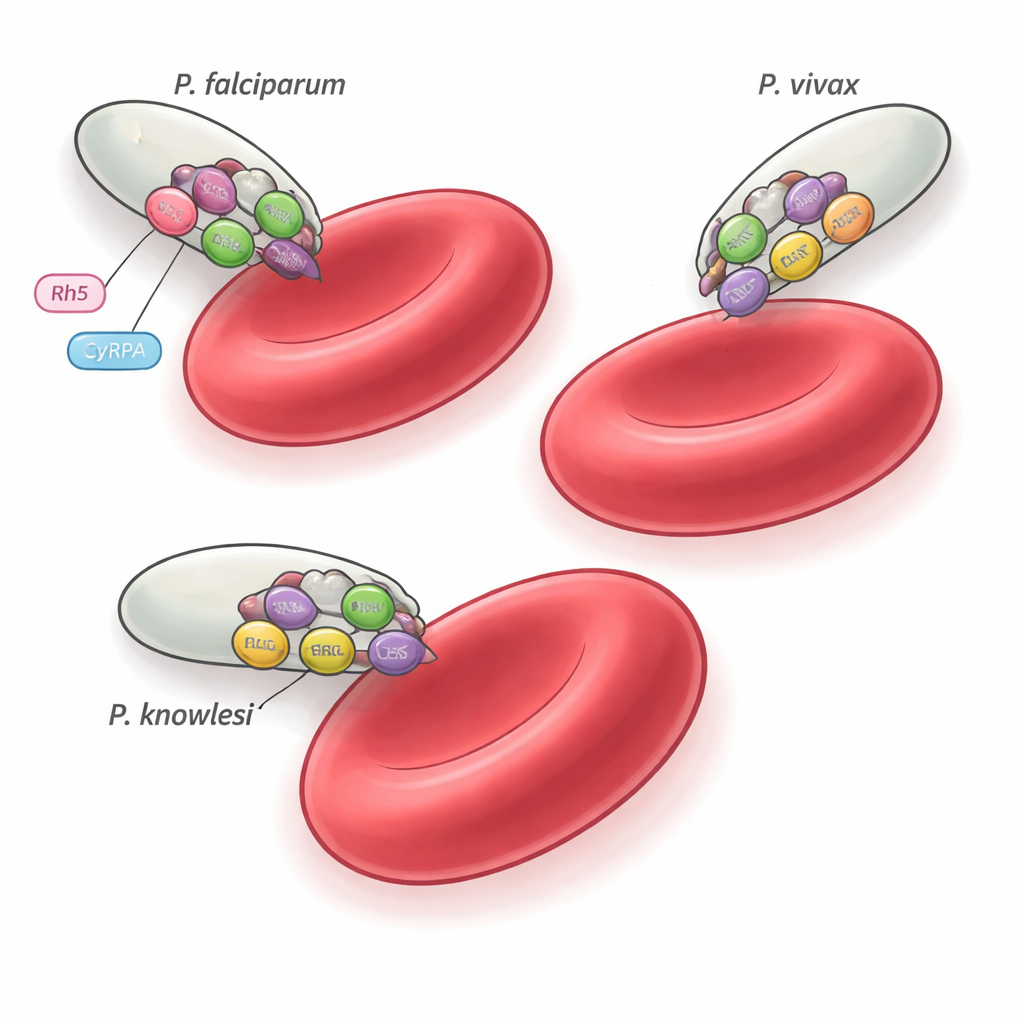
Общий набор инструментов у многих паразитов малярии
Существует более 200 видов Plasmodium, но лишь немногие, такие как P. falciparum, P. vivax и P. knowlesi, инфицируют человека. Эти виды расположены на разных ветвях родословного дерева паразитов и предпочитают разные типы эритроцитов, но всем им требуется точный механизм инвазии. Ранее в P. falciparum был выявлен пятикомпонентный ансамбль — комплекс PCRCR, необходимый для инвазии, который связывается с рецептором на человеческих эритроцитах, называемым базигином. Одна часть этого комплекса, белок Rh5, уникальна для P. falciparum и его близких родственников, что породило вопрос: что используют другие виды малярии вместо него? Настоящее исследование сосредоточено на трёх сопутствующих белках — PTRAMP, CSS и Ripr — которые консервативны в роде и проверяет, образуют ли они универсальный аппарат для инвазии.
Построение трёхкомпонентного «моста» инвазии
С помощью поиска последовательностей в многочисленных геномах паразитов авторы показывают, что PTRAMP, CSS и Ripr присутствуют во всех основных линиях Plasmodium, в отличие от Rh5, ограниченного одной подгруппой. Предсказание структуры с AlphaFold в сочетании с детальными биохимическими измерениями показывает, что PTRAMP и CSS образуют стабильную пару, соединённую специфической дисульфидной связью между двумя консервативными цистеинами. Эта двухбелковая платформа затем зажимает хвостовую часть Ripr, создавая трёхкомпонентный комплекс PTRAMP–CSS–Ripr (PCR). Эксперименты с белками из P. falciparum, P. vivax и P. knowlesi демонстрируют, что этот комплекс образуется во всех трёх видах с высокой аффинностью, и что для прочного связывания требуется лишь небольшая область на С‑конце Ripr. 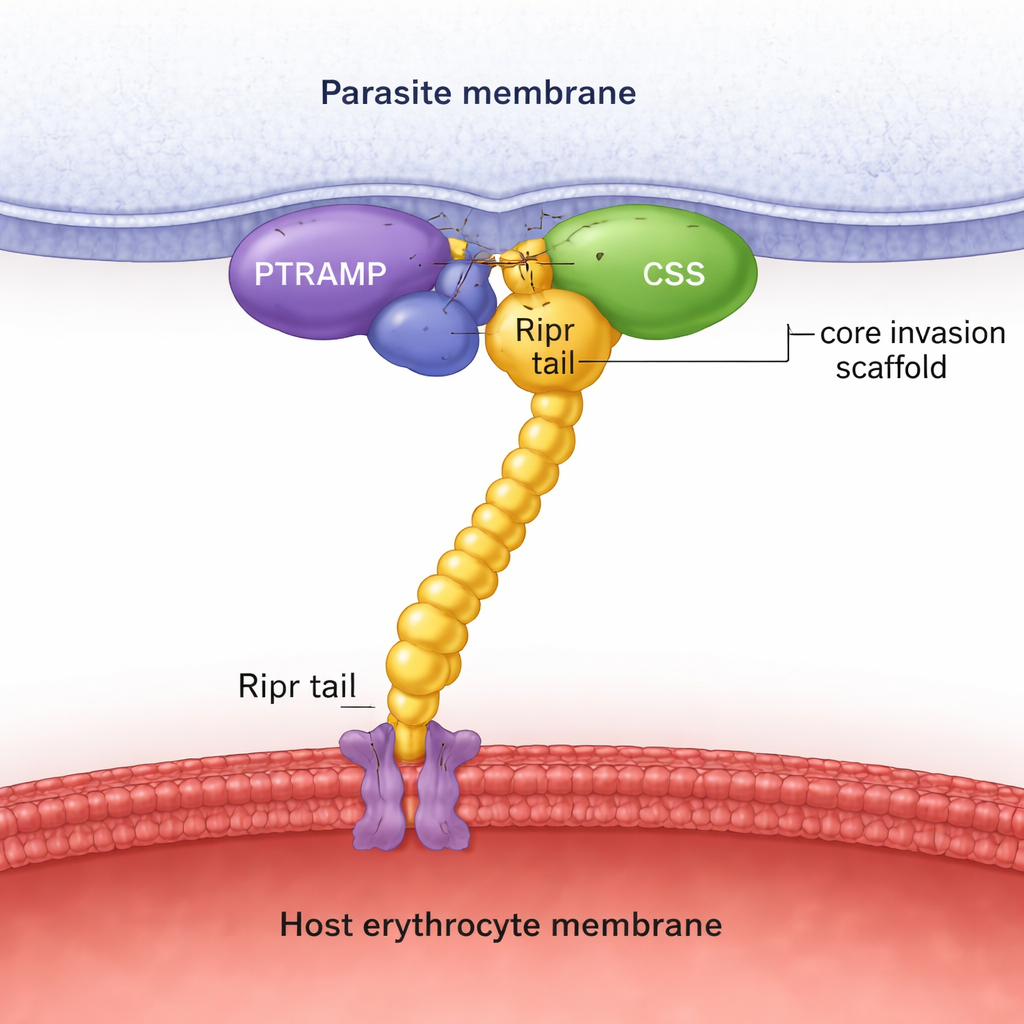
Видеть структуру в атомных деталях
Чтобы выйти за пределы предсказаний, команда решила кристаллические структуры и собрала изображения крио‑электронной микроскопии. Кристаллическая структура пары PTRAMP–CSS из P. vivax показывает, как короткий участок PTRAMP проходит через CSS и формирует ключевую дисульфидную связь. Другая структура фиксирует мощное антитело, связанное с двумя факторами роста подобными доменами Ripr, карта выявляет ингибирующий эпитоп на хвосте Ripr. Крио‑ЭМ анализ комплекса PCR из P. knowlesi подтверждает общую форму, предсказанную AlphaFold: PTRAMP и CSS расположены рядом с мембраной паразита и удерживают Ripr, чей удлинённый корпус простирается в сторону клетки хозяина. В совокупности эти структурные «моментальные снимки» поддерживают идею о том, что трио PCR образует жёсткий каркас, который физически простирается через зазор между паразитом и эритроцитом во время инвазии.
Антитела, распознающие более чем один вид
Поскольку эти белки консервативны, авторы проверили, вырабатывают ли у людей при естественной инфекции антитела, перекрёстно реагирующие между видами. Плазма пациентов, инфицированных P. falciparum, P. vivax или P. knowlesi, показала сильные антительный ответы к CSS и Ripr из нескольких видов, что указывает на то, что люди развивают антитела против общих областей комплекса PCR. Команда затем получила моноклональные антитела и нанотела, нацеленные на PTRAMP, CSS и Ripr P. vivax, и проверила их способность блокировать рост паразита в культуре. Некоторые антитела, особенно одно под названием 5B3, связывающее хвост Ripr, могли ингибировать инвазию P. knowlesi и, при более высоких концентрациях, P. falciparum. Удивительно, что те же антитела не останавливали P. vivax или близкородственного обезьяньего паразита P. cynomolgi, хотя они могли связывать белки из этих видов.
Общий каркас с видовыми дополнениями
Функциональные тесты показывают, что сам комплекс PCR не захватывает эритроциты; скорее, он, по-видимому, служит консервативным структурным каркасом, к которому каждый вид «прикручивает» свои рецептор‑связывающие партнёры. В P. falciparum, например, трио PCR взаимодействует с CyRPA и Rh5 для распознавания базигина на человеческих эритроцитах. У P. vivax и P. knowlesi эквивалентные рецептор‑связывающие белки и мишени хозяина остаются неизвестными, но тот же PTRAMP–CSS–Ripr ядро, по‑видимому, организует аппарат для инвазии. Тот факт, что некоторые антитела могут перекрёстно реагировать, но ингибировать только определённые виды, подчёркивает, насколько тонкие различия в сборке комплекса и времени его работы могут изменить уязвимость к иммунной атаке.
Что это значит для будущих вакцин против малярии
Для неспециалиста ключевая мысль такова: паразиты малярии очень разных видов используют общий «штекер», который они применяют для входа в эритроциты — состоящий из белков PTRAMP, CSS и Ripr — хотя подключают этот штекер к разным рецепторам на поверхности клетки. Этот консервативный штекер теперь картирован структурно и в некоторых случаях может быть поражён антителами, действующими через виды. Хотя необходимы дальнейшие исследования, чтобы определить полный набор партнёрских белков и улучшить ингибирующие антитела, открытие универсального каркаса инвазии открывает путь к разработке вакцин, которые могли бы защищать от нескольких типов малярии, а не только от одного.
Цитирование: Seager, B.A., Lim, P.S., Xiao, X. et al. PTRAMP, CSS and Ripr form a conserved complex required for merozoite invasion of Plasmodium species into erythrocytes. Nat Commun 17, 1780 (2026). https://doi.org/10.1038/s41467-026-68486-1
Ключевые слова: инвазия малярии, белки Plasmodium, проникновение мерозоита, вакцина через виды, инфекция эритроцитов