Clear Sky Science · ru
Структурная основа селективного ингибирования человеческого транспортёра ГАМК GAT3
Почему важно ослаблять сигналы мозга
Наш мозг зависит от тонкого баланса между возбуждающими и успокаивающими сигналами. Одним из ключевых успокаивающих мессенджеров является ГАМК — вещество, которое помогает предотвратить неконтролируемую активность, связанную с такими состояниями, как эпилепсия, повреждение при инсульте и болезнь Альцгеймера. В этом исследовании внимание сосредоточено на белке GAT3, который очищает пространство вокруг нервных клеток от ГАМК. Показывая в атомных деталях, как новая молекула прикрепляется к GAT3 и выключает его, авторы дают структурную карту для разработки лекарств следующего поколения, которые могли бы нежно усилить естественную тормозящую систему мозга.
Собственный тормоз мозга
ГАМК — главный ингибирующий, то есть успокаивающий, нейромедиатор в центральной нервной системе. После высвобождения из нервных окончаний ГАМК нужно быстро удалить, чтобы мозговые цепи могли сбросить состояние. Эту очистку выполняют транспортные белки, которые перекачивают ГАМК обратно в клетки. В мозге доминируют два таких транспортёра: GAT1, в основном на нейронах, и GAT3, расположенный на вспомогательных клетках — астроцитах. В то время как препарат, блокирующий GAT1 (тиагабин), используется десятилетиями для лечения эпилепсии, сопоставимые препараты, нацеленные на GAT3, отставали. Тем не менее GAT3 особенно интересен, так как он контролирует уровни ГАМК вне синапсов и формирует долговременную фоновую ингибицию, способную точно настраивать активность мозга. 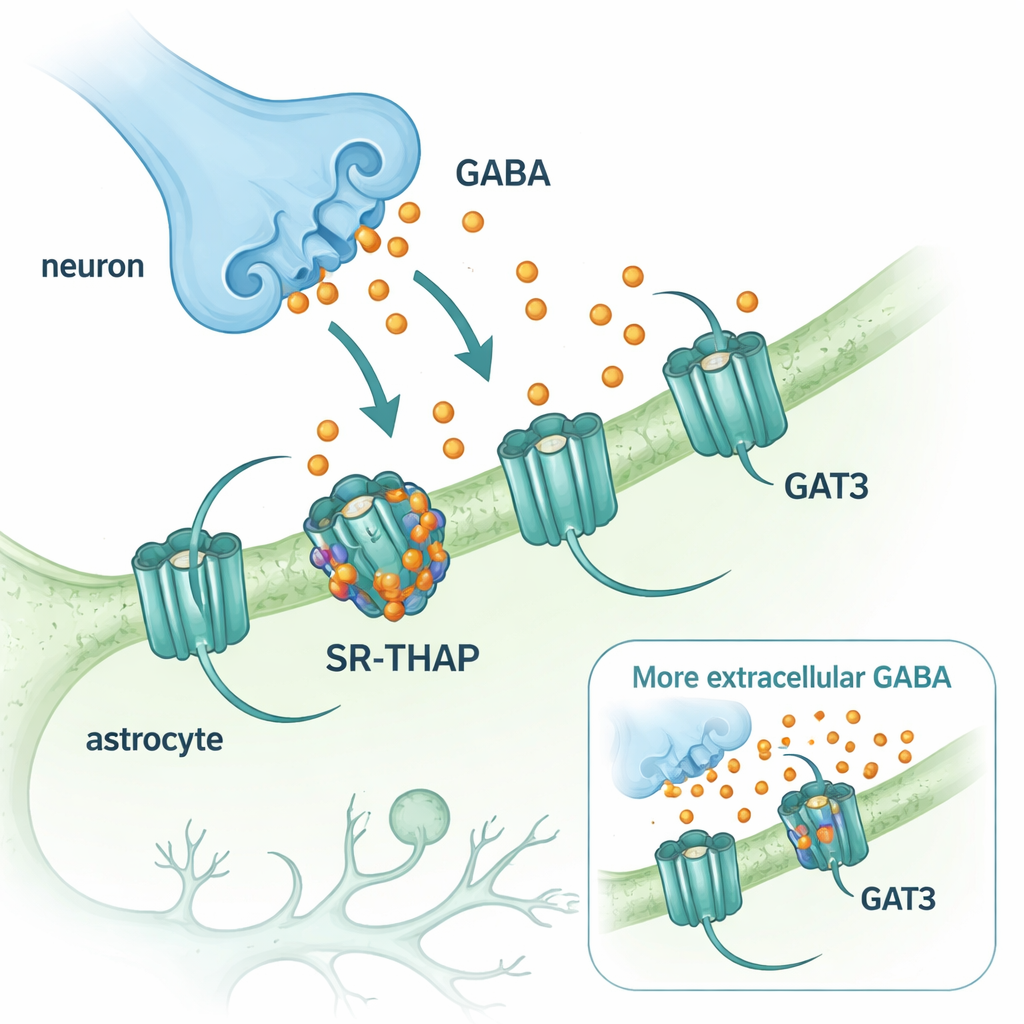
Проектирование более точного молекулярного замка
Попытки ингибировать GAT3 тормозились из‑за отсутствия детальной структурной информации. Многие прежние соединения создавались методом проб и ошибок, часто путём добавления громоздких вариантов к известным молекулам, похожим на ГАМК. Одно из наиболее известных, (S)-SNAP-5114, оказалось химически нестабильным и трудным в применении на живых организмах. Опираясь на более устойчивого родственника этого соединения, авторы разработали SR‑THAP — новую малую молекулу, спроектированную так, чтобы плотнее входить в GAT3 и противостоять разложению. Эксперименты на культурах человеческих клеток показали, что SR‑THAP сильно блокирует GAT3 и делает это неконкурентным способом: вместо простого конкурирования с ГАМК за обычное место связывания он изменяет работу транспортёра, снижая его максимальную транспортную способность.
Рассматривая GAT3 с почти атомным разрешением
Чтобы понять, как именно действует SR‑THAP, команда обратилась к криоэлектронной микроскопии — методу, который изображает быстровымороженые белки с помощью электронов и восстанавливает их трёхмерную форму. Они решили три состояния человеческого GAT3: связанное с SR‑THAP, связанное с ГАМК и в состоянии без субстрата. Все три показали типичную архитектуру, наблюдаемую у родственных транспортёров нейромедиаторов: 12 плотно упакованных спиралей, пронизывающих мембрану и образующих центральный путь для ГАМК и сопутствующих ионов натрия и хлора. В структуре, связанной с ГАМК, транспортёр находится в «внутренне-окклюдированном» состоянии — ГАМК и ион натрия зажаты в середине, изолированы от внешней и внутренней сред. Ключевая ароматическая аминокислота формирует специализированное взаимодействие с аминогруппой ГАМК, что помогает объяснить, как GAT3 распознаёт свой субстрат.
Как SR‑THAP клинит транспортёр в открытом положении
В заметном контрасте, структура, связанная с SR‑THAP, запечатлевает GAT3 в «внутренне-открытом» состоянии, с внутренней стороной белка, раскрытой в сторону клетки. SR‑THAP расположился глубоко в этой внутренней полости, зажатый между несколькими спиралями, которые обычно движутся в ходе транспортного цикла. Он занимает три небольших кармана с разным химическим характером, образуя сеть водородных связей и гидрофобных контактов. Такое положение эффективно клинит транспортёр, так что ГАМК и ионы больше не могут завершить своё перемещение. Авторы показывают, что несколько специфических аминокислот, выстилающих эту полость, отличаются между GAT3 и его ближайшими родственниками; замена одной из этих остатков меняет как транспортную активность, так и силу действия SR‑THAP, что помогает объяснить, почему ингибитор значительно более селективен в отношении GAT3, чем GAT1 или родственные транспортёры. 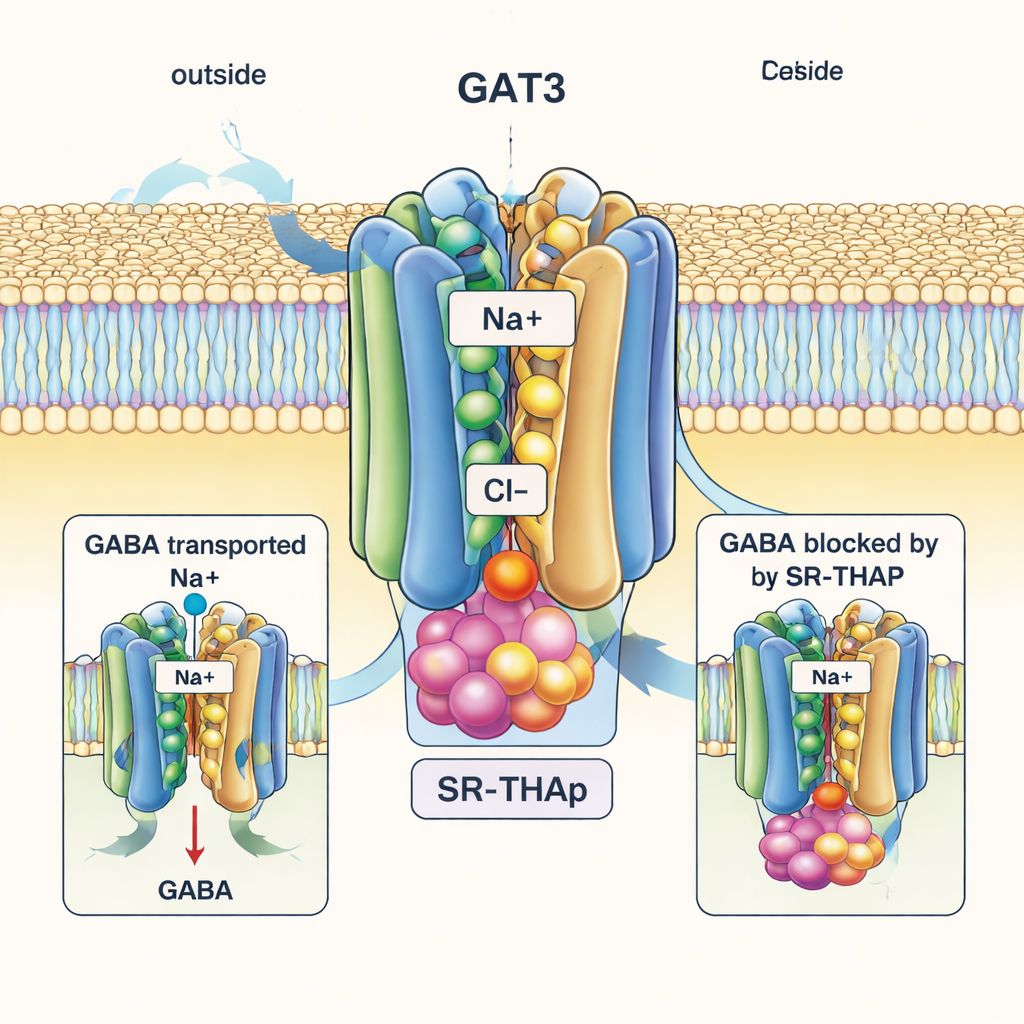
Открывая путь к новым лекарствам при эпилепсии и для здоровья мозга
В совокупности эти структуры показывают, как GAT3 переключается между различными формами для переноса ГАМК и как SR‑THAP использует менее консервативный внутренний карман, чтобы заморозить этот цикл. Для неспециалистов главный вывод состоит в том, что исследование предоставляет детальный молекулярный план для селективного выключения GAT3. Такие соединения могли бы повысить уровни успокаивающего ГАМК в более тонко настроенной манере, чем существующие препараты, что потенциально приведёт к новым методам лечения или инструментам для исследований при эпилепсии, восстановлении после инсульта, болезни Альцгеймера и других состояниях, где нарушена ингибирующая сигнализация.
Цитирование: Mortensen, J.S., Bavo, F., Jensen, M.H. et al. Structural basis for selective inhibition of human GABA transporter GAT3. Nat Commun 17, 1774 (2026). https://doi.org/10.1038/s41467-026-68479-0
Ключевые слова: транспортёр ГАМК, GAT3, эпилепсия, крио-ЭМ, ингибирование нейромедиатора