Clear Sky Science · ru
Стохастический механизм обеспечивает быструю транслокацию субъстрата в машине AAA+ ClpB
Как клеточные машины удерживают белки в движении
В каждой клетке крошечные молекулярные машины постоянно тянут, натягивают и переформировывают белки, чтобы они не слипались и чтобы восстанавливать повреждения. Одна такая машина, называемая ClpB, помогает спасать спутанные белки — важная функция для выживания клетки в условиях стресса. В этом исследовании задаётся простой, но глубинный вопрос: как ClpB превращает химическое топливо ATP в механическую работу по протягиванию цепочки белка через свой центральный канал, и делает ли он это в аккуратных, синхронизированных шагах или более случайным, диффузионным способом?
Кольцо спасения белка в действии
ClpB принадлежит к большой семье ферментов AAA+, которые собираются в кольцевые структуры с центральным туннелем. Многие из них были детально изображены методом крио-электронной микроскопии, что породило популярную модель «рука-за-рукой»: каждая молекула ATP, расходуемая при работе, приводила бы в действие небольшой точный шаг, как команда людей, тянущих канат по очереди. Тем не менее другие эксперименты намекали, что ClpB может перемещать белки гораздо быстрее, чем позволяла бы его медленная скорость гидролиза ATP. Чтобы разрешить этот парадокс, авторы наблюдали за отдельными молекулами ClpB в реальном времени, пока те протягивали гибкий тестовый белок κ-казеин через свой канал.
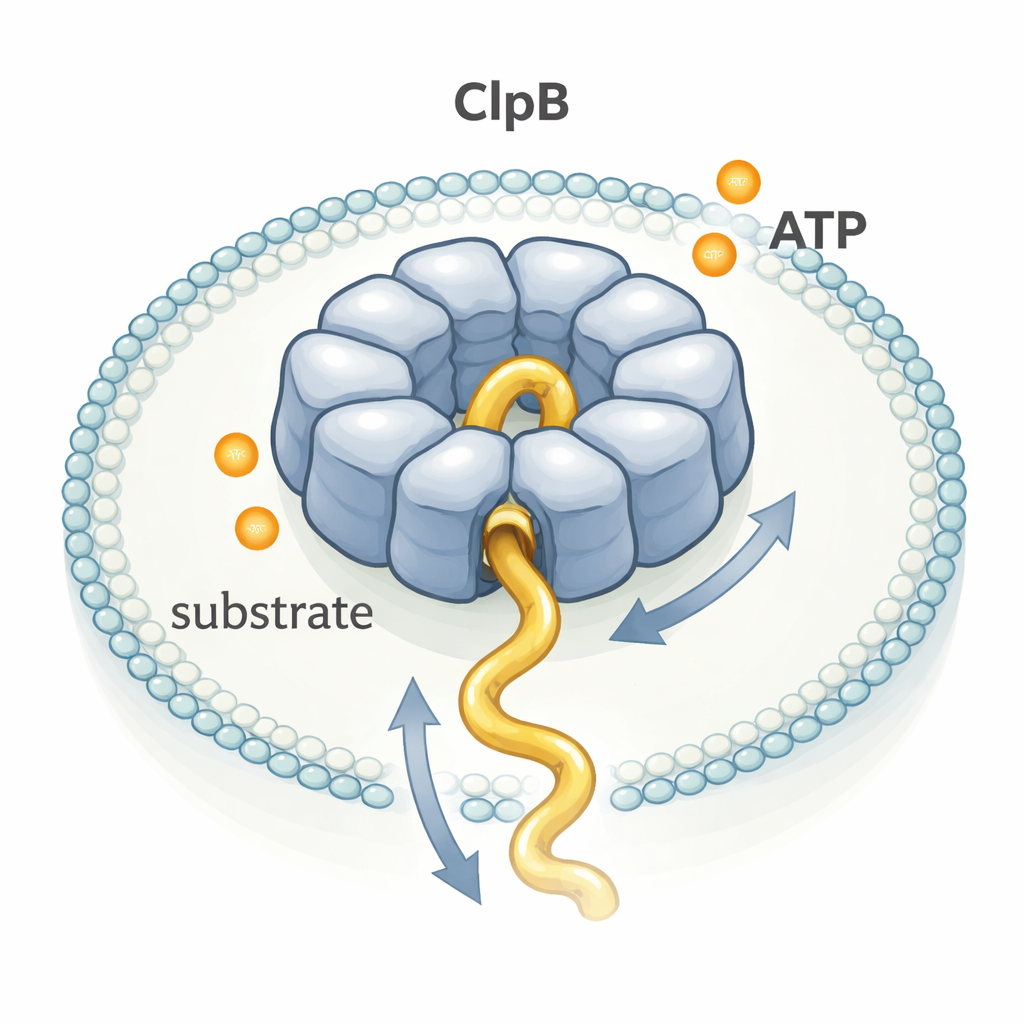
Наблюдая за одной молекулой за раз
Исследователи захватывали отдельные кольца ClpB и отдельные молекулы κ-казеина вместе внутри крошечных липидных пузырьков, прикреплённых к стеклянной поверхности. Они прикрепляли флуоресцентные красители к определённым точкам на ClpB и на полипептидной цепочке, а затем использовали одномолекулярный FRET — метод, который фиксирует изменения расстояния между красителями на нанометровом уровне. Когда κ-казеин заходил в канал ClpB, красители сближались и сигнал FRET резко возрастал в виде короткого всплеска; когда цепочка выходила, сигнал снова падал. Измеряя длительность и амплитуду тысяч таких всплесков, они могли вывести, как быстро и на какое расстояние фрагменты белка протягивались через канал.
Быстро, с малым расходом топлива и почти не зависяще от температуры
Удивительно, но события транслокации были исключительно быстрыми: помеченный фрагмент κ-казеина обычно проходил несколько нанометров канала примерно за 1–2 миллисекунды — примерно в тысячу раз быстрее среднего интервала между событиями гидролиза ATP у ClpB. Большинство событий были такими короткими и следовали широкой распределённой закономерности типа степенного закона, а не единой характерной временной шкале. Изменение температуры от 10 до 32 °C едва замедляло эти движения, что указывает на то, что энергетический барьер для перемещения очень мал по сравнению с классическими «ходовыми» моторами, такими как кинезин. Аналогично, снижение концентрации ATP значительно уменьшало частоту событий, но почти не влияло на их длительность. Иначе говоря, ATP скорее контролировал, когда ClpB подключается и как часто он действует, чем скорость отдельных всплесков протягивания.
Движение вперёд-назад с предвзятостью вперёд
Чтобы понять, всегда ли цепочки движутся в одном направлении, команда провела более сложные эксперименты с трёхцветным FRET, пометив оба конца канала и субстрат. Это позволило им отличать, заходил ли κ-казеин сверху или снизу кольца и проходил ли он полностью или отступал. Они обнаружили шесть различных паттернов: полная передняя и задняя транслокация, более длинные «частичные» визиты, когда цепочка исследовала оба конца канала перед уходом, и мимолётные столкновения у одного из концов. Примерно три четверти полных событий шли в прямом направлении, но заметная доля шла назад, что показывает, что ClpB допускает двунаправленную диффузию субстрата с лишь умеренной предвзятостью вперёд. Когда ATP заменяли на медленно гидролизуемый аналог, события становились редкими и значительно медленнее, а предпочтение вперёд практически исчезало.
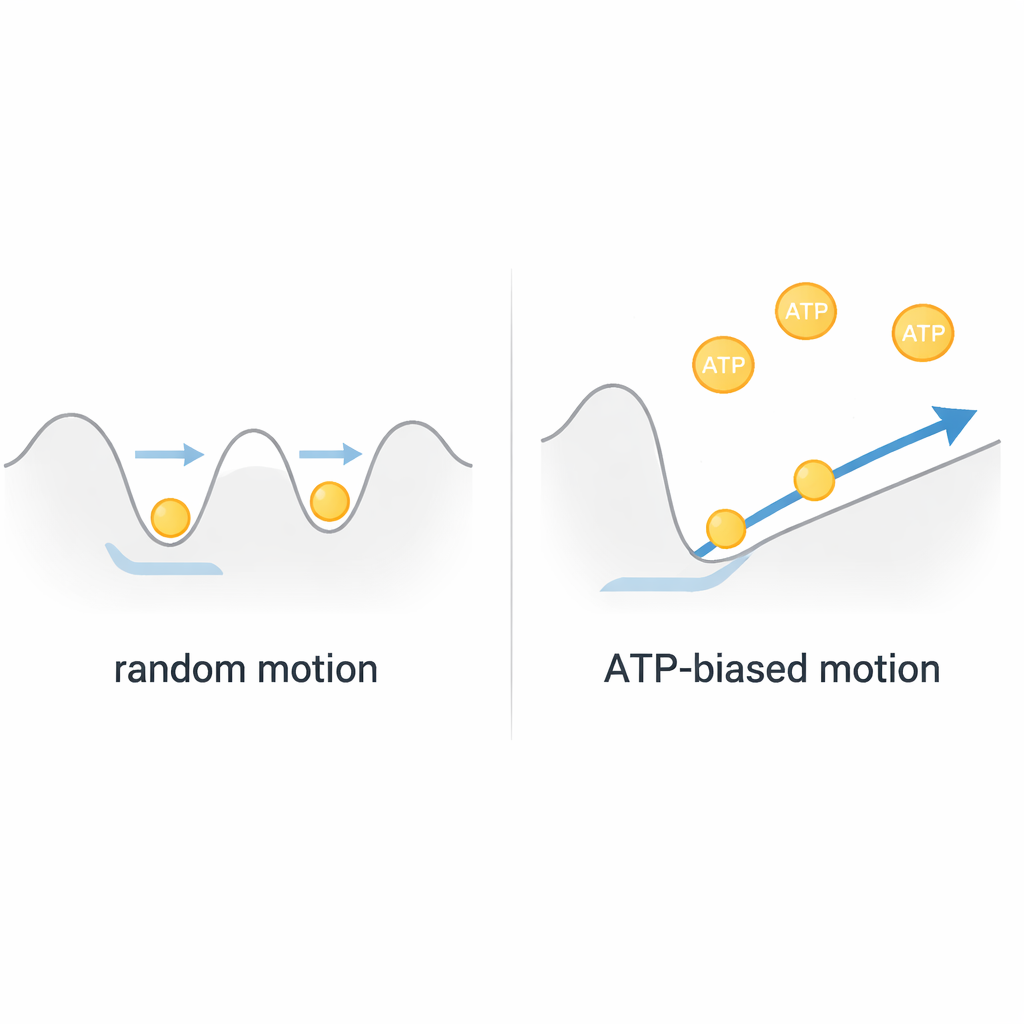
Брауновский мотор, а не простой лебёдочный механизм
Собрав эти наблюдения воедино, авторы приходят к выводу, что ClpB работает скорее как брауновский мотор, чем как жёсткий, приводимый топливом лебёдочный механизм. Белковая цепочка термически колеблется внутри неглубокого энергетического ландшафта в канале, быстро двигаясь вперёд и назад. ATP не даёт прямую силу для больших дискретных «рывков»; вместо этого он подстраивает форму этого ландшафта через быстрые движения внутренних «поровых петель», тонко смещая предпочтение движения в одном направлении. Поскольку каждое полное событие протягивания коррелирует примерно с потреблением одной или двух молекул ATP, ClpB добивается удивительно эффективной, быстрой транспортировки, выпрямляя случайное движение, а не «борясь» с ним. Эта концепция меняет наше представление о многих машинах AAA+, предполагая, что биологические наномоторы часто используют случайность, а не устраняют её.
Цитирование: Casier, R., Levy, D., Riven, I. et al. A stochastic mechanism drives fast substrate translocation in the AAA+ machine ClpB. Nat Commun 17, 1773 (2026). https://doi.org/10.1038/s41467-026-68478-1
Ключевые слова: транслокация белка, машина AAA+, брaуновский мотор, молекулярный шаперон, одномолекулярный FRET