Clear Sky Science · ru
Идентификация термостойких неклассических PAM для надёжного однофазного обнаружения CRISPR‑Cas12a
Нагревая ДНК‑тесты
Быстрые и точные тесты на инфекции и генетические изменения жизненно важны для медицины, но современные ДНК‑методы часто требуют сложного лабораторного оборудования и могут пропускать редкие или тонкие цели. В этом исследовании показано, что простое повышение температуры проведения CRISPR‑теста открывает множество дополнительных полезных «ручек» на ДНК, делая однофазную диагностику быстрее, чувствительнее и способной различать даже одиночные буквенные изменения в генетическом коде. 
Почему CRISPR нужен почтовый индекс
Инструменты CRISPR, такие как Cas12a, работают, нацеливаясь на определённые участки ДНК с помощью короткой направляющей РНК, действующей как поисковая строка. Но они могут прикрепиться и начать работу только если рядом есть четырёхбуквенный тег, называемый PAM, с подходящей последовательностью — традиционно это узкий набор, начинающийся с «TTT». Это похоже на необходимость наличия номера дома перед доставкой письма: если нужного номера нет, сообщение не дошло бы. Требование к PAM ограничивает области, в которых CRISPR может работать, что серьёзно затрудняет обнаружение врачами конкретных мутаций, маркеров лекарственной устойчивости или вирусных вариантов, которые не находятся рядом с этими классическими тегами.
Открытие новых «дверей» при повышенных температурах
Авторы систематически проверили все 256 возможных четырёхбуквенных комбинаций PAM, чтобы оценить, насколько хорошо они запускают «побочное» разрезание Cas12a — способность рассекать множество лежащих поблизости молекул ДНК после распознавания цели, что и даёт диагностический сигнал CRISPR. При обычной температуре тела (37 °C) лишь несколько нестандартных PAM работали так же хорошо, как классические. Но при повышении температуры реакции до ~45 °C произошло заметное явление: 82 различных неклассических PAM внезапно дали сильную активность по разрезанию сигналов, сопоставимую со стандартными тегами. Исследователи полагают, что дополнительное тепло ослабляет локальную структуру ДНК и делает комплекс Cas12a более гибким, снижая барьер для распознавания ранее «слабых» PAM.
Сильный сигнал, щадящее обращение с матрицей
У Cas12a есть два режима разрезания. В «цис»‑режиме он разрезает конкретную ДНК, которую ему поручили найти; в «транс»‑режиме, однажды активированный, он быстро дробит любые близлежащие сигнал‑несущие нитки, что и даёт вспышку сигнала теста. Исследователи обнаружили, что при повышенных температурах неклассические PAM обеспечивают очень сильное транс‑разрезание — отлично для яркого и быстрого считывания — но при этом цис‑разрезание основной ДНК остаётся относительно слабым. Такое сочетание идеально для однофазных тестов, где ДНК сначала нужно амплифицировать, не разрушив её. Они также показали, что при этих тёплых условиях Cas12a становится куда более требовательным к несовпадениям между направляющей РНК и целью: даже один неверный нуклеотид может выключить сигнал, особенно при использовании неклассических PAM. 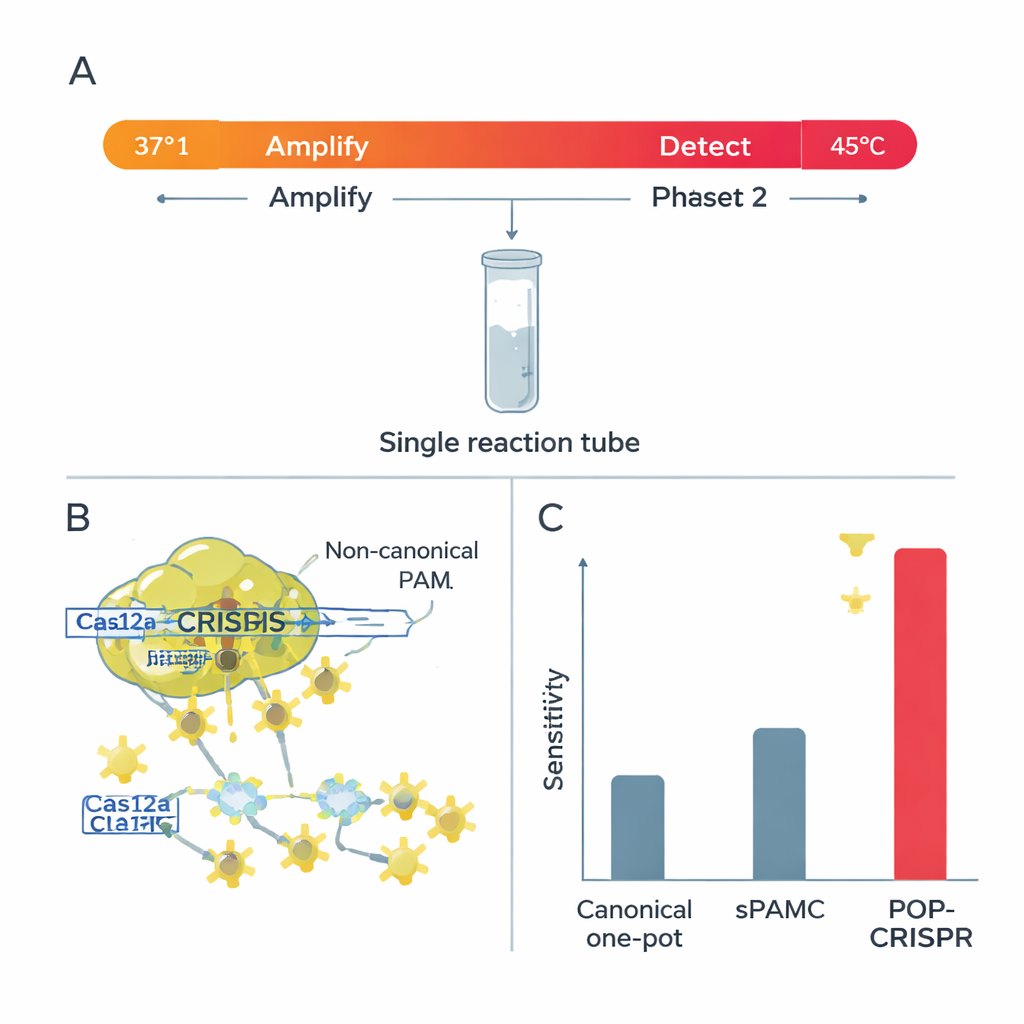
Более умный однофазный тест: POP‑CRISPR
Опираясь на эти наблюдения, команда создала POP‑CRISPR — «пойкилотермический» (с переменной температурой) однофазный анализ. Реакция начинается примерно при 37 °C, где изотермический метод амплификации тихо увеличивает количество целевой ДНК или РНК, пока Cas12a относительно неактивен. Через ~10 минут смесь нагревают до ~45 °C — оптимальной точки, где Cas12a, теперь направляемая к неклассическим PAM, включает мощное транс‑разрезание и генерирует сильный флуоресцентный сигнал. Эта простая двухступенчатая температурная программа повысила чувствительность обнаружения примерно в десять раз по сравнению с ранними однофазными CRISPR‑методами, также использовавшими слабые PAM, и явно превзошла традиционные однофазные форматы с каноническими PAM.
От лаборатории к практическому применению за считанные минуты
Систему POP‑CRISPR протестировали на клинических образцах. Она чувствительно обнаруживала вирус папилломы человека (HPV‑16) в влагалищных мазках и Mycoplasma pneumoniae в респираторных пробах, включая очень низкие «серые» уровни, которые представляют трудности для стандартных методов. Что важно, POP‑CRISPR смог отличить штаммы Mycoplasma с лекарственной устойчивостью, несущие одиночную буквенную замену в рибосомном гене, даже если рядом с этой мутацией не было классического PAM — задача, которая ставит в тупик многие существующие тесты Cas12a. Чтобы сделать подход пригодным для полевых условий, авторы сочетали быстрый двухминутный этап лизиса с нагревом и Chelex (избегая полной экстракции ДНК) с портативным флуоресцентным считывателем размером с ладонь, управляемым смартфоном. В совокупности этот рабочий процесс позволяет превратить сырую мазок‑пробу в цифровой ответ «да/нет» примерно за 20 минут.
Что это значит для повседневного тестирования
Повышая температуру реакции и используя значительно более широкий набор PAM‑«дверей», эта работа превращает Cas12a в более гибкий и точный сенсор. POP‑CRISPR обеспечивает более быстрое, чувствительное и специфичное обнаружение нуклеиновых кислот в одной закрытой пробирке, одновременно расширяя диапазон генетических участков, к которым можно нацеливаться — включая однонуклеотидные мутации, связанные с лекарственной устойчивостью или раком. Для пациентов это может означать более быстрый диагноз на месте и лучше подобранное лечение; для исследователей и разработчиков тестов — мощный новый способ проектирования CRISPR‑диагностик, которые одновременно более надёжны и более избирательны.
Цитирование: Tian, T., Zhang, T., Zhang, W. et al. Identification of thermotolerant non-canonical PAMs for robust one-pot CRISPR-Cas12a detection. Nat Commun 17, 1771 (2026). https://doi.org/10.1038/s41467-026-68476-3
Ключевые слова: Диагностика CRISPR, Cas12a, участки PAM, экспресс‑тестирование, обнаружение нуклеиновых кислот