Clear Sky Science · ru
Структурные механизмы ингибирования и активации человеческого калиевого канала SK2 с малой проводимостью, активируемого Ca2+
Почему крошечные калиевые каналы важны
Каждая ваша мысль и каждый удар сердца зависят от электрических сигналов в клетках. Эти сигналы формируют микроскопические поры — ионные каналы, через которые проходят заряженные ионы. Одна из таких семейств, малопроводящие кальций‑активируемые калиевые каналы (SK), помогает регулировать возбуждение нейронов и поддерживать ритм сердца. В этой работе в атомных деталях показано, как разные лекарства и пчелиный токсин либо блокируют, либо усиливают ключевого члена этого семейства — человеческий канал SK2 — что может послужить ориентиром для создания терапий при таких состояниях, как мерцательная аритмия, тремор и нарушения памяти.
Как SK2 действует как клеточный «тормоз»
Каналы SK2 находятся в мембране клетки и выполняют роль микротормоза электрической активности. Когда внутри клетки в ходе электрического сигнала кратковременно повышается концентрация ионов кальция, белок‑помощник кальмодулин это ощущает. Кальмодулин прикреплён к внутренней стороне SK2 и, связывая кальций, тянет за часть канала подобно шнурку, открывая затвор, через который наружу выходит калий. Этот отток помогает успокоить клетку после возбуждения — он влияет на частоту спайкования нейронов и надёжность сердечных сокращений. Поскольку каналы SK1–3 широко представлены в мозге и сердце, а SK2 является особенно важным подтипом, понимание того, как они открываются, закрываются и реагируют на лекарственные соединения, критично для разработки точных препаратов.
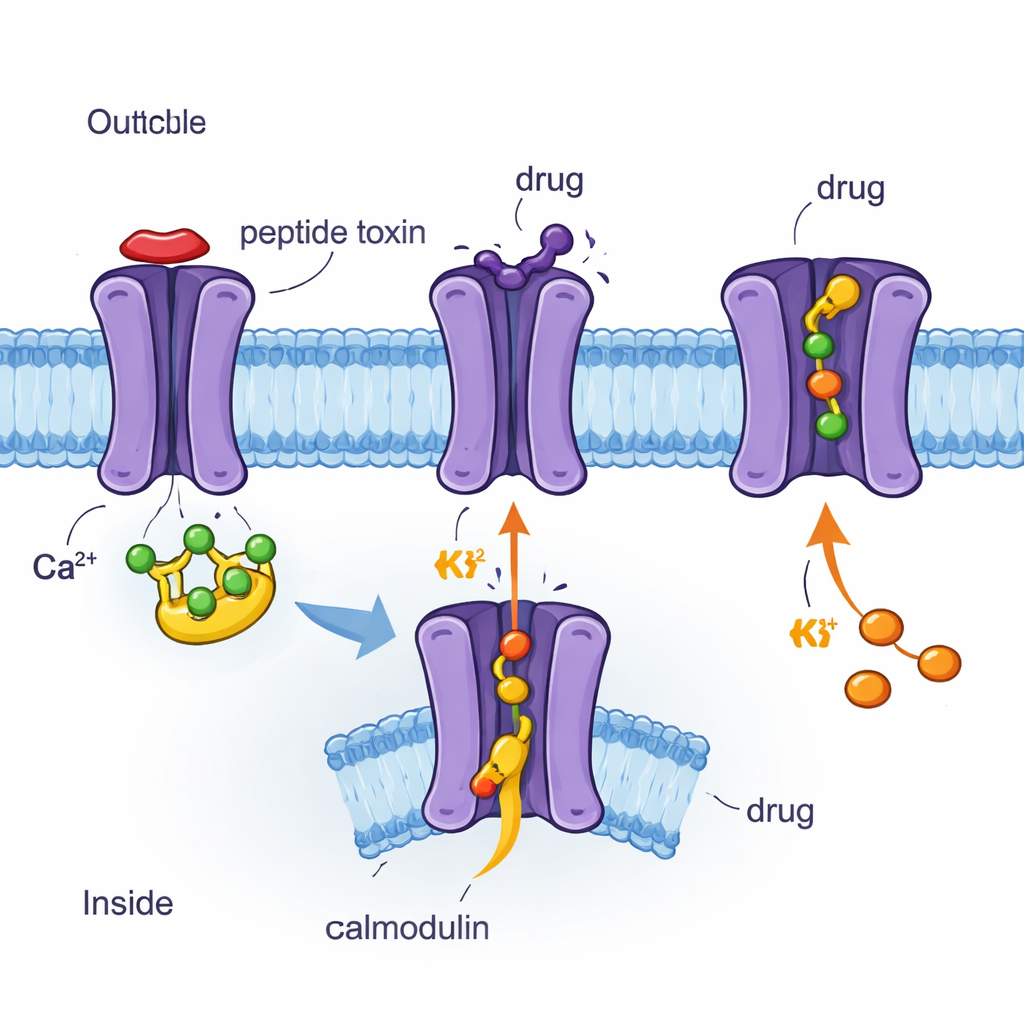
Использование крио‑ЭМ для просмотра каналов и лекарств поатомно
Авторы применили крио‑электронную микроскопию (крио‑ЭМ), метод, который визуализирует быстро замороженные белки с почти атомным разрешением, чтобы определить четыре трёхмерные структуры человеческого канала SK2 в комплексе с кальмодулином и различными молекулами. Это включало пептид апамин из пчелиного яда, синтетический блокатор UCL1684, клинический ингибитор AP30663 и клинический активатор CAD‑1883. Во всех четырёх структурах SK2 показан как четырёхчастная сборка, пронизывающая мембрану, с прикреплённым изнутри кальмодулином. Сравнение этих снимков выявило, какие участки канала жёсткие, какие гибкие, и как двигается кальмодулин в закрытом и открытом состояниях. Исследователи также сочетали эти изображения с электрическими измерениями в клетках, проверяя, как замены отдельных аминокислот меняют ответ канала на каждое соединение.
Пчелиный токсин и лабораторный препарат, затыкающие внешний вход
Апамин, небольшой пептид из пчелиного яда, давно известен как чрезвычайно мощный и селективный блокатор SK2, используемый в исследованиях. Новые структуры показывают, что апамин связывается, как пробка, в наружном входе поры SK2. Он располагается в чашевидном вестибюле, сформированном короткой петлёй между двумя спиралями (связывающий участок S3–S4), который в SK2 хорошо упорядочен, но в родственном канале SK4 более подвижен — это объясняет нечувствительность SK4 к апамину. Ключевые положительно заряженные остатки апамина проникают между четырьмя ароматическими боковыми цепями канала, образуя сильные электростатические и стопочные взаимодействия, которые полностью закупоривают путь для калия. UCL1684, синтетическое бис‑хинолиниевое соединение, занимает по сути тот же внешний карман и также блокирует выход ионов, но за счёт меньших размеров располагается глубже, имитируя позицию критических положительных зарядов апамина. Мутации остатков канала, формирующих этот вестибюль, резко снижают чувствительность к апамину и, в меньшей степени, к UCL1684, подтверждая, что эта скульптурированная внешняя петля является важным детерминантом действия токсина и препарата.
Центральная пробка и внутренний клин, настраивающие активность
Напротив, клинический кандидат AP30663 связывается внутри центральной полости SK2, непосредственно под селективным фильтром, который отбирает ионы калия. Там он действует как физическая пробка, зажатая между определёнными боковыми цепями, выстилающими пору. Изменения в этих выстилающих остатках ослабляют способность AP30663 ингибировать SK2, а сравнение последовательностей объясняет, почему его близкие аналоги различают SK1–3 и SK4. CAD‑1883, позитивный модуль, разработанный для двигательных расстройств, использует иной приём. Он проникает в карман на интерфейсе между N‑лобом кальмодулина и короткой связкой (S4–S5), которая передаёт движение кальмодулина к затвору канала. Укрепляя контакты в этом кармане, CAD‑1883 фактически «склеивает» кальмодулин и SK2 в конфигурации, которая тянет внутренний затвор открытым и расширяет пору. Структурные сравнения показывают, что состояние, связанное с CAD‑1883, походит на полностью открытый канал, хотя селективный фильтр может перейти в инактивированную форму после длительного открытия.
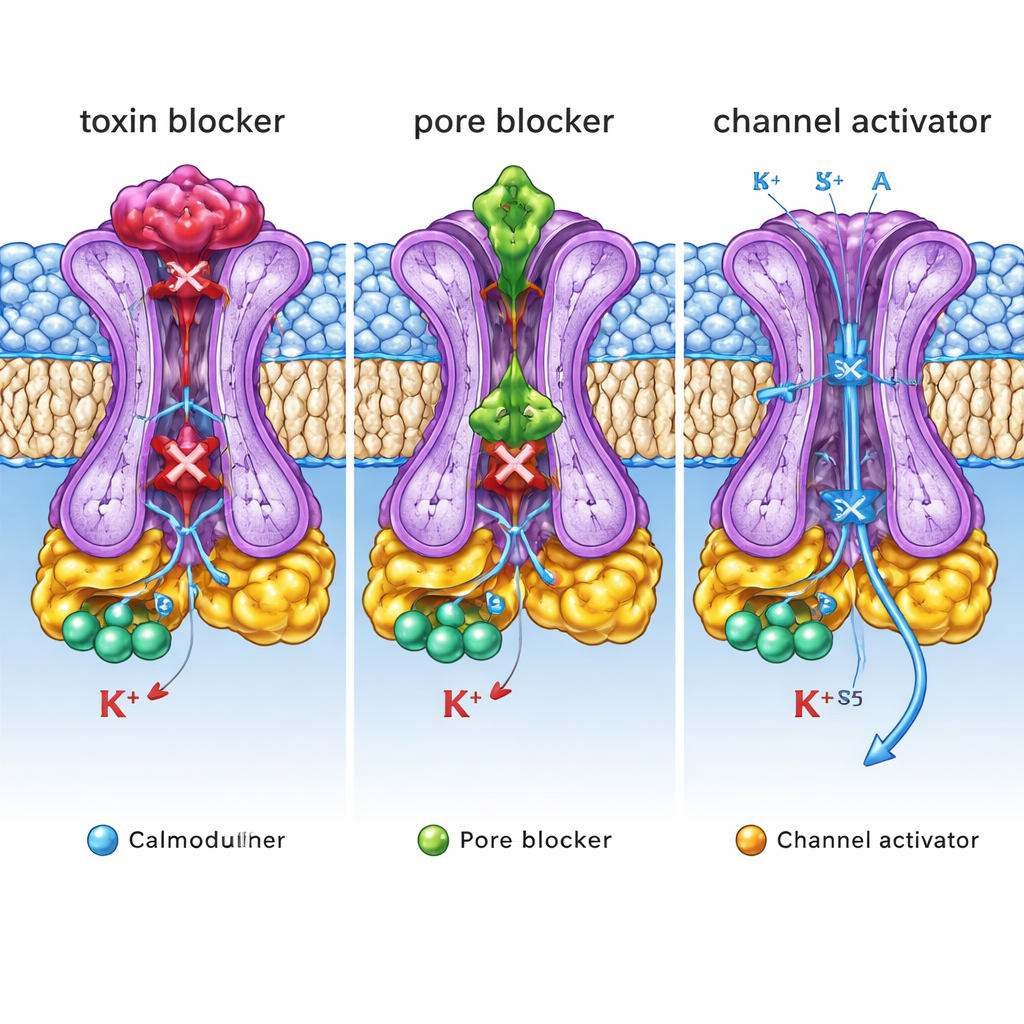
Что эти структурные чертежи значат для медицины
Вместе эти структуры выявляют три различных «регулирующих ручки» на одном канале SK2: внешнюю крышку, где сидят токсины и некоторые блокаторы; внутреннюю полостную часть, где другие ингибиторы затыкают поток; и боковой карман, где активаторы стабилизируют открытие. Для неспециалиста ключевая идея такова: один и тот же ионный канал можно настроить вверх или вниз с помощью препаратов, которые хватаются за очень разные структурные «ручки». Отобразив эти ручки с атомной точностью и связав их с функциональными эффектами, эта работа предоставляет подробную схему для разработки следующего поколения молекул, которые селективно подавляют или усиливают активность SK2. Такие специфические препараты в будущем могли бы помочь нормализовать ненормальные ритмы мозга, облегчить тремор или исправить нерегулярность сердечных сокращений с меньшим количеством побочных эффектов.
Цитирование: Ma, B., Wu, D., Cao, E. et al. Structural mechanisms for inhibition and activation of human small-conductance Ca2+-activated potassium channel SK2. Nat Commun 17, 1770 (2026). https://doi.org/10.1038/s41467-026-68475-4
Ключевые слова: калиевые каналы SK2, кальций‑активируемые каналы, структуры методом крио-ЭМ, модуляторы ионных каналов, мерцательная аритмия и тремор