Clear Sky Science · ru
Системы расщеплённого базового редактирования на основе гетеродимеров коил‑катушек обеспечивают гибкие и надёжные нуклеотидные замены
Исправление ДНК с меньшими побочными эффектами
Многие заболевания вызваны крошечными опечатками в нашей ДНК — одиночными ошибками‑буквами, которые могут иметь угрозу для жизни. У учёных есть мощные инструменты, называемые базовыми редакторами, которые могут исправлять такие опечатки без разрезания ДНК, но эти инструменты громоздки и трудно безопасно доставляются в организм. В этой работе предложен новый способ расщеплять базовые редакторы на меньшие, более умные фрагменты, которые при этом работают так же хорошо или даже лучше оригинала, открывая новые пути для лечения генетических заболеваний в печени, мышцах и других органах.
Почему размер — проблема для инструментов редактирования генов
Базовые редакторы объединяют элементы системы CRISPR с ферментами, которые способны заменить одну букву ДНК на другую, например заменить A на G или C на T. Такие точные замены перспективны для лечения заболеваний вроде высокого холестерина или мышечной дистрофии. Однако ведущий вектор для генной терапии — адено‑ассоциированный вирус (AAV) — может нести лишь около 4,7 тысячи нуклеотидов, тогда как стандартные базовые редакторы больше этого размера. Ранее пытались расщеплять эти редакторы с помощью специальных белковых «ножниц» — интeинов, или уменьшать их мини‑ферментами, но эти подходы часто снижали эффективность, усложняли дизайн или ограничивали участки генома, где инструменты могли работать.
Использование молекулярного «липучего» соединения для воссоединения редактора
Чтобы решить эту проблему, авторы разработали «расщеплённый» базовый редактор, который держится вместе за счёт коротких белковых молекул‑катушек — коил‑гетеродимеров, подобно молекулярной липучке. Они разделили редактор на две части: одну с нуклеазно‑портящей Cas9‑никказой для нацеливания на ДНК и другую с ферментом редактирования. Короткие коил‑пептиды на каждой половинке находят друг друга и защёлкиваются, когда обе половины попадают к одной и той же последовательности ДНК. Получились коил‑катушечные базовые редакторы (CC‑BE), включая варианты для редактирования C (CC‑CBE), A (CC‑ABE) и более сложные модификации, способные вносить разные типы замен. 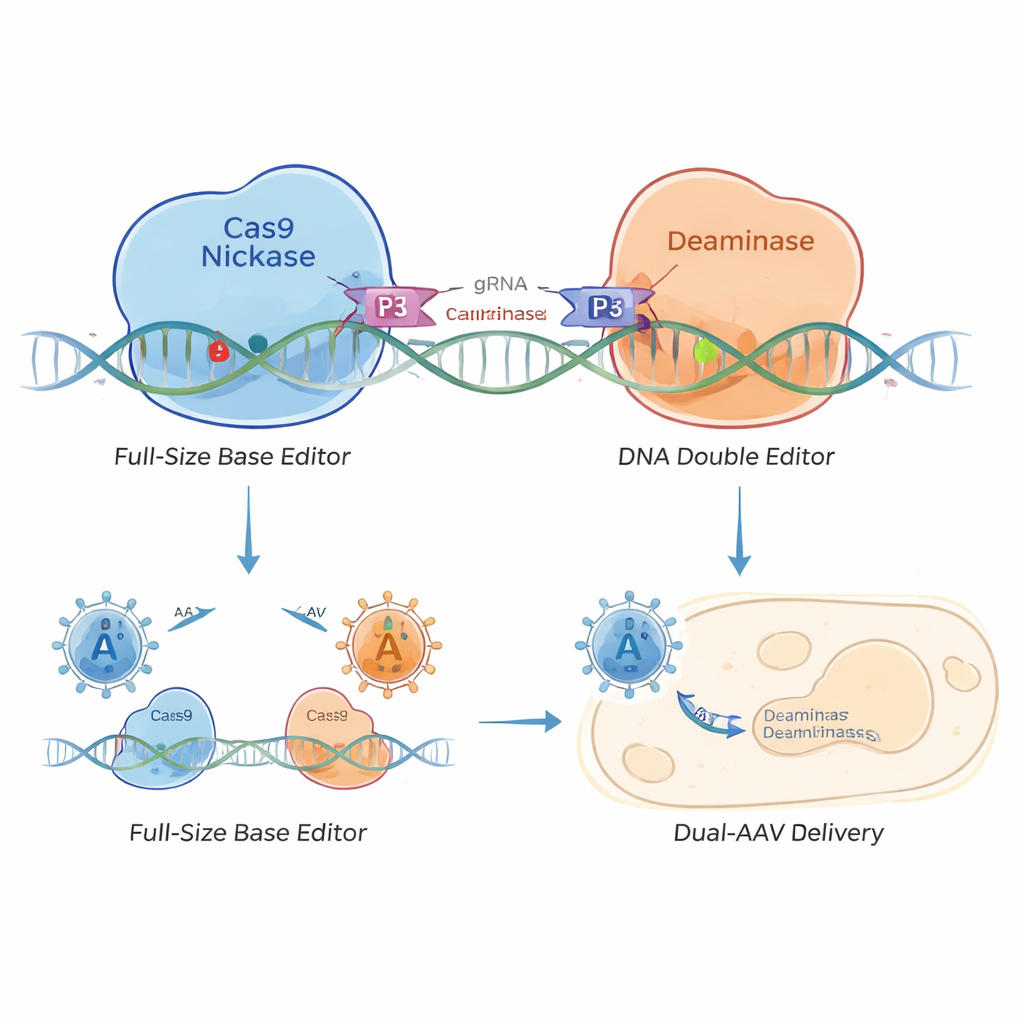
Гибкое, мощное и точное редактирование
Команда протестировала CC‑BE в нескольких типах клеток, включая человеческие клетки и первичные клетки свиньи, а также с различными вариантами Cas9, распознающими более широкий набор последовательностей ДНК. Варианты CC‑CBE работали надёжно во многих локусах и демонстрировали более широкое «окно редактирования», то есть могли менять целевые буквы на более длинном участке ДНК, что даёт учёным большую гибкость при выборе направляющих РНК. Варианты CC‑ABE достигали эффективности, сопоставимой с лучшими существующими адениновыми редакторами, при этом часто давали меньше побочных продуктов. Исследователи также адаптировали стратегию коил‑катушек к новым конструкциям редакторов — таким как компактный TadCBE и точный ABE9 — и вновь обнаружили, что разбиение с помощью коил‑пар сохраняет или улучшает характеристики.
От чашек Петри до живых мышей
Ключевой момент: авторы продемонстрировали работу этих расщеплённых редакторов в живых организмах с помощью двойной доставки AAV, когда каждый вирус несёт половину редактора. У мышей CC‑ABE, нацеленный на ген Pcsk9 в печени, обеспечил конверсии A→G до примерно 70%, резко снизив уровень белка Pcsk9 и LDL‑холестерина в крови без признаков повреждения печени. 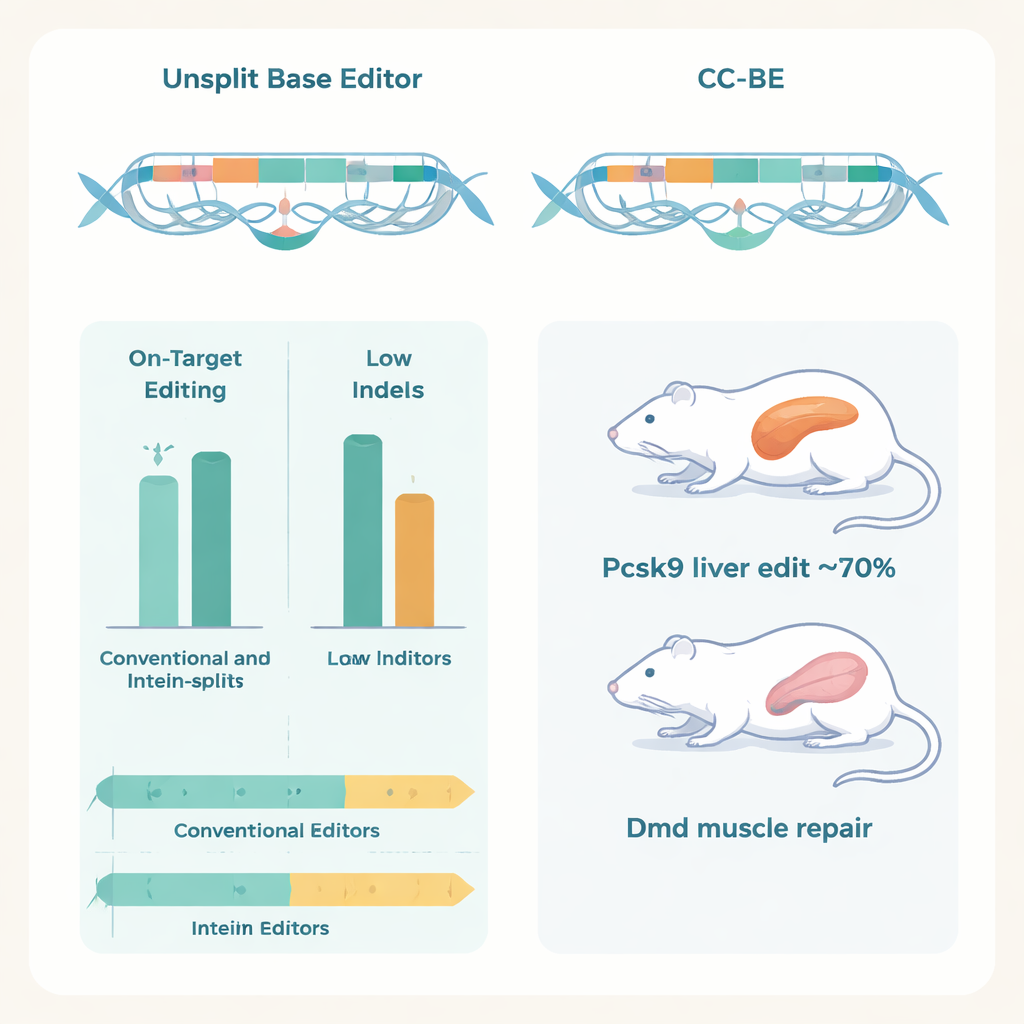
Новый путь к практическому ремонту ДНК
По сути, это исследование предлагает простую, но эффективную инженерную идею: использовать маленькие коил‑«крючки», чтобы разделить большие базовые редакторы на модули, подходящие по размеру для AAV, которые вновь соединяются только там, где это необходимо. Для непрофессионалов вывод ясен: теперь учёные могут упаковывать мощные инструменты для коррекции ДНК в клинически проверенные вирусные носители, не теряя ни точности, ни эффективности. Подход с коил‑катушками может упростить разработку лечений для широкого круга однобуквенных генетических заболеваний в органах вроде печени, сердца и мышц, приблизив тонкую коррекцию генов к реальной клинической практике.
Цитирование: Mu, S., Li, Q., Chen, M. et al. Coiled-coil heterodimer-mediated split base editing systems enable flexible and robust nucleotide substitutions. Nat Commun 17, 1765 (2026). https://doi.org/10.1038/s41467-026-68469-2
Ключевые слова: базовое редактирование, генная терапия, CRISPR, доставка AAV, генетическое заболевание