Clear Sky Science · ru
Использование индуцированного глюканом «тренированного иммунитета» для эпигенетической и метаболической перепрограммировки макрофагов с целью повышения ответа на вакцину против колоректального рака
Пробуждение первичных защитников организма
Колоректальный рак — один из самых смертоносных видов рака в мире, и большинство пациентов не получают ощутимой пользы от доступных сегодня иммунотерапий. В этом исследовании рассматривается интригующая идея: что если мы сможем «обучить» врожденную иммунную систему — первичных защитников организма — запоминать опасность и помогать вакцинам работать лучше против колоректальных опухолей? С помощью природного сахара из дрожжей, называемого бета‑глюканом, авторы показывают, как ранние иммунные клетки можно перепрограммировать так, чтобы вакцины вызывали более мощные и длительные атаки на опухоли.
Почему колоректальному раку нужны новые защитные подходы
Колоректальный рак ежегодно уносит почти миллион жизней во всем мире, и число случаев у молодых людей растет. Стандартные лечения — хирургия, химиотерапия и лучевая терапия — могут быть эффективны, но многие пациенты рецидивируют и сталкиваются с тяжелыми побочными эффектами. Новые иммунные препараты, такие как ингибиторы контрольных точек, очень хорошо действуют только в небольшой части колоректальных опухолей с особыми дефектами репарации ДНК. Для большинства пациентов эти препараты и даже экспериментальные вакцины неэффективны, поскольку опухолевое окружение доминируют клетки и сигналы, подавляющие иммунную атаку.
Обучение врожденного иммунитета новым приёмам
Врожденные иммунные клетки организма — особенно макрофаги — обычно реагируют быстро, но недолго, и считалось, что у них отсутствует память. Однако за последнее десятилетие было показано явление «тренированного иммунитета», когда сильный первоначальный стимул оставляет длительные отпечатки на этих клетках, позволяя им позже отвечать более энергично. Авторы использовали бета‑глюкан — компонент клеточной стенки дрожжей — для индукции этого тренированного состояния. У мышей кратковременная обработка цельными частицами бета‑глюкана перепрограммировала макрофаги как на уровне активности генов, так и на уровне клеточного метаболизма. Когда эти тренированные животные позже получали вакцину против колоректального рака на основе модифицированного аденовируса (названного PeptiCrad), их иммунные системы продуцировали более мощные киллерные Т‑клетки, которые лучше распознавали и атаковали опухолево‑специфические мишени. 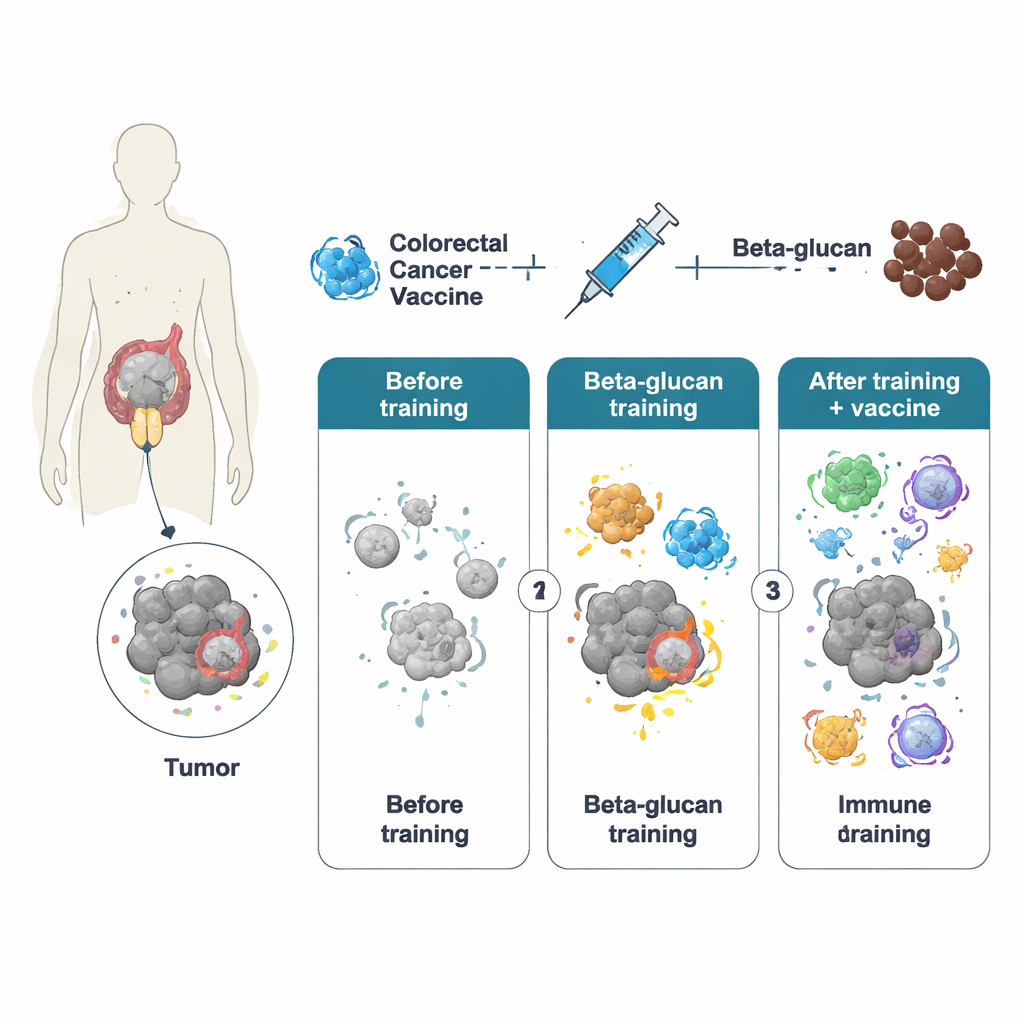
Перепрограммирование энергии и коммуникации внутри опухолей
Углубившись, исследователи выделили иммунные клетки из опухолей и профилировали их метаболизм и активность генов поодиночке. Оказалось, что тренированные макрофаги переключались в высокоактивный метаболический режим, напоминающий «эффект Варбурга», при котором клетки быстро распознают и сжигают сахар, перенаправляя ресурсы на синтез строительных блоков для роста и функции. Эти клетки также усиливали креатиновый обмен — более известный по спортивным добавкам — что помогало обеспечивать дополнительную энергию, необходимую для выработки провоспалительных молекул. Одновременно специфические химические метки на белках, связанных с ДНК (в частности, увеличение H3K4me3), отмечали гены, вовлечённые в выработку хемокинов, фактически закрепляя прогенераторную, противоопухолевую программу, которая сохранялась во времени.
Создание имунной эстафеты
Секвенирование отдельных клеток выявило поэтапную эстафету между разными иммунными клетками внутри опухоли. Сначала тренированные макрофаги выделяли высокие уровни двух ключевых сигналов — CXCL9 и CXCL10 — которые привлекали натуральные киллеры (NK‑клетки) через рецептор CXCR3. Привлечённые таким образом NK‑клетки не только убивали раковые клетки; они также секретировали другой посредник, CCL5, привлекавший специализированный поднабор дендритных клеток, известный как cDC1. Эти дендритные клетки особенно хорошо презентуют фрагменты опухоли Т‑клеткам. В результате больше CD8‑Т‑клеток активировалось и переходило в эффекторные клетки памяти — клетки, которые отвечают быстро и решительно при повторной встрече с опухолью. Блокирование использования креатина, истощение макрофагов или NK‑клеток, а также прерывание этих хемокиновых путей ослабляло контроль над опухолью, подчёркивая, насколько успех вакцины зависел от этой цепочки макрофаг–NK–дендритная клетка–Т‑клетка. 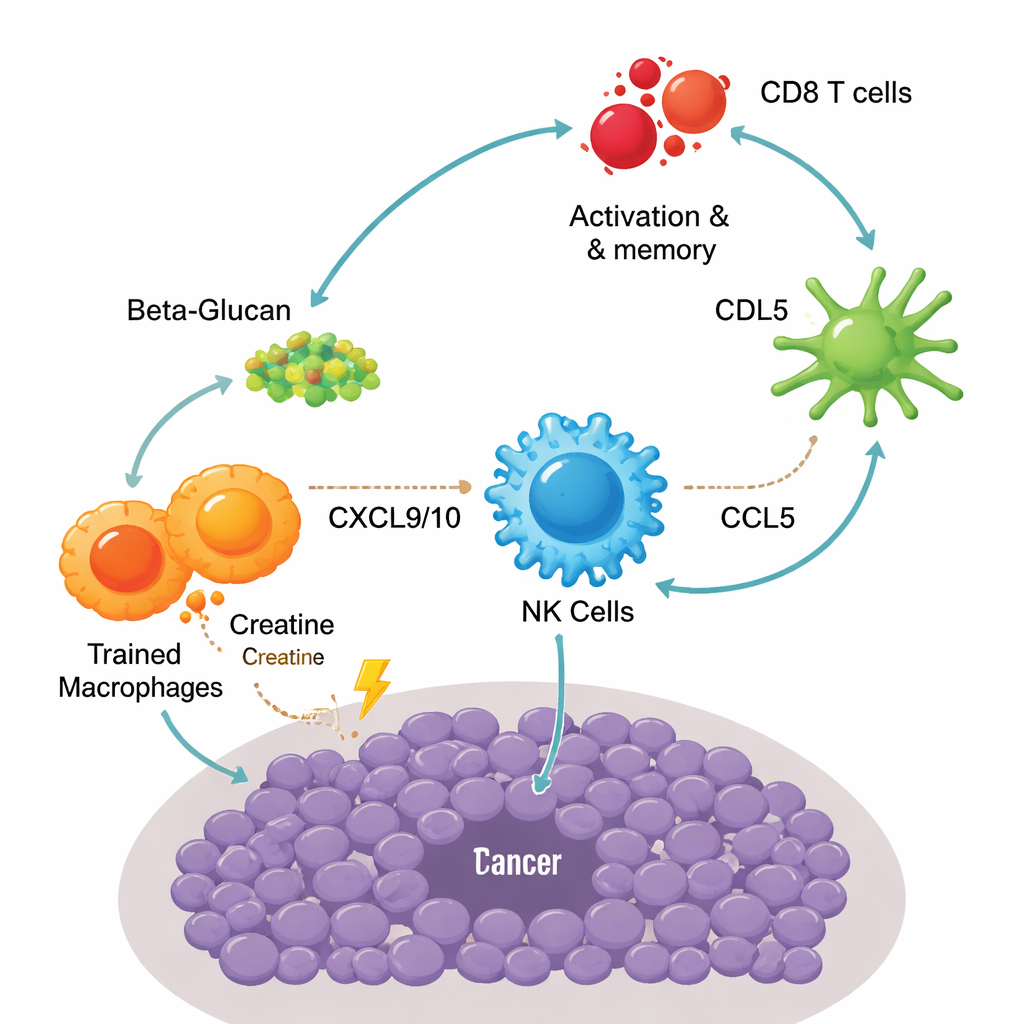
От мышиных моделей к человеческим органоидам опухолей
Команда протестировала подход в нескольких мышиных моделях колоректального рака, включая особенно устойчивый тип, резистентный к обычным иммунотерапиям. В каждом случае сочетание тренировки бета‑глюканом и вакцины замедляло рост опухоли эффективнее, чем любое из лечений по отдельности. Важно, что исследование вышло за пределы мышей: человеческие клетки крови, подвергнутые воздействию бета‑глюкана, лучше реагировали на пептид вакцины против колоректального рака, вырабатывая больше иммуностимулирующих цитокинов. Когда эти тренированные иммунные клетки расширяли и совместно культивировали с миниатюрными опухолями, полученными от пациентов (органыиды), они уничтожали больше раковых клеток, чем нетренированные клетки. Удаление человеческих моноцитов и макрофагов из системы стирало этот эффект, подтверждая, что именно эти тренированные клетки выступают ключевыми организаторами, а не прямыми исполнителями убийства опухолевых клеток.
Что это может значить для будущих вакцин против рака
Проще говоря, работа демонстрирует, что безопасный сахар, получаемый из дрожжей, может «наставлять» врожденные иммунные клетки, чтобы поддержать более эффективную вакцинацию против колоректального рака. Перепрограммируя то, как макрофаги используют энергию и какие гены у них остаются готовыми к действию, тренировка бета‑глюканом запускает эффект домино: макрофаги призывают NK‑клетки, NK‑клетки привлекают экспертные дендритные клетки, и вместе они формируют более мощную армию клеток памяти CD8. Хотя многое ещё предстоит проверить в клинических испытаниях — в том числе безопасность, оптимальное время и лучшие комбинации вакцин — тренированный иммунитет здесь выступает перспективной адъювантной стратегией, способной превратить «холодные», иммуносупрессивные колоректальные опухоли в те, которые иммунная система сможет распознать и контролировать.
Цитирование: Hamdan, F., Gandolfi, S., D’Alessio, F. et al. Leveraging glucan-induced trained immunity for the epigenetic and metabolic rewiring of macrophages to enhance colorectal cancer vaccine response. Nat Commun 17, 1757 (2026). https://doi.org/10.1038/s41467-026-68466-5
Ключевые слова: иммунотерапия колоректального рака, тренированный иммунитет, бета-глюкан, макрофаги и NK-клетки, вакцины против рака