Clear Sky Science · ru
In vivo CRISPR-скрининг выявляет члены комплекса SAGA как ключевые регуляторы гемопоэза
Почему важно поддерживать баланс кроветворения
Каждый день ваш организм тихо производит сотни миллиардов новых клеток крови, которые переносят кислород, борются с инфекциями и останавливают кровотечение. Эта непрерывная продукция опирается на редкие «материнские» клетки в костном мозге, называемые кроветворными стволовыми клетками. Когда механизмы контроля этих клеток дают сбой, у людей может развиться анемия, ослабление иммунитета или рак, например лейкемия. В этом исследовании задают простой, но мощный вопрос: среди тысяч генов в нашем геноме какие действительно необходимы, чтобы поддерживать здоровое и сбалансированное кроветворение?
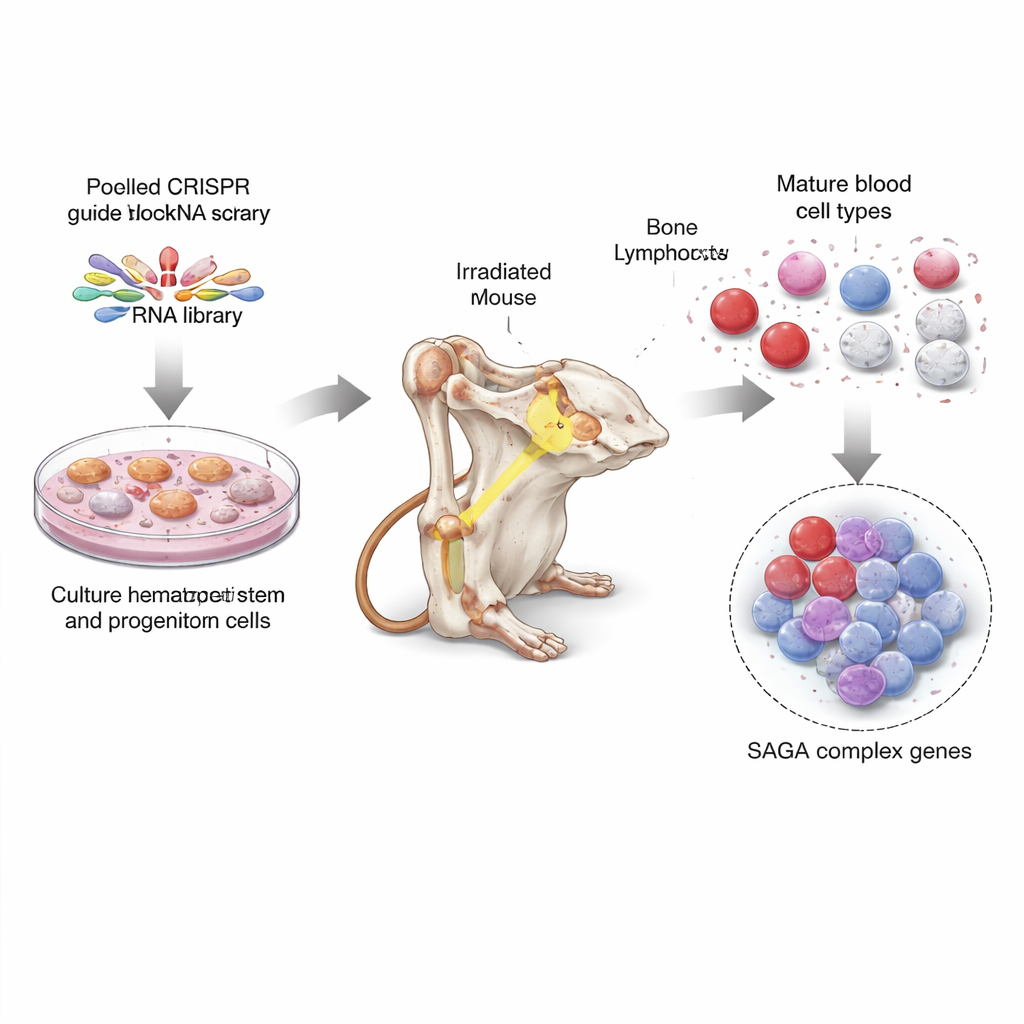
Геномная охота за сокровищами в стволовых клетках мыши
Для этого исследователи использовали CRISPR — инструмент редактирования генома, часто сравниваемый с молекулярными ножницами — чтобы выключить почти каждый ген в геноме мыши, по десять направляющих РНК на каждый ген. Сначала они вырастили большое число стволовых и предшественниковых клеток костного мозга в специальных условиях культивирования, затем инфицировали эти клетки пулом направляющих CRISPR так, чтобы в каждой клетке был нокаут разного гена. Далее они пересадили эту смесь отредактированных клеток десяткам облучённых мышей, позволив им восстановить кровеносную систему животных. Через несколько месяцев исследователи очистили различные зрелые типы клеток крови и клеток, похожих на стволовые, из костного мозга и проанализировали, какие направляющие CRISPR оказались избыточно или недостаточно представлены. Это показало, какие потери генов способствуют накоплению незрелых клеток, а какие поддерживают образование полностью сформированных клеток крови.
В фокусе скрытый центр управления — комплекс SAGA
Среди многих известных регуляторов кроветворения всплыл неожиданный набор мишеней: несколько структурных компонентов крупного белкового комплекса под названием SAGA, включая гены Tada2b, Taf5l и Tada1. SAGA не производит клетки крови напрямую; он помогает включать или выключать другие гены, химически помечая белки, упаковывающие ДНК, — гистоны. Когда команда по отдельности выводила из строя эти компоненты SAGA и пересаживала отредактированные клетки мышам, наблюдалась последовательная картина. Незрелые клетки костного мозга накапливались, но их способность созревать в циркулирующие лейкоциты, эритроциты и некоторые иммунные клетки резко снижалась. По сути, стволовые и предшественниковые клетки застревали в «бутылочном горлышке», не проходя путь до полноценно функционирующих клеток крови.
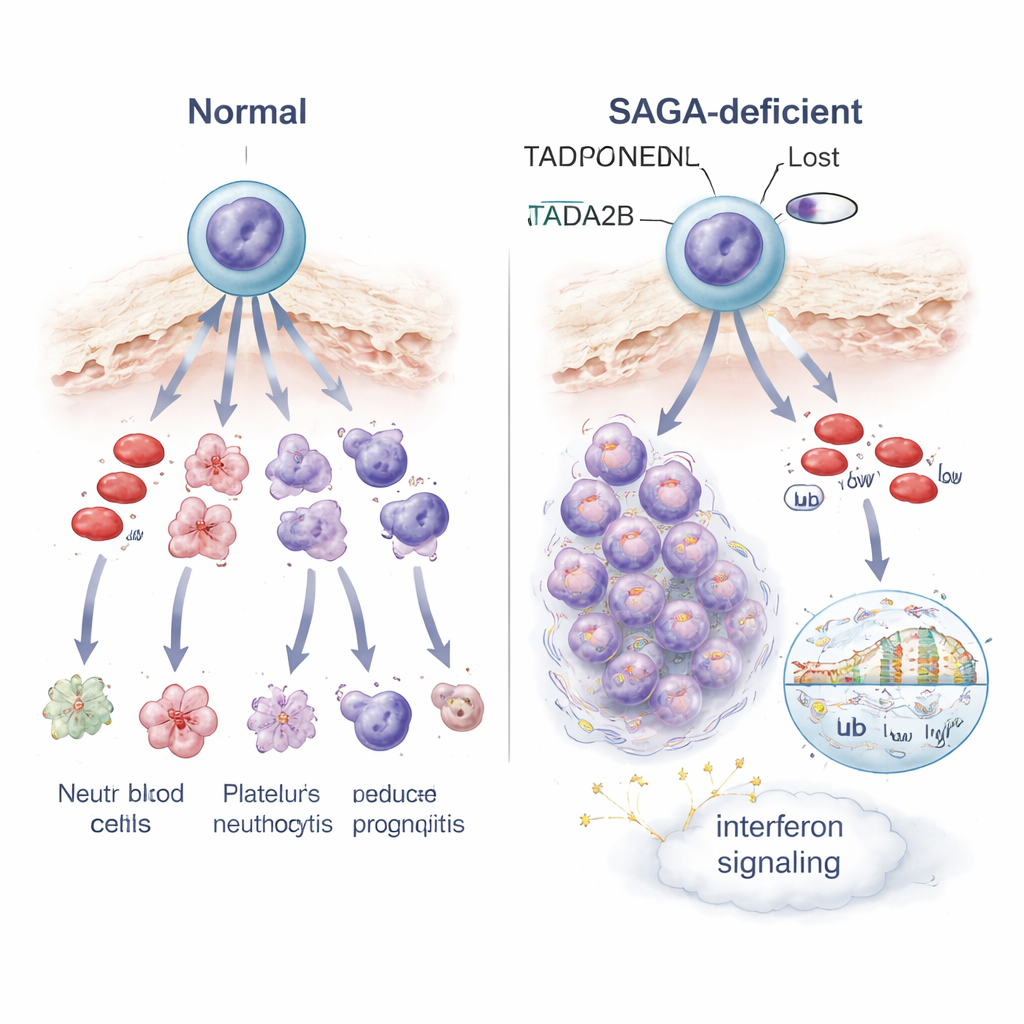
Как нарушение контроля генов меняет судьбу клеток и сигналы стресса
Чтобы понять, что идёт не так внутри этих блокированных клеток, учёные профилировали активность генов по одной клетке и в массе. Потеря Tada2b или Taf5l перенастраивала активность множества генов в стволовых клетках, с двумя ярко выраженными темами. Во-первых, были включены гены, участвующие в интерферонной сигнализации — обычно части антивирусной защиты организма — что указывает на внутренний сигнал тревоги или стрессовое состояние. Во-вторых, митохондрии клеток, крошечные энергетические станции, стали менее активны, и изменённые клетки стали более чувствительны к препарату, направленному на митохондриальное производство энергии. На уровне упаковки ДНК клетки без Tada2b показали снижение уровня гистоновой метки, связанной с открытой, активной хроматином, и изменения в другой метке, влияющей на то, как считываются гены. Эти изменения в химии хроматина, вероятно, помогают объяснить, почему многие гены, в том числе управляющие нормальным созреванием крови, оказываются неправильно регуляционными.
От основных механизмов к моделям заболеваний
Затем команда спросила, можно ли вернуть эти эффекты, изменив активность SAGA вверх или вниз. Принудительная экспрессия дополнительного Tada2b снижала активность интерферон-ассоциированных генов и уменьшала долю стволоподобных клеток — зеркальное отражение фенотипа нокаута. Лечение нормальных стволовых клеток препаратом, ингибирующим ключевые ферментативные субъединицы SAGA, воспроизвало большую часть сигнатуры потери Tada2b, что усиливает идею о центральной роли хроматин-модифицирующей активности SAGA. Наконец, исследователи обратились к модели человеческих клеток миелодиспластического синдрома, предлейкемического расстройства, при котором кроветворение ухудшается, а пути интерферона часто активированы. Когда они выводили из строя компоненты SAGA в этих человеческих клетках и пересаживали их иммунодефицитным мышам, отредактированные клетки получали преимущество в росте и снова активировали интерферонные и миелоидные генетические программы, что указывает на то, что этот регуляторный узел также формирует поведение заболевания.
Что это значит для здоровья крови и будущих терапий
Для непрофессионального читателя основная мысль такова: это исследование выявляет мощный центр управления — комплекс SAGA — который помогает кроветворным стволовым клеткам решать, когда оставаться незрелыми, когда созревать и как избегать вредных стрессовых ответов. Когда ключевые части SAGA отсутствуют, стволовые клетки накапливаются, но не способны производить достаточное количество работоспособных клеток крови, при этом усиливаются стрессовые и анти-вирусоподобные сигналы, а митохондрии дают сбои. Эти открытия не только углубляют наше понимание того, как поддерживается здоровое кроветворение в течение жизни, но и намекают, что тонкие изменения активности SAGA могут способствовать возрастным проблемам крови и расстройствам, таким как миелодиспластический синдром. В долгосрочной перспективе картирование этой цепи управления может помочь учёным разработать терапии, которые подтолкнут повреждённые стволовые клетки к восстановлению сбалансированного и устойчивого кроветворения.
Цитирование: Shankar, A., Olender, L., Hsu, I. et al. In vivo CRISPR screening identifies SAGA complex members as key regulators of hematopoiesis. Nat Commun 17, 1756 (2026). https://doi.org/10.1038/s41467-026-68465-6
Ключевые слова: гемопоэтические стволовые клетки, CRISPR-скрининг, комплекс SAGA, интерферонная сигнализация, миелодиспластический синдром