Clear Sky Science · ru
Вывод архитектуры хроматина в одном локусе методом вероятностной in situ локализации ДНК
Как 3D‑форма ДНК контролирует включение генов
ДНК обычно представляют как прямую лестницу, но внутри клеток она складывается в сложные петельные и спиральные структуры. Эти формы важны: они помогают определить, какие гены включаются, когда и где. В этом исследовании предложен новый способ изучения крошечных 3D‑расположений ДНК вокруг одного гена в развивающихся эмбрионах дрозофилы, который показывает, как тонкие изменения в укладке ДНК могут менять паттерны активности генов, формирующие план тела.
Наблюдение за контролем генов в развивающемся эмбрионе
В ходе развития эмбриона тысячи генов должны включаться и выключаться в точно заданные моменты. Многие из этих решений принимают короткие участки ДНК — энхансеры, которые могут располагаться в десятках тысяч пар оснований от управляемого ими гена. Для работы энхансеры должны физически сближаться со своей целью в 3D‑пространстве, формируя петли, при которых удалённые участки соприкасаются. Но эти петли малы, динамичны и трудноуловимы. Авторы сосредоточились на одном гене, brinker (brk), у дрозофилы Drosophila. Этот ген участвует в паттернинге раннего эмбриона, включаясь полосой вдоль стороны яйца. Три соседних регуляторных элемента — два энхансера (E1 и E2) и элемент, расположенный рядом с промотором (PPE) — взаимодействуют, чтобы создать этот точный узор.
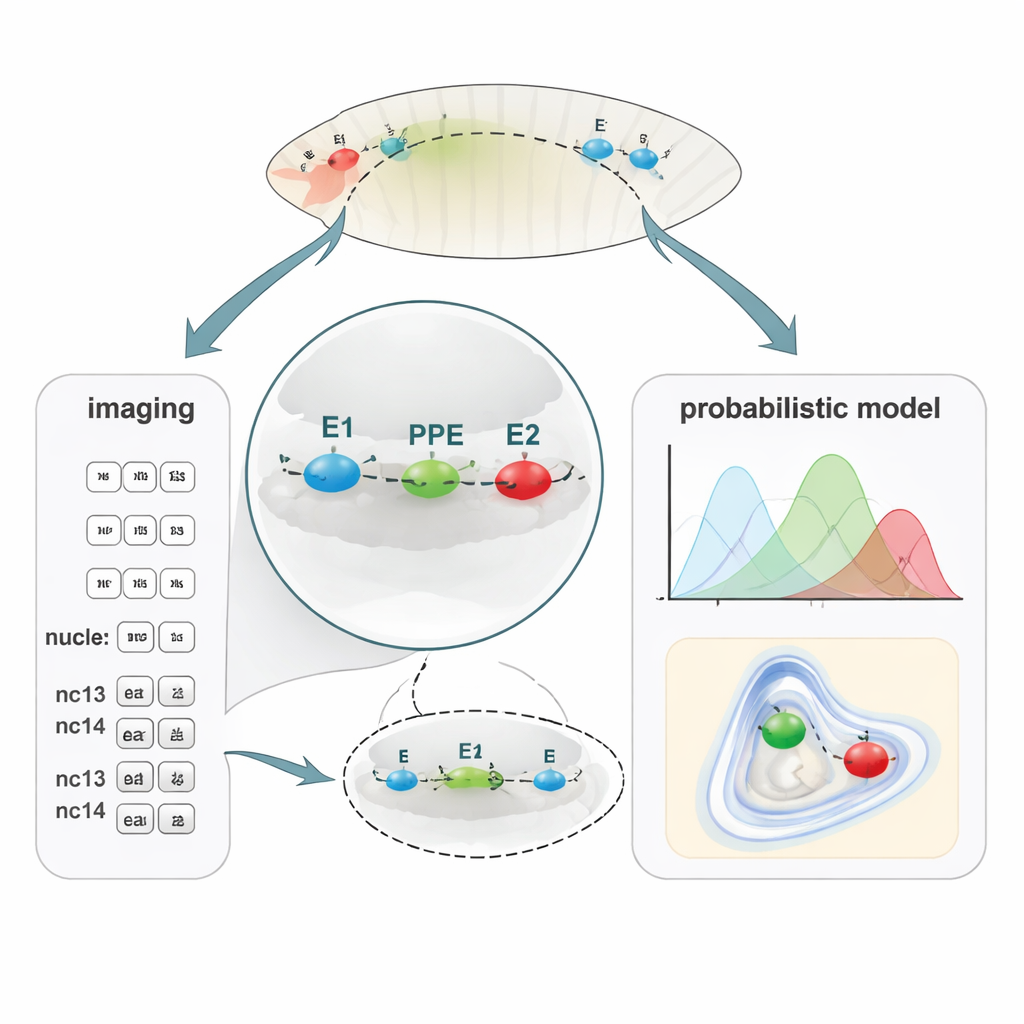
Новый способ картирования крошечных ДНК‑расстояний
Чтобы связать укладку ДНК с активностью гена, команда разработала PLOTTED (Probabilistic Localization of Oligopaint Tagged Target Element Distances). Сначала они использовали метод маркировки ДНК Oligopaint FISH, чтобы прикрепить три разных флуоресцентных метки к регионам E1, PPE и E2 в фиксированных эмбрионах мух. С помощью сверхразрешающего конфокального микроскопа они измеряли 3D‑расстояния между этими тремя цветными пятнами в десятках тысяч ядер в эмбрионах на последовательных ядерных циклах — от незадолго до начала активности гена (pre‑nc13) до более поздних стадий (nc13 и nc14). Затем все эти расстояния пропускались через собственный вычислительный конвейер, который отбрасывает шумные измерения и строит вероятностные карты, показывающие, где каждый элемент наиболее вероятно располагается относительно других. Вместо одной статичной «петли» PLOTTED создает ландшафт вероятных форм хроматина на каждой стадии развития.
Когда ДНК уплотняется, ген просыпается
В нормальных эмбрионах исследователи обнаружили, что по достижении ядерного цикла 13 оба энхансера сближаются с PPE: локальная ДНК‑окрестность вокруг гена brk становится более компактной. После этого расстояния между тремя элементами остаются относительно стабильными. Важно, что это временное совпадение соответствует началу экспрессии brk, что указывает на то, что уплотнение конфигурации ДНК помогает гену включиться. PLOTTED также показал, что компактная конфигурация чаще встречается в областях эмбриона, где brk активен, а более развернутые конфигурации доминируют там, где ген репрессирован, что подтверждает связь между 3D‑архитектурой и транскрипцией.
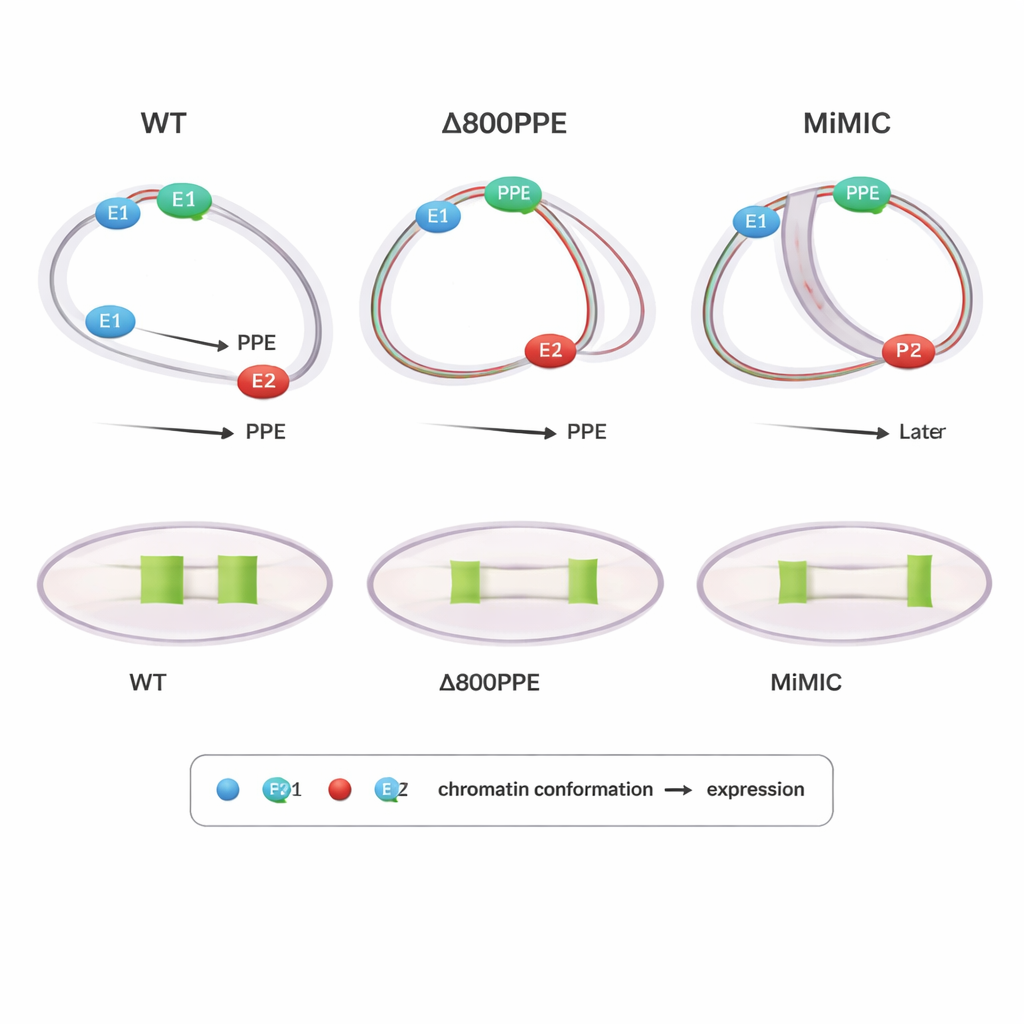
Мутации показывают, почему важны время и партнёры
Чтобы проверить причинно‑следственные связи, авторы исследовали мух с инженерными изменениями в локусе brk. В одном мутанте удалили 800 пар оснований PPE, ослабив этот центральный элемент; в другом между E1 и PPE вставили кассету длиной 7,3 килобазы (MiMIC), фактически раздвинув их и добавив дополнительный промотор. Оба мутанта демонстрировали отложенную или сниженную экспрессию brk. PLOTTED показал, почему: в линии с делецией PPE уплотнение расстояний между PPE и обоими энхансерами происходило позже обычного, а на поздних стадиях PPE оставался слишком близко к E1, мешая E2 формировать широкую картину экспрессии, характерную для дикого типа. В линии MiMIC PPE ассоциировался слишком рано и сильно с E2 и лишь позже сближался с E1, вновь нарушая нормальную передачу между энхансерами. Эти результаты показывают, что важно не только то, собираются ли элементы вместе, но и когда это происходит и с каким партнёром они наиболее близки — это критично для правильного уровня генной активности.
Укладка ДНК варьирует по всему эмбриону
Поскольку PLOTTED сохраняет пространственную информацию внутри целых эмбрионов, команда могла также проверить, различается ли архитектура ДНК в разных областях тела. Сравнивая латеральные зоны, где brk активен, с вентральными зонами, где он репрессирован, они обнаружили, что три элемента находятся ближе друг к другу в активных областях и дальше разнесены в репрессированных доменах. По оси голова‑хвост наблюдалось, что расстояния E1–PPE изменяются по‑разному в передней и задней частях эмбриона, намекая на то, что региональные сигналы настраивают архитектуру хроматина для тонкой регулировки паттернов экспрессии генов. Эти результаты поддерживают представление о том, что 3D‑расположение регуляторной ДНК зависит от контекста, отслеживая и время, и положение в развивающемся организме.
Почему это важно за пределами дрозофилы
Проще говоря, исследование показывает, что то, как ДНК складывается вокруг одного гена, тесно связано с тем, когда и где этот ген включается. Новый метод PLOTTED предоставляет практичный способ картирования этих крошечных ДНК‑окрестностей в целых тканях с использованием широко доступных микроскопов и относительно простой химии в сочетании с мощным вероятностным моделированием. Хотя метод продемонстрирован на эмбрионах мушки, подход применим ко многим организмам и моделям заболеваний. По мере того как учёные всё чаще обнаруживают, что неправильная укладка хроматина лежит в основе нарушений развития и рака, такие инструменты, как PLOTTED, помогут выяснить, как небольшие смещения в 3D‑раскладке энхансеров и генов могут приводить к крупным изменениям судьбы клеток и здоровью.
Цитирование: Le, M.T., McGehee, J., Dunipace, L. et al. Inferring chromatin architecture at a single locus through probabilistic in situ DNA localization. Nat Commun 17, 1752 (2026). https://doi.org/10.1038/s41467-026-68460-x
Ключевые слова: архитектура хроматина, взаимодействия энхансер-промотор, эмбриогенез Drosophila, регулирование генов, сверхразрешающая микроскопия