Clear Sky Science · ru
DKK1 и NEDD4, происходящие из нервного гребня, модулируют Wnt‑сигнализацию во втором сердечном поле, чтобы координировать развитие выводного тракта сердца
Почему важны крошечные строители сердца
Сердце раннего эмбриона начинается как простая трубка, но ему предстоит быстро перестроиться в сложный орган, который разгоняет кровь и по телу, и в легкие. Незначительные сбои в этом процессе формирования могут вызывать серьёзные врождённые дефекты, в том числе состояния, требующие хирургического вмешательства вскоре после рождения. В этом исследовании показано, как две популяции клеток взаимодействуют при формировании главного выходного пути сердца, и выявлена молекулярная ошибка, которая может способствовать врождённым порокам сердца у мышей и у людей.
Две команды, строящие «выезд» сердца
Часть сердца, по которой кровь выходит из желудочков — выводной тракт — формируется из области, называемой вторым сердечным полем. Клетки здесь должны сохранять гибкое «прогениторное» состояние достаточно долго, чтобы пополнять растущий выводной тракт, а затем вовремя переключаться в зрелую мышечную форму. Рядом с ними мигрируют клетки нервного гребня — подвижная популяция, помогающая формировать крупные артерии и клапаны. Ранние работы намекали, что клетки нервного гребня как‑то влияют на второе сердечное поле, но механизм этого диалога оставался неизвестным. 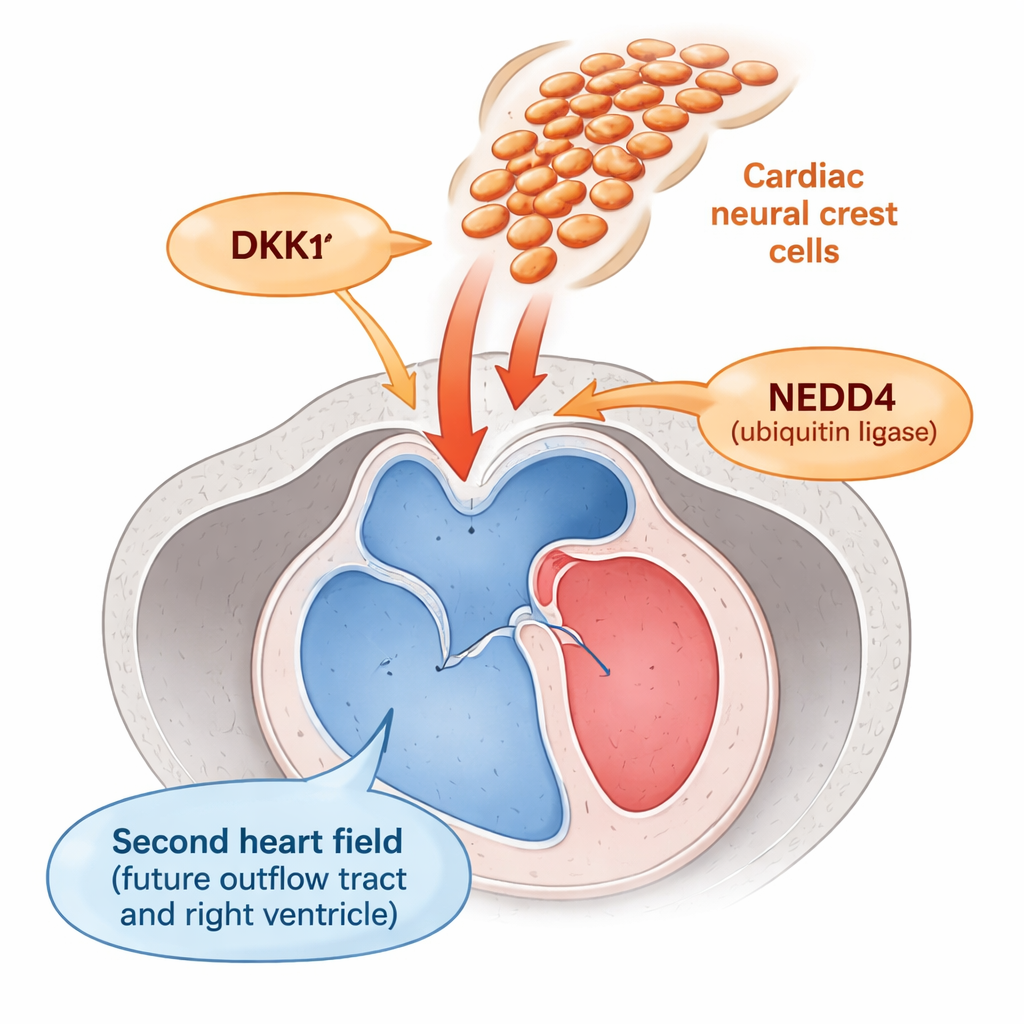
Молекулярный регулятор интенсивности сигнала роста
Авторы обнаружили, что клетки нервного гребня действуют как регулятор интенсивности (димер‑выключатель) ключевого сигнала роста Wnt, который поддерживает деление прогениторов и задерживает их созревание. Они показали, что клетки нервного гребня являются главным источником DKK1 — небольшого секретируемого белка, который подавляет Wnt‑сигнализацию в соседних клетках. Сам DKK1 обычно контролируется белком NEDD4, который помечает DKK1 для утилизации. У эмбрионов мышей, у которых Nedd4 был удалён специально в клетках нервного гребня, DKK1 накапливался до аномально высокого уровня. Избыток DKK1 снижал активность Wnt в соседнем втором сердечном поле, что подтверждалось уменьшением ядерного бета‑катенина — стандартного индикатора Wnt‑сигнализации — и пониженным уровнем нескольких Wnt‑ответных генов.
Когда нарушается тайминг, страдает геометрия сердца
Избыток DKK1 и дефицит Wnt имели очевидное следствие: клетки второго сердечного поля начинали преждевременно превращаться в сердечную мышцу. Маркеры зрелой мышцы появлялись раньше в этой зоне прогениторов, и оставалось меньше недифференцированных клеток для удлинения выводного тракта. Отслеживая делящиеся клетки со временем, исследователи показали, что в мутантов в выводной тракт попадало меньше клеток второго сердечного поля. В результате выводной тракт был короче и неправильно повернут, что приводило к несоответствию между крупными артериями и желудочками. Эти структурные нарушения напоминали конотрункальные дефекты у людей, такие как двойной выезд правого желудочка, и сходные пороки, наблюдаемые при полном нокауте Nedd4 у мышей.
Подтверждение роли сигнала и связь с человеческим заболеванием
Чтобы подтвердить, что именно изменённая Wnt‑сигнализация вызывает эти проблемы, исследователи подправляли путь с помощью препаратов у беременных мышей. Блокирование Wnt в иначе здоровых эмбрионах приводило к тем же преждевременным дифференцировкам и дефектам поворота, что и потеря Nedd4, тогда как уменьшение дозы гена Dkk1 на фоне дефицита Nedd4 частично восстанавливало размер и поворот выводного тракта. Наконец, команда выявила ребёнка с тетрадой Фалло, у которого была редкая наследуемая вариация в NEDD4, ослаблявшая его способность помечать DKK1 для разрушения. Мыши, созданные с той же вариантом Nedd4, развивали правосторонние дефекты стенки и перегородок сердца, что поддерживает идею о том, что нарушенный контроль NEDD4–DKK1 может вносить вклад в человеческие врождённые пороки сердца. 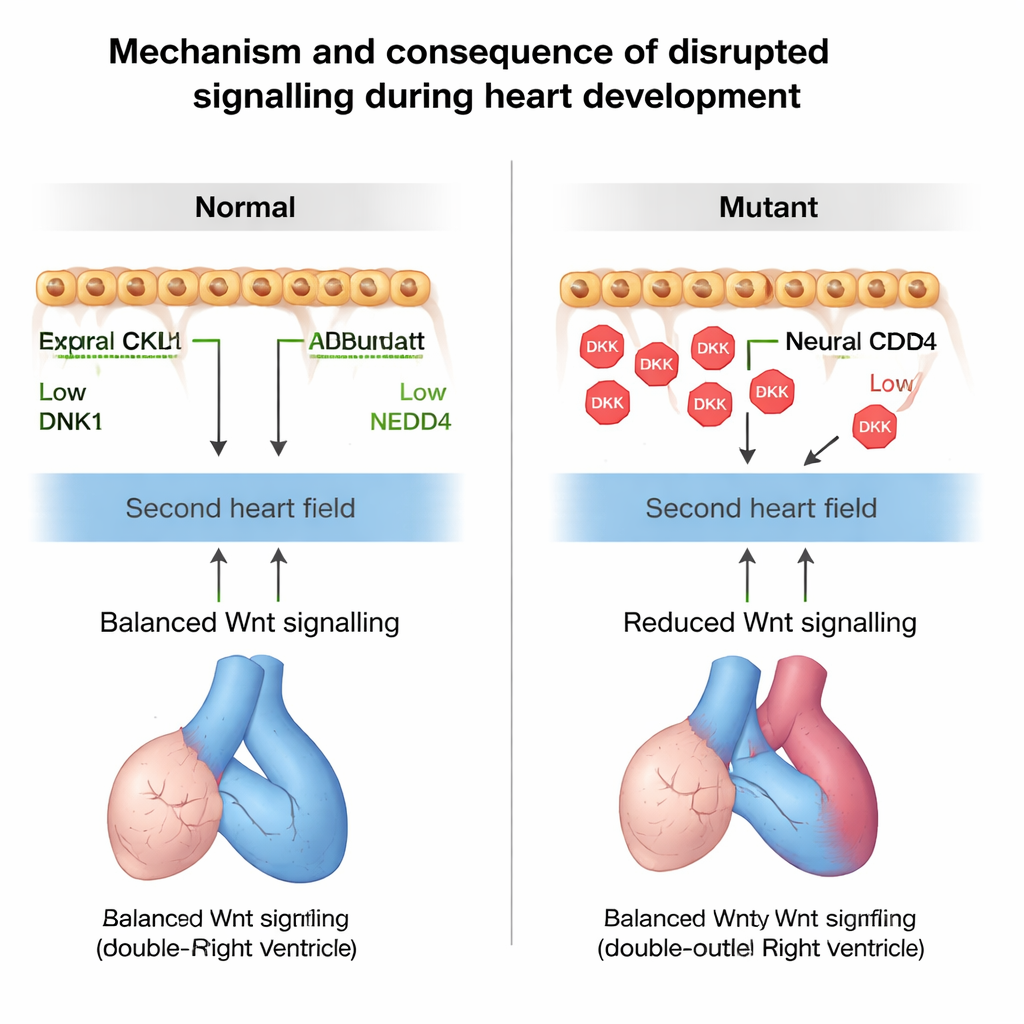
Что это означает для понимания пороков сердца
Для неспециалистов главный вывод таков: «выезд» сердца зависит от точного тайминга того, когда его строительные блоки прекращают делиться и начинают превращаться в мышцу. Этот тайминг регулируется не только внутри самого сердечного поля, но и соседними клетками нервного гребня, которые тонко настраивают сигнал роста через пару NEDD4–DKK1. Когда этот молекулярный регулятор оказывается чрезмерно «выключенным», выводной тракт недобирает и неверно выстраивается, что приводит к серьёзным врождённым дефектам. Прослеживание этого пути и установление связи с человеческим генетическим вариантом даёт новые подсказки о том, как возникают некоторые врождённые пороки сердца, и выделяет потенциальные молекулярные мишени для будущей диагностики или вмешательства.
Цитирование: Wiszniak, S., Alankarage, D., Lohraseb, I. et al. Neural crest cell-derived DKK1 and NEDD4 modulate Wnt signalling in the second heart field to orchestrate outflow tract development. Nat Commun 17, 1751 (2026). https://doi.org/10.1038/s41467-026-68459-4
Ключевые слова: врожденный порок сердца, развитие сердца, клетки нервного гребня, Wnt‑сигнализация, сердечный выводной тракт