Clear Sky Science · ru
Функциональные варианты в 1p36.23 повышают риск шизофрении через модуляцию RERE
Почему крошечные изменения ДНК важны для психического здоровья
Шизофрения — серьёзное психическое заболевание, которое влияет на мышление, чувства и способы взаимодействия с другими. Оно сильно наследуется, но большинство вовлечённых генетических изменений — это небольшие, разбросанные правки в нашей ДНК. В этом исследовании подробно рассматривается один такой участок генома и по шагам показывается, как два тонких варианта ДНК могут изменять развитие и коммуникацию нервных клеток таким образом, что это может повышать риск шизофрении. 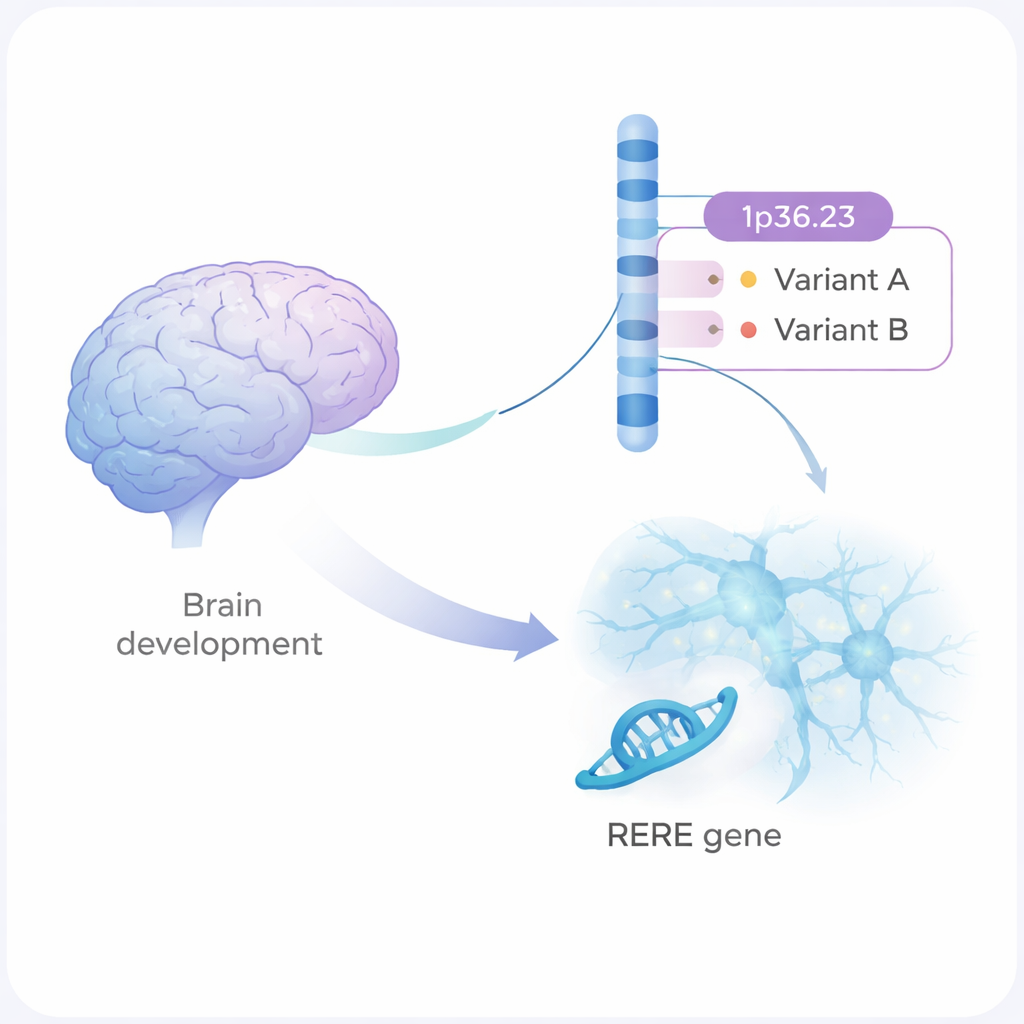
Генетический горячий участок на хромосоме 1
Крупные генетические исследования указали более 300 участков человеческого генома, связанных с шизофренией. Один из них — участок ДНК на хромосоме 1, обозначаемый как 1p36.23. До сих пор учёные не знали, какие именно изменения в этом регионе, или какой ген, действительно ответственны. Авторы объединили статистическую генетику с лабораторными экспериментами и выделили два варианта ДНК — rs159961 и rs301792 — расположенные внутри гена RERE. Эти варианты не изменяют сам белок RERE; они находятся в регуляторных «переключателях» внутри гена, которые контролируют, насколько сильно включается RERE.
Как риск‑варианты увеличивают активность RERE
Команда сначала проверила, действуют ли эти два варианта как функциональные переключатели. С помощью репортёрных анализов — тестов, где фрагмент ДНК приводит в действие ген, производящий свет — они показали, что версии rs159961 и rs301792, связанные с шизофренией, ведут себя как более сильные энхансеры (усилители) в нервоподобных клетках, но не в нерелевантных типах клеток. Биохимические тесты связывания объяснили, почему: риск‑форма одного варианта ослабляет связывание REST — белка, который обычно подавляет активность генов, в то время как риск‑форма другого усиливает связывание POLR2A — ключевого компонента аппарата считывания генов. В сумме эти изменения в белковом связывании увеличивают активность элементов‑энхансеров и поднимают экспрессию RERE.
От повышенного RERE к изменённому росту нервных клеток
Далее исследователи выяснили, что даёт избыток RERE в мозге. Они обнаружили, что у людей, умерших от шизофрении, уровни RERE в тканях мозга были выше по сравнению с контролями. Чтобы смоделировать это, они искусственно повысили уровень RERE в нейрональных стволовых клетках мыши — незрелых клетках, дающих начало нейронам и глии. При избыточной продукции RERE эти стволовые клетки реже делились, застревали на поздней стадии клеточного цикла и давали меньше зрелых нейронов, тогда как другие типы клеток в основном не менялись. В культуре нейронов избыток RERE также менял их ветвление и уменьшал количество и тип маленьких выростов — дендритных шипиков, где формируются синапсы. Эти изменения соответствуют давним данным о нарушённом развитии мозга и потере шипиков при шизофрении. 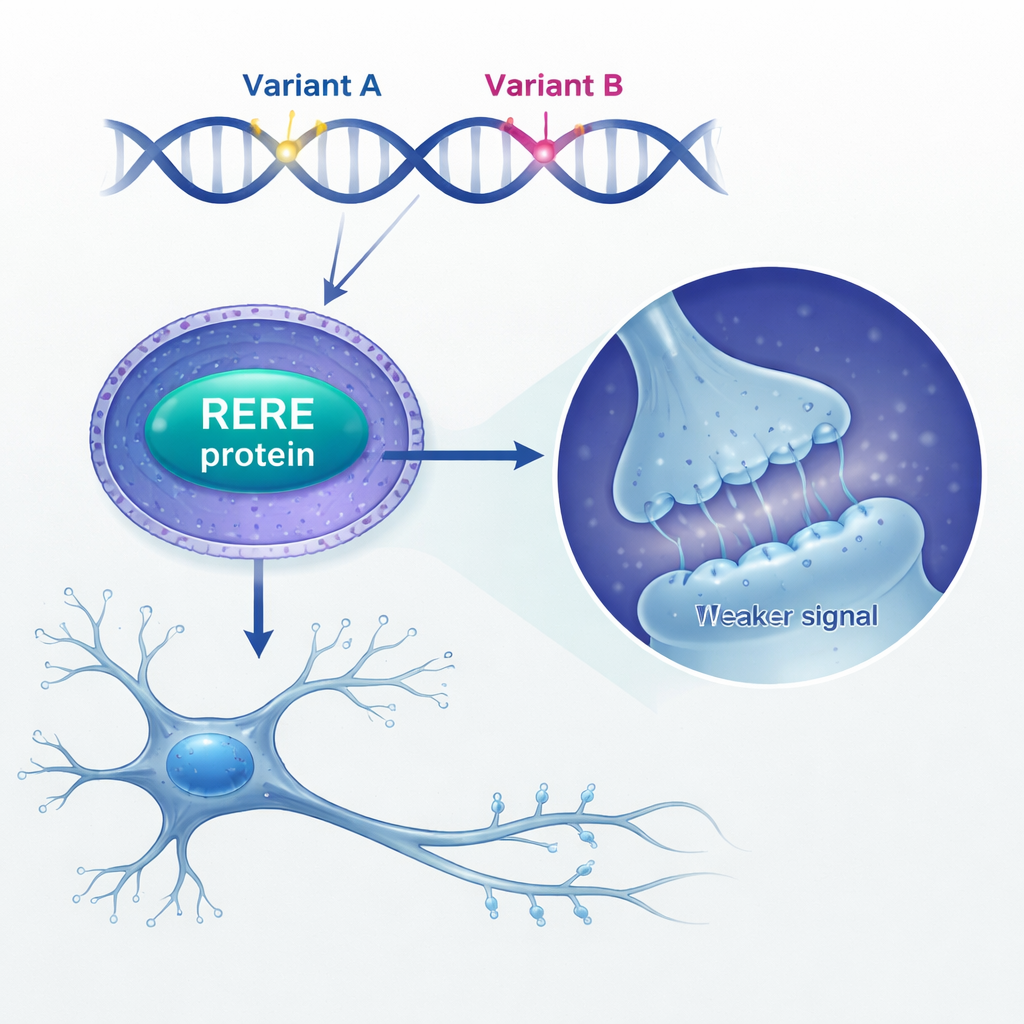
Нарушение «разговора» головного мозга на глутамате
При более тщательном изучении активности генов команда обнаружила, что сверхэкспрессия RERE нарушает сети генов, вовлечённых в рост дендритов и основные системы химической передачи, особенно глутаматный путь. Выделился один ключевой мишень: ген GRIN2A, кодирующий важный субъюнит (GluN2A) NMDA‑типных глутаматных рецепторов, давно связанных со шизофренией. Авторы показали, что RERE в партнёрстве с двумя другими ядерными белками, RARB и RXRA, напрямую связывается с промотором GRIN2A и подавляет его активность. В нейронах с избытком RERE уровни GluN2A падали, а электрические записи показали ослабление синаптических токов, опосредованных NMDA‑рецепторами, хотя частота синаптических событий не изменилась. Иными словами, «громкость» отдельных возбуждающих сигналов была уменьшена.
Связь вариантов ДНК с работой мозга
Связывая генетику, молекулярную биологию, клеточные культуры и электрофизиологию, эта работа выстраивает ясную причинно‑следственную цепочку: риск‑варианты ДНК в 1p36.23 усиливают регуляторные элементы внутри гена RERE, приводя к повышению экспрессии RERE в клетках мозга. Повышенный RERE, в свою очередь, нарушает рост и созревание нейронов, изменяет форму и число их синаптических шипиков и ослабляет глутаматную сигнализацию через NMDA‑рецепторы — особенно содержащие GluN2A. Для непрофессионального читателя основной вывод таков: очень небольшие изменения в ДНК могут слегка сдвинуть активность одного гена, и на уровне многих нервных клеток и в течение многих лет это способно подвинуть развитие и коммуникацию мозга в сторону, способствующую возникновению шизофрении.
Цитирование: Liu, Y., Wang, J., Yang, H. et al. Functional variants at 1p36.23 confer risk of schizophrenia through modulating RERE. Nat Commun 17, 1742 (2026). https://doi.org/10.1038/s41467-026-68449-6
Ключевые слова: генетика шизофрении, ген RERE, нейроразвитие, глутаматная сигнализация, синаптическая функция