Clear Sky Science · ru
Улучшение эректильной функции у диабетических самцов мышей посредством восстановления депальмитоилированного FBP1 для снижения лактата в кавернозной ткани
Почему это важно для мужчин с диабетом
Эректильные нарушения часто встречаются у мужчин с диабетом: они нередко проявляются раньше и хуже реагируют на обычные таблетки вроде Виагры. В исследовании на мышах выявлена неожиданная причина: накопление молочной кислоты (лактата) в ткани, формирующей эрекцию. Авторы не только проследили, как это накопление повреждает ткань, но и опробовали экспериментальную РНК‑терапию, доставляемую в крошечных жировых пузырьках, которая восстанавливает эректильную функцию. Работа наводит на мысль, что в будущем лечение диабетической эректильной дисфункции может сводиться к исправлению метаболизма, а не только к кратковременному увеличению кровоснабжения.
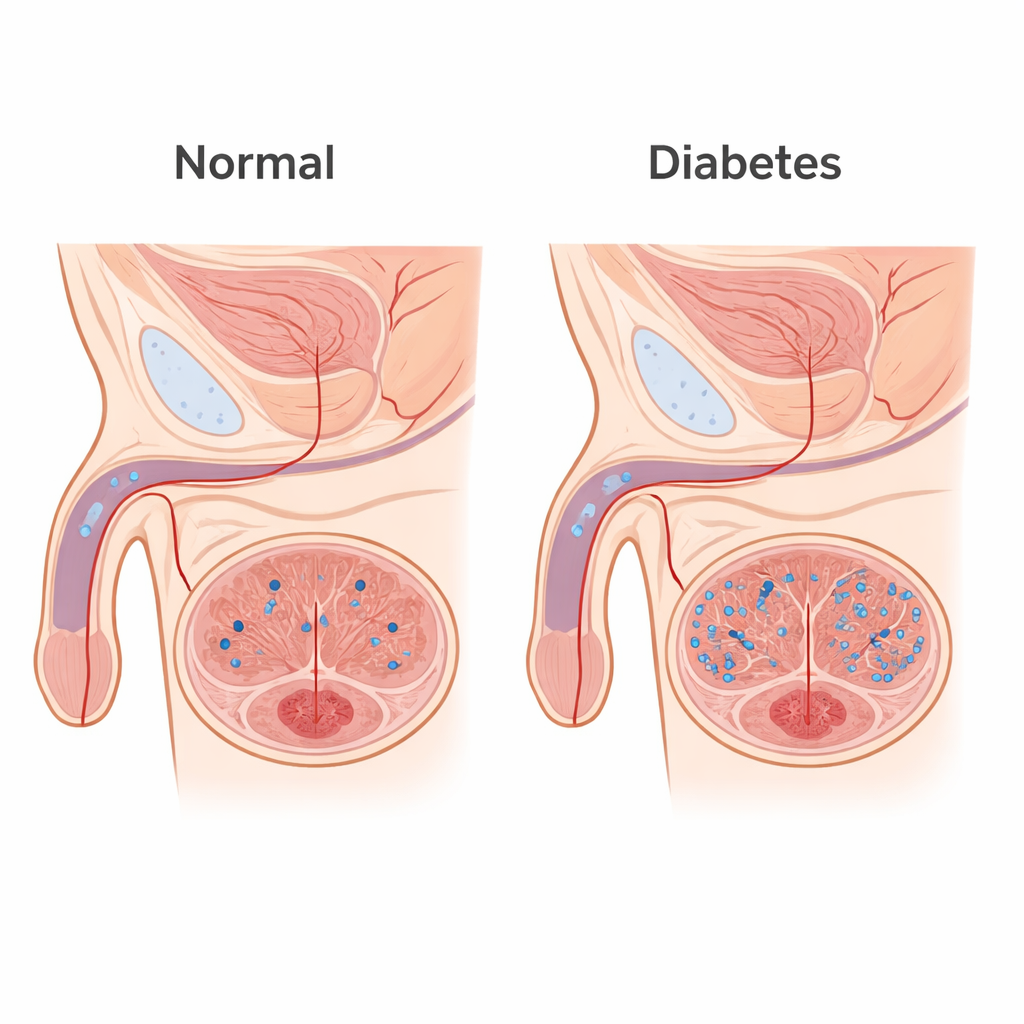
От потери энергии до повреждения ткани
Лактат часто воспринимают как простой «отход» активных мышц, но он также является мощным сигнальным молекулой. У мужчин с диабетической эректильной дисфункцией авторы обнаружили повышенные уровни лактата в крови по сравнению с ровесниками. В диабетической модели мышей лактат в губчатой эректильной ткани полового члена (кавернозе) постоянно возрастал, тогда как давление, создаваемое при эрекции, падало. Здоровым мышам, которым давали дополнительный лактат, в пенильной ткани накапливался лактат, снижалось эректильное давление, а микроскопические исследования показали потерю гладкой мышцы и увеличение коллагенового рубцевания. В культурах гладкомышечных клеток из полового члена высокий лактат замедлял миграцию клеток и переводил их из контрактильного, «готового к работе» состояния в синтетическое, формирующее рубец состояние, частично за счёт чрезмерной активации аутофагии — путей самопереваривания.
Ключевой фермент исчезает
Чтобы понять, почему накапливается лактат, команда сравнила гены, вовлечённые в два противоположных энергетических пути: гликолиз, который производит лактат, и глюконеогенез, который перерабатывает лактат обратно в глюкозу. Признаков гиперактивного гликолиза не обнаружили. Вместо этого центральный фермент глюконеогенеза — FBP1 — последовательно снижался в пенильной ткани у диабетических мышей, у диабетических крыс и в данных одиночных клеток от мужчин с диабетической эректильной дисфункцией. Когда исследователи генетически уменьшили экспрессию Fbp1 у мышей, лактат в половом члене вырос, а эректильные показатели ухудшились, даже при относительно низком общем уровне лактата. В гладкомышечных клетках возвращение функционирующего FBP1 защищало от вредных эффектов высокого лактата, тогда как неактивный вариант FBP1 не давал эффекта. Это показало, что ферментативная активность FBP1 критична для контроля уровня лактата и поддержания здоровой эректильной ткани.
Эпигенетические «замки» и жировые «бирки» на FBP1
Почему FBP1 снижен при диабете? Исследование выявляет двухуровневую систему контроля. Во‑первых, ген Fbp1 зажат на уровне ДНК. Химические метки на гистонах — в частности две «выключающие» метки H3K9me3 и H3K27me3 — накапливаются в промоторе Fbp1 в диабетической пенильной ткани. Эти метки наносятся ферментами вроде SUV39H1 и EZH2 и считываются белком CBX3, образуя репрессивный комплекс, который держит Fbp1 в выключенном состоянии. Препараты и дизайн‑дегрейдеры, направленные на эти ферменты, частично снимали репрессию в клетках, но давали лишь скромное улучшение у диабетических мышей. Во‑вторых, даже при наличии белка FBP1 он может быть отключён жирной модификацией — палмитоилированием на одной аминокислоте, Cys282. Команда идентифицировала фермент ZDHHC13 как палмитоилтрансферазу, прикрепляющую эту жирную группу. Палмитоилирование тонко меняет конформацию FBP1 рядом с критическим остатком, ослабляя его способность перерабатывать лактат. Блокирование Zdhhc13 в клетках и мышах несколько улучшало метаболизм и эректильную функцию, что подчёркивает: ни эпигенетические препараты, ни блокаторы палмитоилирования по‑одиночке недостаточны.
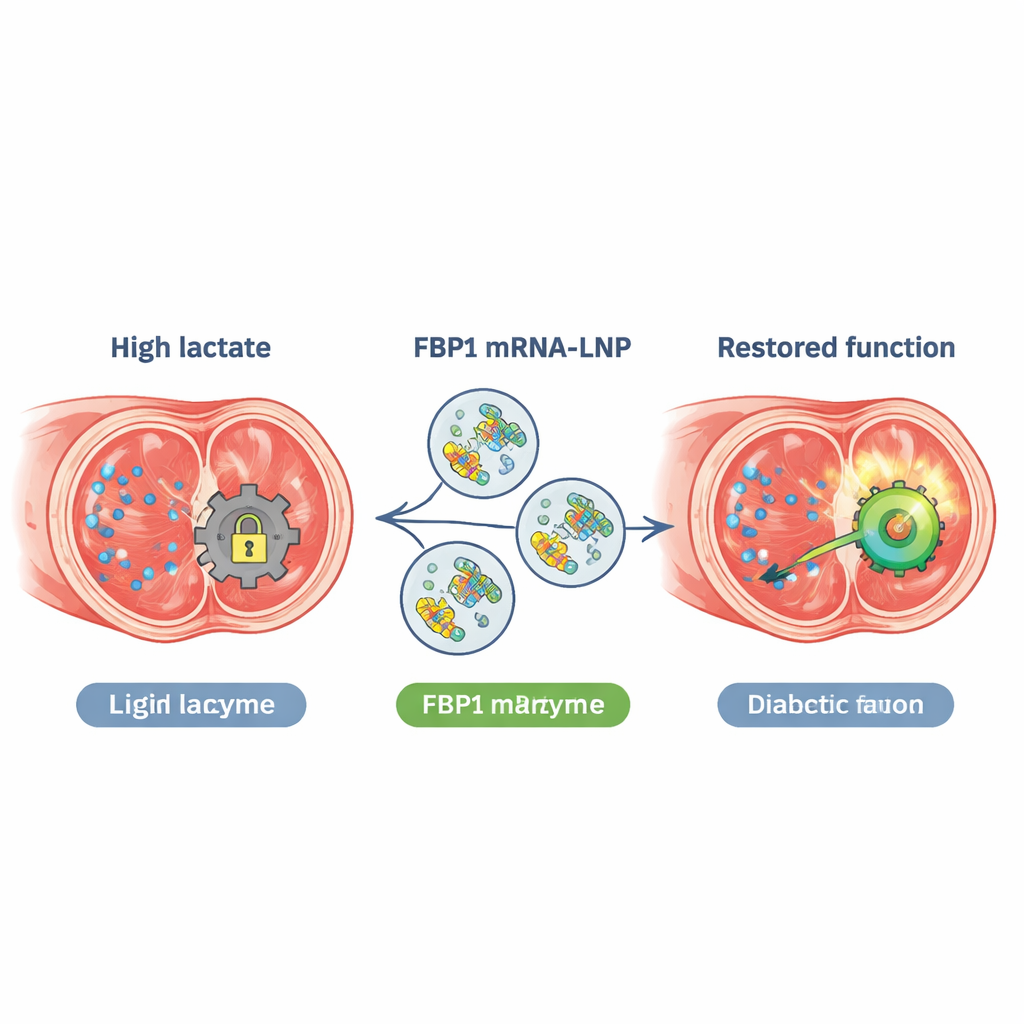
Наночастицы с РНК как набор для ремонта
Чтобы решить обе проблемы одновременно, исследователи сконструировали мРНК, кодирующую вариант Fbp1, устойчивый к палмитоилированию (C282S), и упаковали её в липидные наночастицы — по духу напоминающие мРНК‑вакцины против COVID‑19. При прямой инъекции в пенильную ткань диабетических мышей эти частицы эффективно захватывались гладкомышечными клетками. У обработанных животных наблюдались более высокие уровни белка FBP1, резкое снижение кавернозного лактата, повышение эректильного давления, больше гладкой мышцы и меньше фиброза. Средняя доза оказалась оптимальной; более высокая доза не добавляла пользы. Терапия также нормализовала чрезмерную аутофагию, наблюдавшуюся в диабетических моделях, и улучшала эректильные показатели в нескольких типах диабетических мышей без очевидной токсичности для печени или почек в течение периода исследования.
Что это может означать для будущих методов лечения
Проще говоря, эта работа переосмысляет проблемы с эрекцией при диабете как проблему «кислого» метаболизма в пенильной ткани: слишком много лактата и недостаток функционирующего FBP1. Восстановив непальмитоилированную, активную версию FBP1 именно там, где это необходимо, терапия на основе мРНК в наночастицах восстанавливает энергетический баланс ткани, сохраняет гладкую мышцу и позволяет вернуть нормальную эрекцию — по крайней мере у мышей. Хотя остаются вопросы о долгосрочной безопасности, дозировке и переносимости на людей, исследование намекает на новый класс подходов, который восстанавливает метаболическое здоровье эректильной ткани и однажды может дополнить или помочь пациентам, не отвечающим на существующие препараты.
Цитирование: Xiao, M., Guo, W., Zeng, R. et al. Improving erectile function in diabetic male mice by rescuing depalmitoylated FBP1 to reduce cavernosal lactate. Nat Commun 17, 1740 (2026). https://doi.org/10.1038/s41467-026-68443-y
Ключевые слова: диабетическая эректильная дисфункция, метаболизм лактата, фермент FBP1, мРНК-терапия в липидных наночастицах, гладкая мышца полового члена