Clear Sky Science · ru
Улучшенный in vivo нокаут генов с высокой специфичностью с помощью мультиплексированных sgРНК Cas12a
Более надёжное редактирование генов
Редактирование генов обещает новые возможности для изучения биологии, лечения болезней и даже контроля за насекомыми-вредителями, но в живых организмах оно часто работает не так чисто, как нам рисуют заголовки. Многие клетки избегают редактирования или изменяются лишь частично, что может размывать результаты экспериментов и ограничивать практическое применение. В этой статье описан новый метод на основе CRISPR у плодовой мушки, который делает нокауты генов более полными и более точными, предлагая шаблон для более надёжного редактирования генома в сложных организмах.
Почему стандартный CRISPR часто не дотягивает
Традиционные инструменты CRISPR, такие как Cas9, разрезают ДНК в выбранном месте с помощью одной или небольшого числа направляющих РНК. В живом организме этот подход сталкивается с несколькими препятствиями. Некоторые направляющие просто плохо работают; некоторые сайты-мишени труднодоступны для фермента; и механизмы восстановления ДНК в клетке часто «чинят» разрыв мелкими изменениями, которые не выводят ген из строя. В результате возникает мозаика: соседние клетки в одной и той же ткани могут нести разные мутации или вовсе оставаться нетронутыми. Такая пятнистость затрудняет понимание того, что происходит при полном выключении гена, и создает проблему для приложений, например генной терапии или генетических драйвов, которые должны эффективно действовать в большинстве клеток.
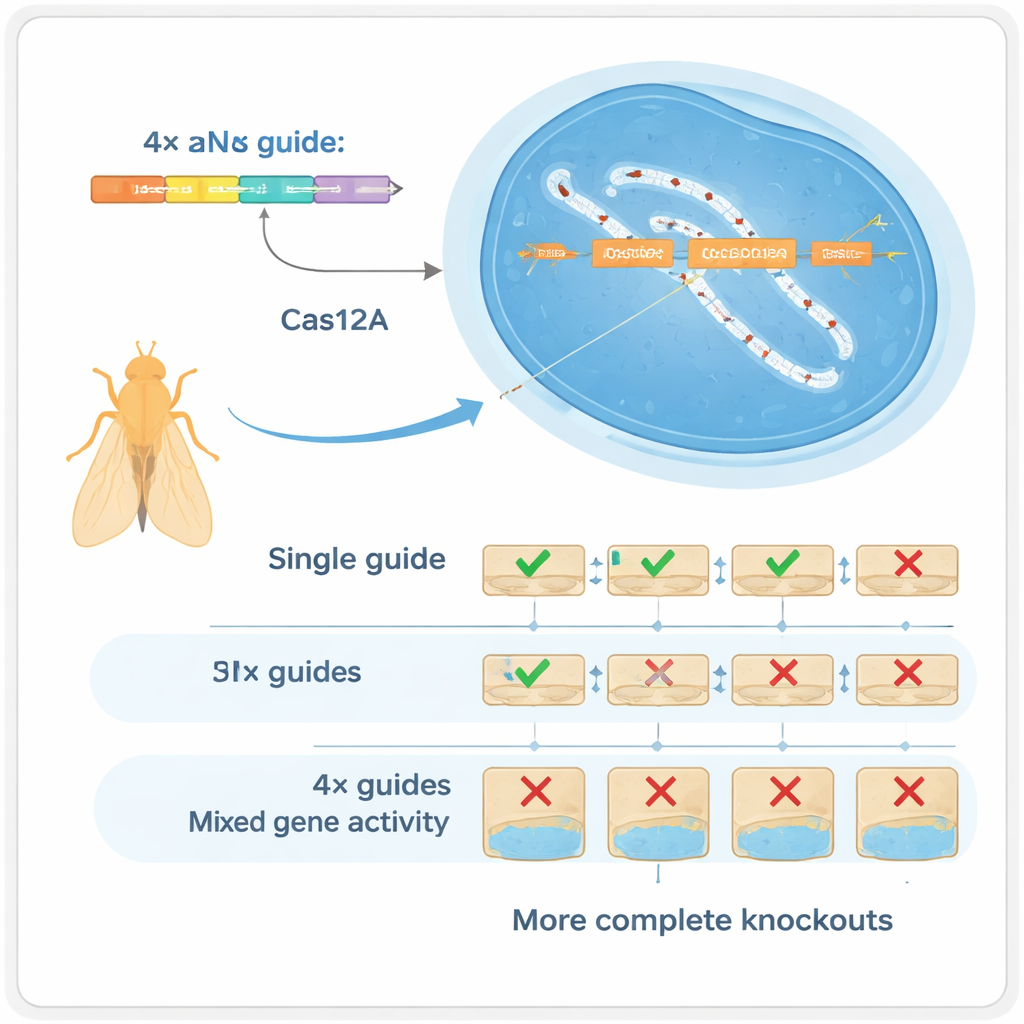
Четыре направляющих лучше, чем одна
Авторы обратились к другому ферменту CRISPR — Cas12a, который удобнее обрабатывает компактные массивы направляющих, чем Cas9. Они создали набор инструментов для Drosophila, в котором каждый ген поражается массивом из четырёх направляющих РНК, закодированных на одном небольшом фрагменте ДНК, который можно массово производить. В тщательно контролируемых тестах они показали, что использование четырёх направляющих на ген кардинально меняет характер образующихся изменений ДНК: вместо преимущественно мелких вставок или делеции в одной точке система часто формирует большие удаления между местами разреза, которые почти всегда разрушают функцию гена. Эта «мультиплексировка» работает двояко: если одна направляющая не срабатывает, другие всё равно могут выполнить задачу (резервирование), а при одновременном срабатывании нескольких направляющих удаляются более крупные участки гена (синергия).
Высокая эффективность без дополнительных побочных повреждений
Увеличение числа разрывов ДНК ставит очевидные вопросы безопасности. Не приведут ли множественные разрезы в одном участке к случайному удалению соседних генов? Не начнут ли направляющие чаще срабатывать в неверных участках генома? Чтобы ответить на это, исследователи измеряли гибель клеток, оценивали влияние на соседние гены и разработали хитрый тест для визуализации событий репарации хромосом — потерю гетерозиготности на больших участках ДНК. Они обнаружили, что группировка четырёх разрезов внутри одного гена хорошо переносится: она не увеличивала гибель клеток по сравнению с обычными подходами на базе Cas9 и редко нарушала соседние гены, если только направляющая не попадала очень близко к регуляторному элементу. Масштабные скрины с более чем 2000 направляющих по третьей части генома мухи показали, что свыше 99% массивов направляющих активны по назначению, в то время как воспроизводимая вне-мишенная активность была ниже 1%, что указывает на очень высокую специфичность даже в мультиплексном режиме.
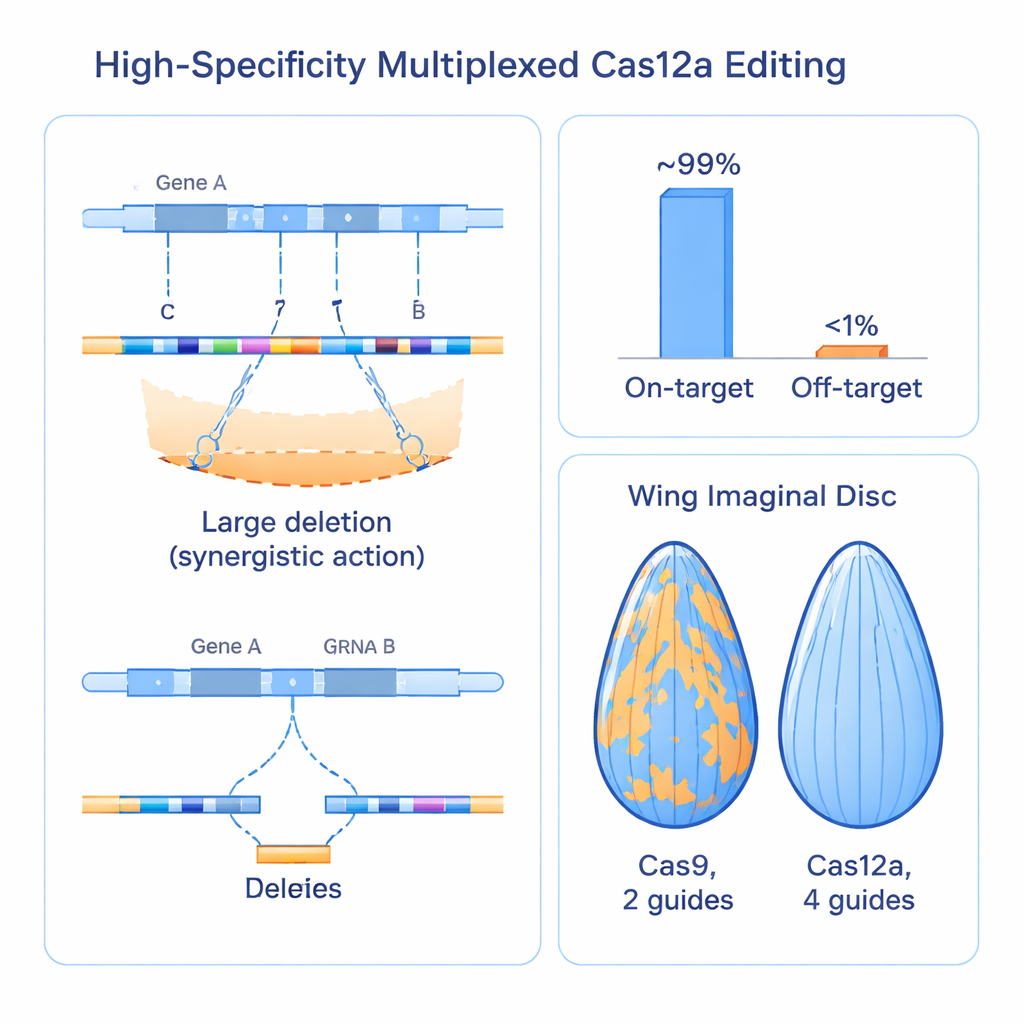
Лучше устоявшихся систем Cas9 в реальных тканях
Чтобы проверить, переносятся ли эти молекулярные улучшения на более ясную биологию, команда сравнила свою систему Cas12a с четырьмя направляющими напрямую с широко используемыми ресурсами на базе Cas9, нацеленными более чем на 100 генов у мухи. В тканях, таких как глаз, кишечник и развивающееся крыло, подход Cas12a давал более сильные и однородные эффекты потери функции по сравнению с Cas9, который часто оставлял очевидные участки нетронутой нормальной ткани. При использовании размера крыла в качестве количественной метрики новая система последовательно вызывала более выраженные и воспроизводимые нарушения роста для известных регуляторов, что показало: некоторые гены, ранее оценённые как слабые или несущественные, на самом деле были пропущены, потому что старые инструменты не инактивировали их полностью. Возросшая мощность метода даже выявила ранее неизвестную, жизненно важную роль гена под названием trade embargo в развитии крыла и выживании.
Что это значит для будущего редактирования генов
Проще говоря, эта работа показывает, как превратить CRISPR из иногда неаккуратного скальпеля в более решающий переключатель для выключения генов в живых организмах. Комбинируя Cas12a с четырьмя направляющими на ген, авторы достигают почти полного нокаута при очень низком уровне непреднамеренных эффектов, причём в формате, который практически масштабируется на сотни генов. Хотя метод разработан у плодовой мушки, лежащие в его основе принципы — использование множества направляющих для резервирования и синергии и тщательная проверка хромосомных побочных эффектов — имеют широкую применимость. Эта стратегия может улучшить фундаментальные исследования, усилить генетические скрины и помочь в разработке более безопасных подходов для будущих медицинских и экологических применений редактирования генов.
Цитирование: Port, F., Buhmann, M.A., Zhou, J. et al. Improved in vivo gene knockout with high specificity using multiplexed Cas12a sgRNAs. Nat Commun 17, 877 (2026). https://doi.org/10.1038/s41467-026-68434-z
Ключевые слова: CRISPR, Cas12a, нокаут генов, Drosophila, специфичность редактирования генома