Clear Sky Science · ru
Контроль рекрутирования теломеразы и защиты концов хромосом независимыми компонентами шелтерина
Как клетки защищают концы своих хромосом
С каждым делением клетки самые кончики хромосом — теломеры — немного укорачиваются. Чтобы не потерять важную генетическую информацию, клетки используют специальный фермент, теломеразу, и набор защитных белков для поддержания этих концов. В этом исследовании изучают, как два из таких белков, TPP1 и POT1, управляют тонким балансом между допуском теломеразы для восстановления теломер и сохранением концов хромосом в защищённом состоянии, чтобы избежать повреждений.
Проблема стареющих концов хромосом
Теломеры действуют как пластиковые наконечники на шнурках, предотвращая снашивание хромосом или их ошибочную интерпретацию как повреждённой ДНК. Если клетка воспримет конец хромосомы как повреждение, это может запустить аварийные системы ремонта, которые сшивают хромосомы или останавливают деление клеток. Одновременно теломеры периодически должны открываться, чтобы теломераза могла их удлинять, особенно в стволовых клетках, которые многократно делятся. Биологи давно предполагали, что теломеры переключаются между «закрытым» защищённым состоянием и «открытым» состоянием, допускающим теломеразу, но сопряжённым с временными сигналами повреждения. Остаётся открытым вопрос: отражают ли эти два состояния разные физические формы теломера или это действительно отдельные механизмы контроля.
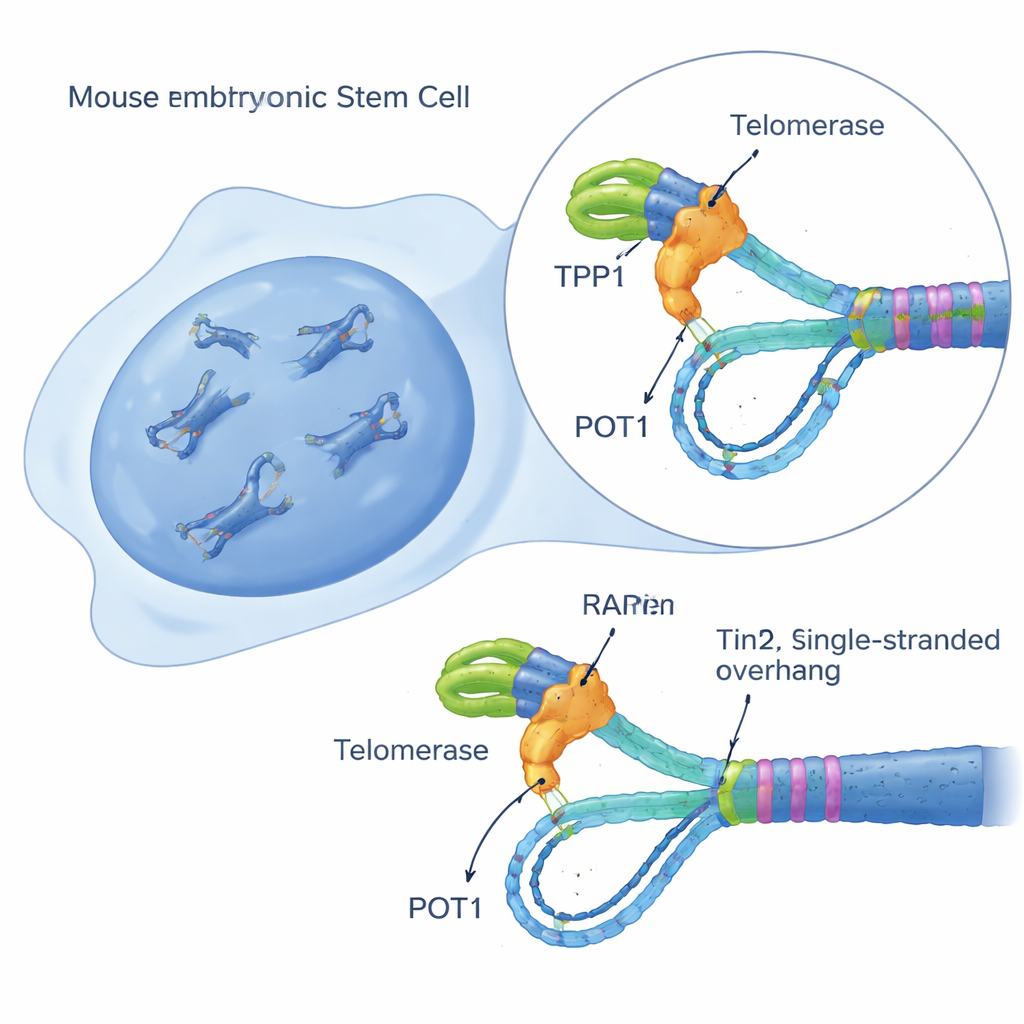
Создание датчика активности теломеразы в одиночной клетке
Чтобы распутать эту задачу, исследователи разработали чувствительный тест в живых клетках, названный iTAP (inducible Telomerase Activity Probing), на мышиных эмбриональных стволовых клетках. Они модифицировали клетки так, чтобы те синтезировали слегка изменённую версию РНК-шаблона теломеразы только при добавлении доксициклина. Этот «мутантный» шаблон заставляет теломеразу добавлять модифицированную последовательность ДНК в теломеры, которую можно визуально отличить от нормальной теломерной ДНК. С помощью флуоресцентных зондов, ДНК-блоттинга и метода секвенирования, обогащающего фрагменты теломер, команда могла непосредственно видеть в каждой отдельной клетке, когда и где теломераза была активна. Важно, что эта система сама по себе не нарушала рост клеток и не вызывала ответ на повреждение, что позволило получать чистые измерения поведения теломеразы в иначе здоровых клетках.
TPP1 привлекает теломеразу, POT1 сдерживает её
Воспользовавшись iTAP, авторы проверили, как два ключевых белка теломер, TPP1 и POT1, влияют на активность теломеразы. Оба входят в более крупный комплекс, известный как шелтерин, который покрывает теломеры. При удалении TPP1 с помощью инструментов генного редактирования мутантные теломерные последовательности почти исчезали, хотя мутантная РНК теломеразы продолжала вырабатываться на нормальном уровне. Дальнейшие эксперименты показали, что TPP1 должен физически связываться с другим компонентом шелтерина, TIN2, чтобы рекрутировать теломеразу; разрушение связи TPP1 с TIN2 выключало активность теломеразы. Удивительно, но нарушение взаимодействия между TPP1 и POT1 не давало такого эффекта, а удаление самого POT1 не снижало активности теломеразы. Наоборот, клетки без POT1 демонстрировали небольшое увеличение количества добавляемой мутантной последовательности, что указывает на то, что POT1 обычно действует как тормоз — ограничивая частоту, с которой теломераза взаимодействует с теломерами, а не способствуя ей.
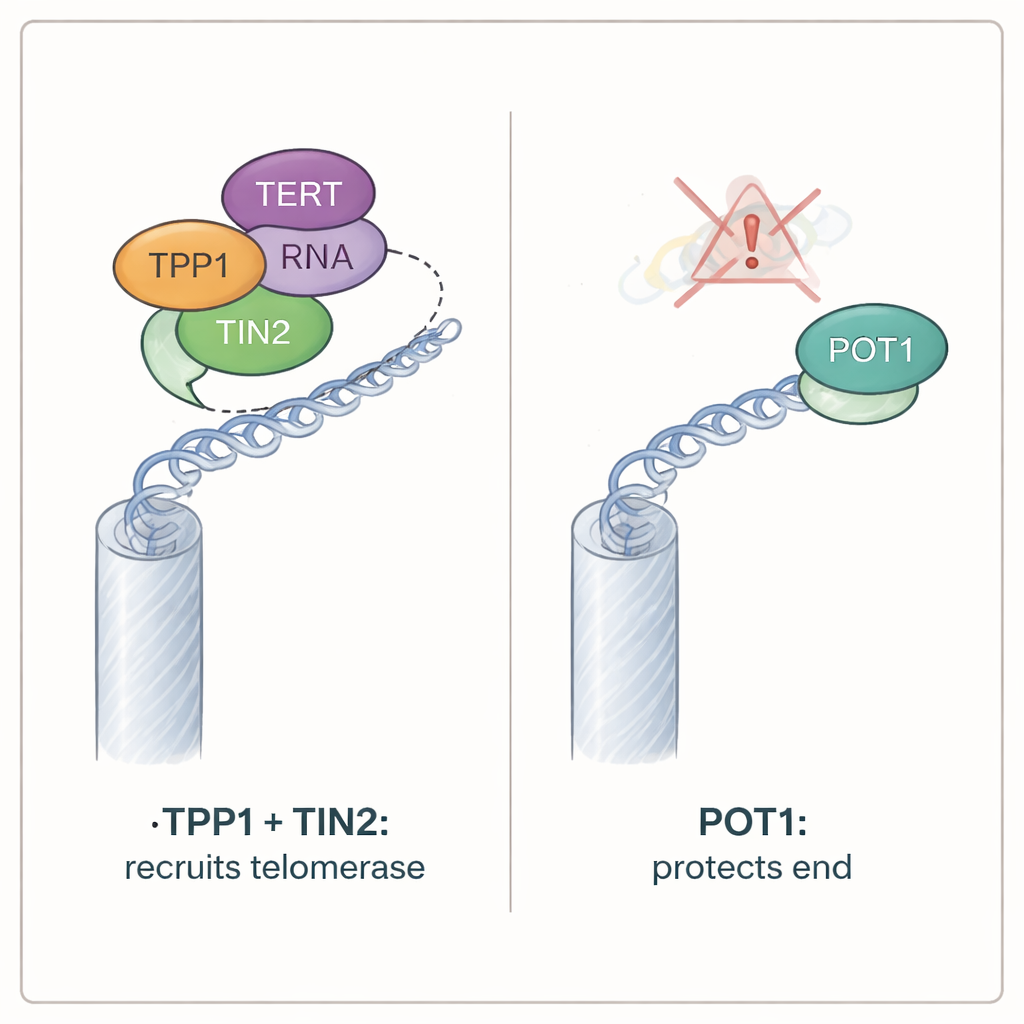
POT1 охраняет концы, тогда как TPP1 может быть заменим
Хотя POT1 оказался ненужным для рекрутирования теломеразы, он оказался жизненно важным для защиты концов хромосом. Клетки, лишённые обеих версий POT1 у мышей, быстро прекращали пролиферацию и демонстрировали все признаки обнажённых теломер: маркеры повреждения ДНК накапливались на концах хромосом, включался чувствительный к повреждениям фермент ATR, и концы хромосом сливались. Напротив, клетки без TPP1 продолжали расти и почти не показывали признаков стресса теломер, хотя у них и была утрачена нормальная активность теломеразы. Дополнительные тесты показали, что защитная роль POT1 зависит от его способности связывать одноцепочечный нависший конец теломер. Мутантные версии POT1, которые не могли захватить эту открытую ДНК, не подавляли сигналы повреждения, даже если они по‑прежнему могли взаимодействовать с TPP1. И наоборот, варианты POT1, способные связывать нависание, но потерявшие привязку к TPP1, всё равно защищали концы хромосом.
Новая модульная картина контроля теломер
Эти результаты опровергают простую модель, где теломеры переключаются между единым «открытым» состоянием для теломеразы и единым «закрытым» состоянием для защиты. Вместо этого исследование показывает, что рекрутирование теломеразы и защита концов контролируются раздельными молекулярными схемами. TPP1, действуя через TIN2, является главным шлюзом, приводящим теломеразу к теломерам, тогда как POT1 независимо охраняет одноцепочечную ДНК на концах хромосом и сдерживает ответ на повреждение. Для неспециалиста вывод прост: клетки не полагаются на единый универсальный выключатель на кончиках хромосом. Скорее они используют отдельные, но скоординированные регуляторы — один, чтобы пропускать теломеразу, и другой, чтобы сохранять концы в безопасности — для поддержания стабильности генома в течение жизни.
Цитирование: Sandhu, R., Tricola, G.M., Lee, S.Y. et al. Control of telomerase recruitment and end protection by independent shelterin components. Nat Commun 17, 1733 (2026). https://doi.org/10.1038/s41467-026-68433-0
Ключевые слова: теломеры, теломераза, стволовые клетки, повреждение ДНК, защита хромосом