Clear Sky Science · ru
Shigella flexneri ускользает от септин-опосредованного клеточно-автономного иммунитета с помощью белковой ADP-рибоксанации
Как некоторые кишечные бактерии обманывают нашу внутреннюю систему безопасности
Тяжелая диарея, вызванная бактериями рода Shigella, остается серьезной проблемой во всем мире, особенно для маленьких детей. Наши клетки не беспомощны: у них есть встроенные механизмы, способные поймать и уничтожить вторгающиеся микроорганизмы. В этом исследовании показано, как Shigella flexneri, одна из основных причин дизентерии, использует молекулярные трюки, чтобы разрушить один из таких механизмов, что помогает бактерии распространяться из клетки в клетку в кишечнике.
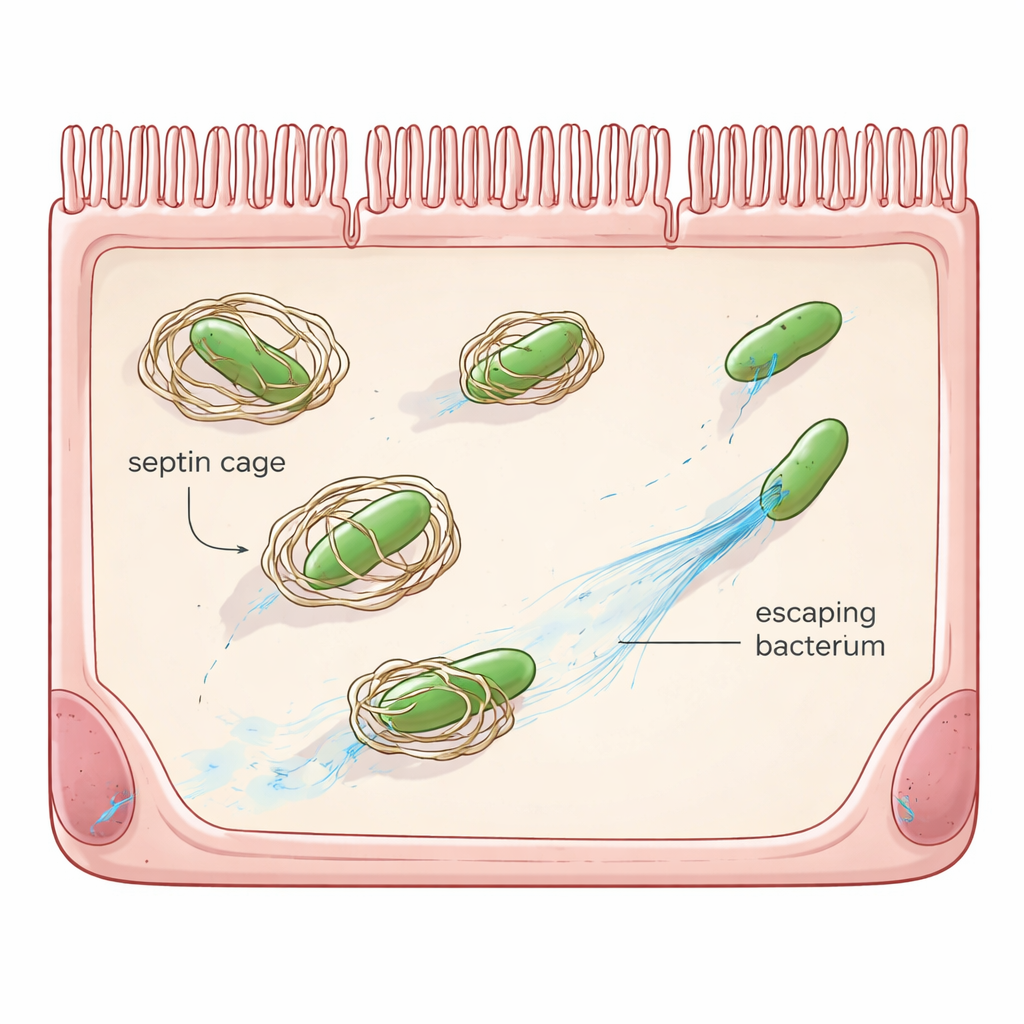
«Самодельная» оборона клетки
Помимо лейкоцитов и антител, многие обычные клетки имеют собственные экстренные системы безопасности, известные как клеточно-автономный иммунитет. Один из таких механизмов опирается на септины — семейство каркасных белков, формирующих кольца и структуроподобные клетки. Когда Shigella проникает в клетку и убегает в желеобразное внутреннее пространство, септины могут собраться вокруг бактерии, лишив ее подвижности и пометив для уничтожения клеточными путями утилизации. Предыдущие работы показали, что у Shigella уже есть одна контрмера — белок OspG, который помечает септины для удаления. Однако даже при отсутствии OspG большинство бактерий все же избегают заключения в клетку, что указывает на наличие у Shigella дополнительных приемов.
Выявление второго бактериального саботажника
Авторы обратили внимание на другую группу белков Shigella, известную как семейство OspC. С помощью глобального картирования белков в человеческих клетках они искали белки хозяина, которые подвергаются химической модификации при наличии OspC. Наряду с известными целью, вовлеченными в синтез белка, они обнаружили, что несколько септинов, особенно SEPT9, постоянно помечаются. Детальные биохимические тесты показали, что три белка OspC могут напрямую присоединять небольшой энергоемкий фрагмент, происходящий из молекулы NAD, ко многим сайтам в септинах. Эта химическая модификация, называемая ADP-рибоксанацией, представляет собой особый необратимый вариант более распространенной белковой модификации.
Разрушение белкового каркаса изнутри
Чтобы понять, как эта химическая метка ослабляет клеточную оборону, команда сосредоточилась на SEPT9. Септины обычно формируют упорядоченные цепочки из восьми звеньев, которые затем выстраиваются в филаменты и, наконец, в полные клетки вокруг бактерий. Исследователи обнаружили, что одна конкретная позиция в SEPT9, аминокислота аргинин 561, является основным сайтом для ADP-рибоксанации во время инфекции. Структурные работы и эксперименты по рекомбинации с очищенными белками показали, что этот сайт находится на критической контактной поверхности, где два звена SEPT9 сцепляются друг с другом. Когда этот аргинин химически модифицирован — или заменен на остаток, имитирующий добавленный отрицательный заряд — октамерные цепочки распадаются на более мелкие фрагменты и лишаются способности формировать стабильные филаменты.
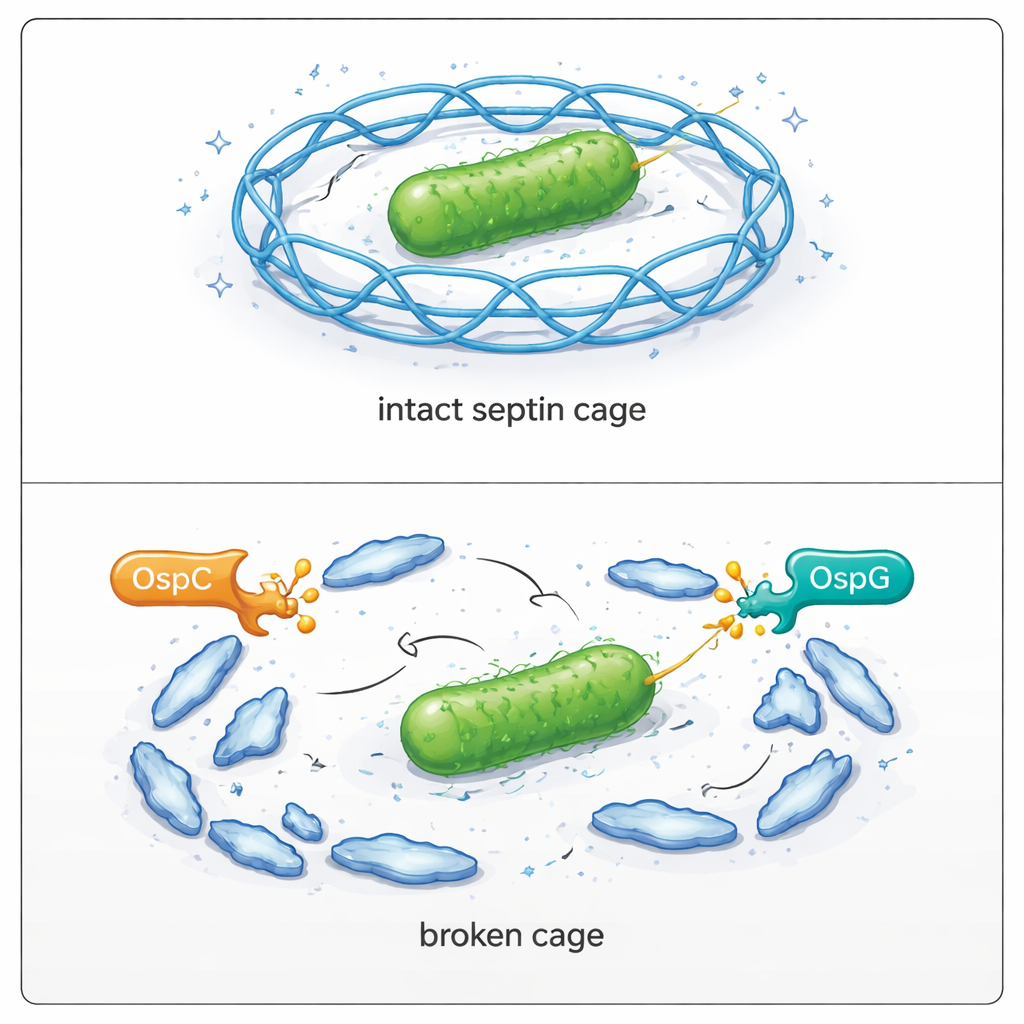
Наблюдая, как клетки-«клетки» дают сбой внутри инфицированных клеток
Затем команда вернулась к живым клеткам, чтобы увидеть последствия. В человеческих клетках, инфицированных обычной Shigella, лишь меньшинство бактерий оказывалось внутри септиновых клеток. При генетическом удалении всех белков OspC доля заключенных бактерий почти удвоилась. Удаление OspG давало аналогичный эффект, а удаление одновременно OspC и OspG еще больше увеличивало формирование клеток и значительно нарушало способность бактерий распространяться по клеточному слою. Повторное введение активных белков OspC в мутантные штаммы восстанавливало их способность избегать клеток, размножаться и образовывать большие бляшки. Микроскопия подтвердила, что когда SEPT9 не может быть модифицирован в позиции аргинина 561, он эффективно входит в клетки; при же модификации OspC образование клеток вокруг бактерий резко снижается.
Что это означает для борьбы с Shigella
Проще говоря, эта работа показывает, что Shigella несет пару согласованных молекулярных инструментов, предназначенных для того, чтобы распахнуть прутья внутриклеточной «тюрьмы». OspC напрямую ослабляет белковые строительные блоки, необходимые для сооружения септиновых клеток, в то время как OspG способствует их удалению другим химическим путем. Вместе эти стратегии позволяют бактериям вырваться, перемещаться внутри клеток и проникать в соседние. Понимание этих точных механизмов побега не только углубляет наше представление о работе клеточно-интринсивного иммунитета, но и указывает на новые терапевтические направления: препараты, блокирующие OspC или защищающие ключевые контакты септинов, могли бы помочь восстановить естественную способность клетки захватывать и убирать этого опасного патогена.
Цитирование: Tang, Z., Xian, W., Özbaykal Güler, G. et al. Shigella flexneri evades septin-mediated cell-autonomous immunity via protein ADP-riboxanation. Nat Commun 17, 1727 (2026). https://doi.org/10.1038/s41467-026-68425-0
Ключевые слова: Shigella, септиновые клетки, клеточно-автономный иммунитет, факторы вирулентности бактерий, ADP-рибозилирование